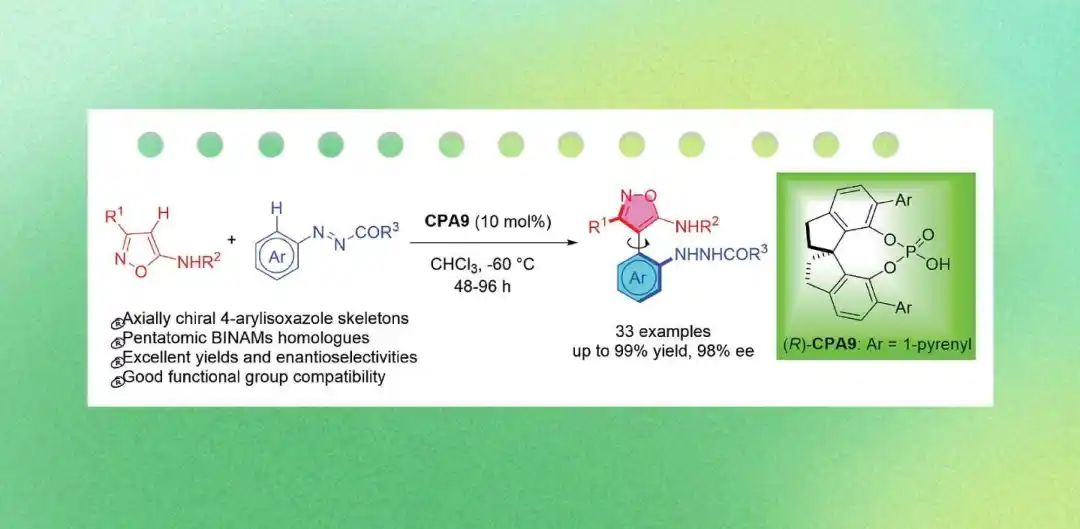
导语
轴向手性分子的手性源于单键的旋转受阻,它们广泛存在于具有生理活性的药物分子、手性农药以及天然产物中,并且在不对称催化领域有着广泛的应用。其中,官能团化的轴向手性联芳基化合物,如1,1'-联萘二胺(BINAM)已被广泛用于手性配体和手性催化剂的开发。然而,通过不对称催化方法合成BINAM及其类似物的发展仍较为缓慢。近年来,多个课题组在轴手性二胺化合物的不对称合成方面取得了突破性进展。例如:List课题组和Kürti课题组分别报道了手性磷酸催化的联芳基肼类化合物的[3,3]-sigma重排反应,用于BINAM化合物的不对称合成(J. Am. Chem. Soc. 2013, 135, 7414;Angew. Chem. Int. Ed. 2013, 52, 9293);谭斌课题组和张志鹏分别发展了手性镍-双噁唑啉配合物和手性铜-菲罗啉配合物催化的偶氮萘与2-萘胺的不对称交叉偶联反应,用于构建手性BINAM化合物(Nat. Catal. 2019, 2, 314;Nat. Commun. 2022, 13, 4735);谭斌课题组和杨晓瑜课题组分别发展了BINAM类化合物的动力学拆分方法(Angew. Chem. Int. Ed. 2014, 53, 3684;Angew. Chem. Int. Ed. 2020, 59, 23598)。值得一提的是,Lassaletta和Hornillos团队运用动态动力学反应策略实现了联芳基缩醛胺的催化转移氢化反应,可以高效地得到一系列手性BINAM类似物(ACS Catal. 2021, 11, 4117)。
目前发展的合成轴手性二胺化合物的方法采用的都是六元环芳烃作为底物,具有五元杂环骨架的轴手性二胺化合物研究相对较少,值得深入研究。究其原因,主要是五元杂芳环的轴两侧邻位基团与中心轴的距离较远,构象稳定性较差,手性轴的旋转能垒较低;如果适当增加邻位基团的位阻,可提高手性轴的稳定性,同时又会导致反应的活性降低。因而,其不对称构建相对困难,具有较大挑战。
长沙理工大学罗维纬和周俊团队长期致力于通过烯胺催化构建五元杂芳环化合物的研究(Chem. Sci., 2020, 11, 9386;ACS Omega 2022, 7, 45341)。在前期工作的基础上,团队发展了手性磷酸催化的5-氨基异噁唑与偶氮萘的不对称交叉偶联反应(图1),用于构建具有萘-异噁唑骨架的轴手性杂芳基二胺化合物,相关研究成果在线发表于Organic Letters(DOI: 10.1021/acs.orglett.4c00440)。
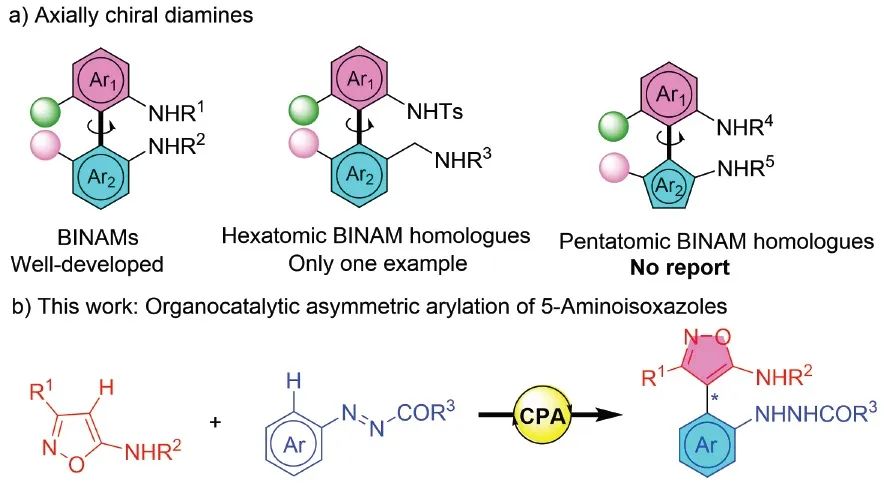
图1. 研究背景(来源:Organic Letters)
前沿科研成果
不对称合成轴手性杂芳基二胺化合物
首先,作者以偶氮萘1a和5-氨基异噁唑2a为标准底物进行条件的筛选。从表1中可以看出,即使在没有催化剂的条件下,该反应仍然可以缓慢地进行,说明要想实现不对称催化反应,需要找到一个优异的催化体系克服背景反应的影响。作者猜想偶氮萘和异噁唑底物的官能团是很好的氢键受体和供体,于是考察了手性磷酸的催化效果。结果表明,具有联萘骨架的手性磷酸有一定的催化效果,可以给出72-99%的收率和19-62% ee的对映选择性。这些结果表明手性磷酸可以很好地催化偶氮萘和5-氨基异噁唑的不对称交叉偶联反应。于是,作者尝试了南开大学周其林院士团队发展的螺二氢茚手性螺环骨架衍生的手性磷酸催化剂(谢建华,周其林,神奇的手性螺环配体,化学学报,2014, 72, 778)。令人惊喜的是,手性螺环磷酸(R)-CPA9表现出最优的催化活性,可以给出高达99%的收率和97% ee的对映选择性。
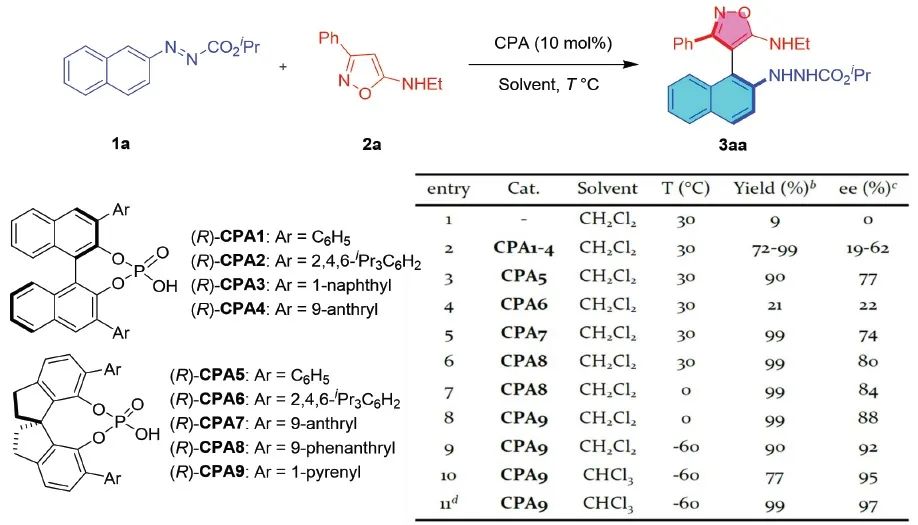
表1. 反应条件的筛选(来源:Organic Letters)
在最优的反应条件下,作者首先对偶氮萘化合物进行了底物扩展。从表2可以看出,偶氮基上连有不同酯基或者酰基官能团的底物均能以较好的收率以及优异的对映选择性获得相应的目标产物(3aa-3ga)。同时,C-6位连有不同的取代基也是可行的,除了供电子基团的对映选择性有所降低(3ja, 81% ee)。除此之外,对于C-7位连有供电子基的底物,反应收率和对映选择性均有所下降(3ka, 63%, 81% ee)。作者猜测,除了供电子效应对反应底物的对映选择性有影响之外,C-7位的空间位阻效应也一定程度地影响着整个反应的收率。
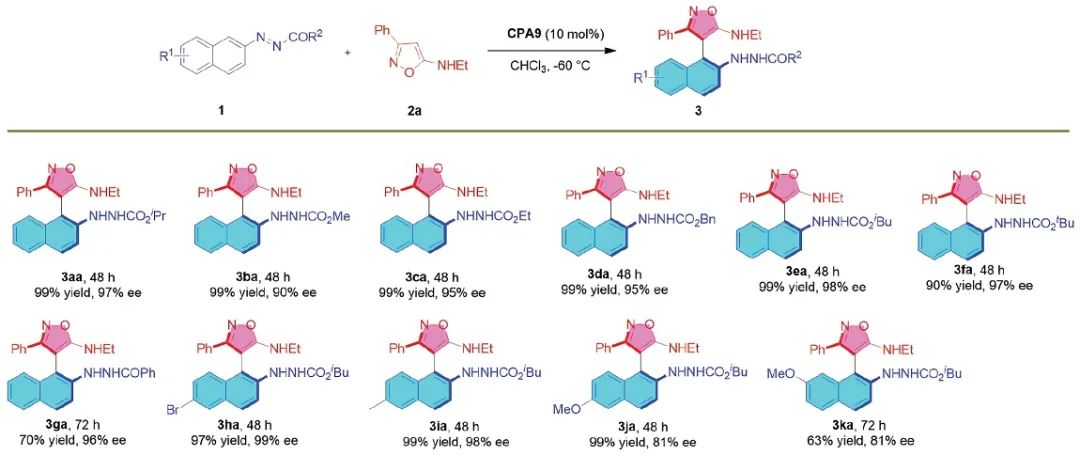
表2. 偶氮萘底物的扩展(来源:Organic Letters)
随后,作者对5-氨基异噁唑底物进行了底物普适性的考察(表3)。实验结果表明,在模板反应条件下,氮原子上不同的烷基取代基均可以以良好的收率和对映选择性得到相应的目标产物(3ab-3ae)。然而,当氮原子连有Boc基团时,该底物的催化反应不能发生,说明异噁唑环C-4位的亲核性受C-5位氮原子上吸电子取代基的影响(3af)。另外,异噁唑环C-3位上无论是吸电子取代的苯环、供电子取代的苯环、多取代的苯环、稠芳环、杂芳环、烷基等均可以很好兼容,以较高收率和优异的立体选择性得到目标产物(3ag-3aw)。有趣的是,当氮原子没有保护基的时候,异噁唑环C-4位的亲核性并没有受到影响,反应仍能以中等的收率和较高的立体选择性得到目标产物(3ax)。
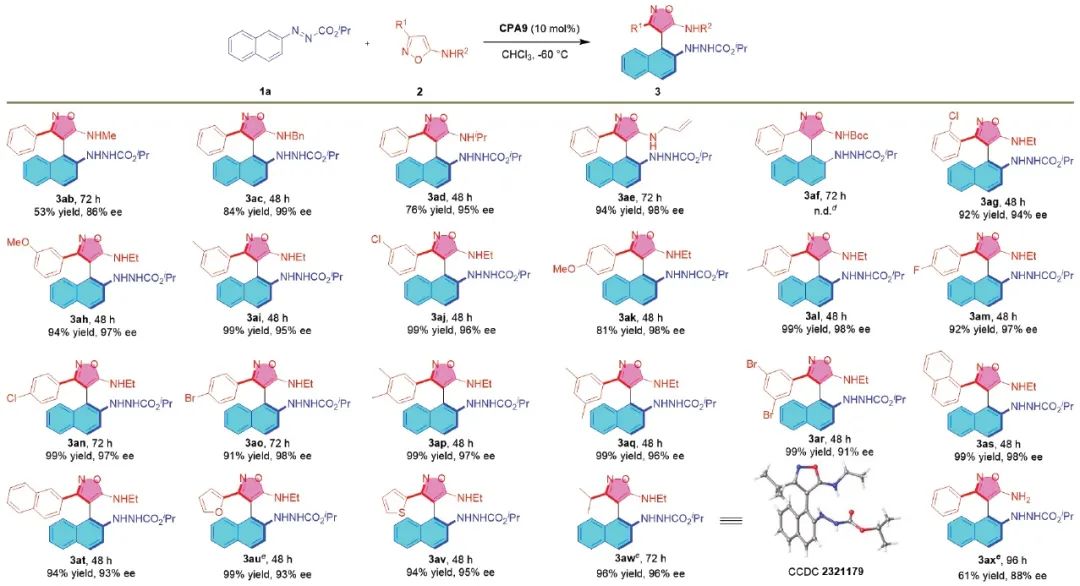
表3. 5-氨基异噁唑底物的扩展(来源:Organic Letters)
为了探究该催化反应的应用潜力,作者进行了克级规模放大实验(表4)。在标准条件下,以偶氮萘1a(2.2 mmol)和5-氨基异噁唑2a(2.0 mmol)为起始原料,催化反应能够以99%的收率和93% ee的对映选择性得到目标产物3av。经过简单的重结晶操作,可以得到近乎光学纯的目标产物。随后,催化产物通过简单的脱氢氧化反应,又可以重新获得含有偶氮基官能团的轴向手性化合物6。当然,该产物的ee值有所降低,作者猜测是偶氮基团相对于肼基的体积要小一些,导致手性轴的旋转能垒降低,出现部分消旋化现象。
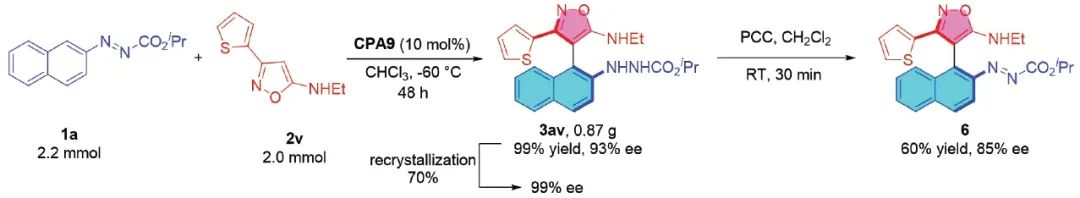
表4. 实用性考察(来源:Organic Letters)
为了进一步了解反应机理,作者做了一些机理考察实验(表5)。首先,作者进行了非线性效应研究,发现产物的ee值和手性磷酸催化剂的ee值是线性相关的,表明决定产物对映选择性的过渡态中只有一个分子的手性磷酸催化剂参与了反应,活性催化剂倾向于以单体形式存在。随后,作者分别对三种不同类型的异噁唑底物进行对比控制实验。当氮原子上连有两个氢原子的时候,催化反应虽然能够发生,但是收率并不是很高;当其中的一个氢原子被乙基取代的时候,催化反应的活性和对映选择性得到很大的提升;然而,当氮原子上连有两个乙基取代基的时候,催化反应不能够发生。因此,作者猜测,异噁唑底物的N-H键和偶氮萘的氮原子可能分别通过与双功能手性磷酸产生氢键作用,从而能够控制反应的活性及对映选择性。同时,手性磷酸扮演着手性质子梭的作用,实现氢原子的快速转移,从而得到目标产物。
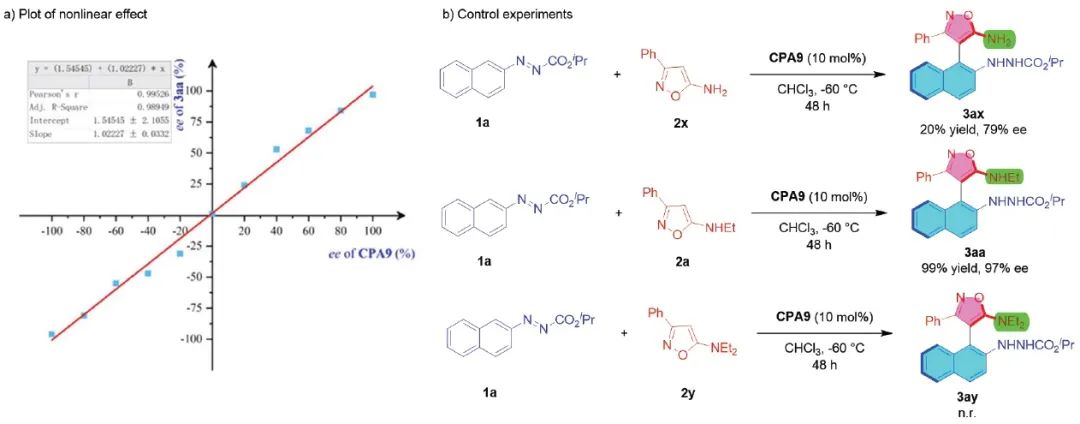
图5. 机理考察实验(来源:Organic Letters)
最后,作者对催化产物3av进行了手性轴稳定性的研究。在90°C条件下,该手性轴的消旋能垒和半衰期分别达到32.4 kcal·mol-1和20.5 h,远高于一般构型稳定的轴手性分子(>28 kcal·mol-1),充分表明作者设计的轴手性骨架具有很高的化学稳定性和构型稳定性,表现出良好的应用前景。
综上所述,该工作报道了手性磷酸催化的偶氮萘与5-氨基异噁唑底物的不对称交叉偶联反应,合成了一系列含有异噁唑结构的轴手性杂芳基二胺化合物。该反应操作简单、反应条件温和兼具良好的底物普适性,为轴向手性二胺化合物的高效构建提供了新思路。该工作以“Organocatalytic Atroposelective Construction of Pentatomic Heterobiaryl Diamines through Arylation of 5-Aminoisoxazoles with Azonaphthalenes”为题发表在Organic Letters(DOI: 10.1021/acs.orglett.4c00440)。研究工作得到国家自然科学基金(No. 22201022),湖南省自然科学基金(Nos. 2021JJ40563, 2023JJ40012),湖南省教育厅优秀青年项目(No. 21B0312)和细胞化学湖南省重点实验室开放基金项目(No. 2020xbhx02)的大力资助。长沙理工大学化学化工学院研究生郭欢欢完成主要实验工作,罗维纬博士和周俊教授为论文的共同通讯作者。课题组实验条件优越,经费充足,氛围融洽,欢迎有志于有机合成化学方法学研究的优秀学生报考本课题组!