摘要
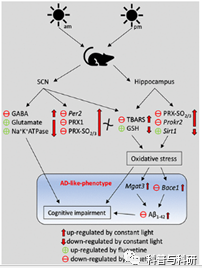
越来越多的证据表明阿尔茨海默病的昼夜节律紊乱;然而,它们之间的因果关系并不清楚。长期持续光照有效地扰乱了大鼠的昼夜节律。基于以前的出版物,我们假设慢性持续光照可能显著促进大鼠AD样表型的发展,氟西汀(Flx)治疗可能保护大脑免受其害。成年雄性大鼠暴露于正常的光暗周期、恒定光(L1)、恒定暗和L1+Flx(5毫克/千克/天,ZT5)四个月。昼夜节律分子标记的表达:Per2转录本;过氧化还原蛋白-1 (PRX1)和过氧化过氧化还原蛋白(PRX-SO2/3)的蛋白表达在L1大鼠视交叉上核(SCN)中显著失调,与氟西汀合用可阻止这种失调。谷氨酸和γ-氨基丁酸水平失调,并且在L1大鼠的脊髓神经和海马中观察到氧化损伤。
氟西汀治疗对LL大鼠的氧化损伤有保护作用。持续光照还会损害大鼠在Y迷宫、莫里斯迷宫和新物体识别试验中的表现,氟西汀可防止这种情况。在L1大鼠海马中观察到可溶性Aβ1-42水平显著升高,这与Bace1和Mgat3转录物的上调密切相关。此外,抗衰老基因Sirt1表达下调,海马神经元损伤指标Prokr2表达上调。氟西汀挽救了Aβ1-42上调和AD相关基因的失调。我们的发现表明,长期持续光照对昼夜节律的破坏可能导致阿尔茨海默病的进展,这可以通过氟西汀治疗来预防。
关键词:昼夜节律,视交叉上核,海马,过氧化还原蛋白,过氧化氢酶2,Bace1,Mgat3
介绍
阿尔茨海默病(AD)影响全球超过4400万人,预计到2050年患病率将达到1亿。我们目前对AD的理解是,β-淀粉样蛋白(Aβ)肽的过量和聚集是AD病理学的核心。β-位点淀粉样蛋白前体裂解酶-1 (BACE1)是Aβ合成的限速酶,其过度活跃是a d的决定因素之一衰老是阿尔茨海默病发病的主要危险因素,这可能因不良的生活方式选择而加剧。流行病学研究表明轮班工作与认知缺陷、颞叶相关的空间记忆缺陷和代谢综合征有关。越来越多的证据表明昼夜节律紊乱与AD样病理有关;但是,两者之间的因果关系还没有完全弄清楚。最近对这种关系进行了详细的回顾。昼夜节律是所有生命形式的基础,它们在分子水平上表现为时钟蛋白的振荡表达。哺乳动物的昼夜节律钟可以分为两个齿轮,即转录(或转录翻译反馈环,TTFL)和非转录振荡。TTFL包含一组时钟基因,其中周期(Per)基因被设置在自我调节环路中。非转录振荡产生于节律性氧化还原状态,被观察为过氧化还原蛋白-1 (PRX1)的振荡表达,PRX1是一种巯基依赖的过氧化物酶,在所有王国和门中都是保守的。所有哺乳动物细胞都表现出昼夜节律,并由位于下丘脑腹侧两侧的视交叉上核(SCN)同步化。
短链氯化石蜡可以通过光或非光的线索被带到地球物理时间,这种线索被称为“光信息”,然而,光信息在短链氯化石蜡的传输中起着主导作用。光通过Per2基因重塑。SCN通过可扩散的神经肽(包括前激动素-2 (PK2))带动神经元和外周时钟。PK2的表达受TTFL和光的双向控制。前激动素-2受体-2 (Prokr2)基因编码PK2的G蛋白偶联受体,该受体对行为昼夜节律的调节至关重要,它广泛表达于SCN的靶区,包括海马。昼夜节律可能因基因突变而内源性中断或因不合时宜的光暴露而外源性中断。不合时宜的光暴露对昼夜节律有许多有害影响;然而,这些影响从轻微到严重,取决于夜间光照的强度和持续时间。不当暴露在180 lx强度的光线下足以导致人类昼夜节律的相移。此外,长期暴露在200 lx强度以上的恒定光线下会完全扭曲啮齿动物的活动、体温和时钟基因表达的昼夜节律。恒定光线暴露会导致SCN中的异步神经元放电,从而导致节律的“分裂”并使中枢时钟心律失常。慢性恒定光线作为不可避免的应激源,会使SCN神经元失去同步,而不会损害其产生昼夜节律的能力。神经元同步性的丧失导致神经元电振幅的衰减和神经元对外围时钟的相位控制的丧失。SCN的相位控制的丧失随后会导致进食节律、能量消耗和胰岛素敏感性的完全丧失,与老龄小鼠相似。
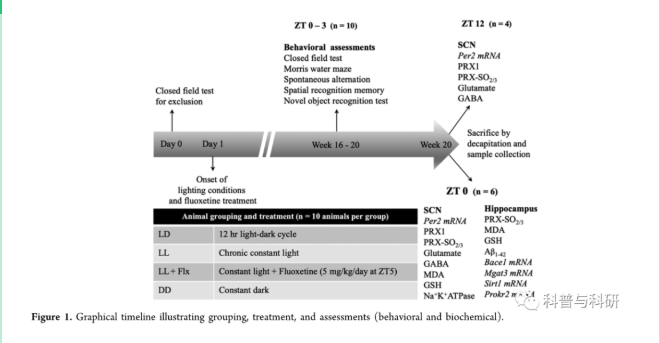
我们以前已经表明,在持续光照下暴露两个月会导致认知障碍,并促进Wistar大鼠外源性β-淀粉样蛋白42 (Aβ42)亚病理浓度的聚集。我们还表明氟西汀可以挽救Aβ42的聚集。首先,SCN可以通过血清素能信号被非热信号携带。氟西汀是一种传统的血清素再摄取抑制剂,已被证明可以诱导啮齿动物的相位/昼夜节律变化。众所周知,氟西汀可以通过影响啮齿动物SCN中的神经元放电和Per2表达来诱导昼夜节律相位变化,并且这种作用仅限于白天给药。扩展了我们先前的发现,即两个月的暴露加速了Aβ42的聚集和认知缺陷,我们假设四个月的恒定光暴露可以在没有外源性Aβ42给药的大鼠中诱导Aβ样表型,并且伴随的氟西汀治疗可以防止昼夜节律的破坏并从而防止Aβ样表型的发展。在这里,我们报道了慢性恒光和氟西汀治疗对认知能力的影响;昼夜节律(Per2、PRX1和PRXSO2/3)和神经元失调的分子标记;SCN和海马中的氧化损伤标记物;和大鼠海马中的阿尔茨海默病样病理学标记物(图1)。
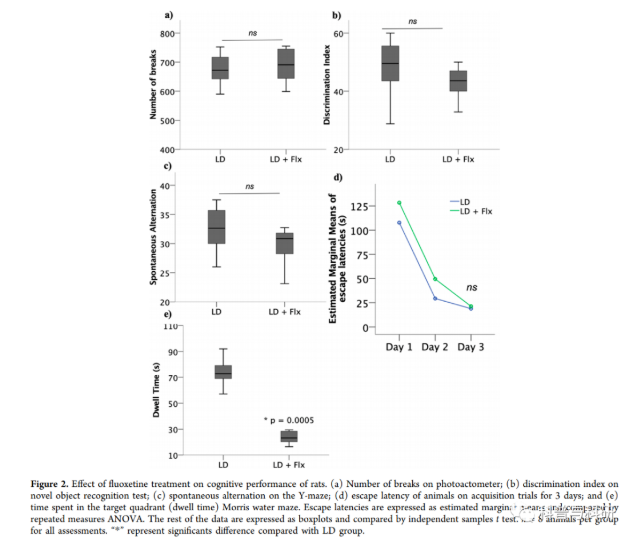
结果和讨论进行了一系列的行为测定,以评估氟西汀对大鼠认知能力的影响,并排除潜在的混杂因素。本身组(光暗周期(LD) +氟西汀(Flx))服用氟西汀(5毫克/千克/天,T5)四个月,认知表现与注射载体的LD组进行比较。数据通过独立样本t检验进行比较。光感受器自发运动活性显示氟西汀治疗无效:t(14)= 0.413,p = 0.686。负的t值表明LD + Flx大鼠的自发运动活性比LD动物中等(尽管不显著)高(图2a)。新物体识别试验的辨别指数也显示氟西汀治疗无效:t(14) = 1.088,p = 0.295(图2b)。Y-迷宫的自发交替显示氟西汀治疗没有显著效果:t(14) = 1.404,p = 0.182(图2c)。此外,习得性学习显示氟西汀治疗对受试者因素(时间)有显著影响:维尔克氏λ= 0.030,F(2,13) = 209.021,p < 0.001;但不包括受试者之间和受试者之间的因素(氟西汀治疗和时间),维尔克氏λ= 0.654,F(2,13) = 3.438,p = 0.063(图2d)。这表明在习得试验过程中,两组都获得了学习;而LD组与LD + Flx组之间无显著差异。相比之下,探针试验的记忆回忆显示氟西汀治疗对目标象限的时间(停留时间)有显著影响:t(14) = 11.443,p = 0.0005(图2e)。类似地,先前的一项研究报告称,氟西汀治疗15天会损害莫里斯水迷宫中未受压迫小鼠的空间记忆回忆,但不会损害习得性学习或新物体识别。由于在记忆评估中未发现混杂因素,因此对动物进行了康复,并且没有对LD + Flx组进行进一步评估。
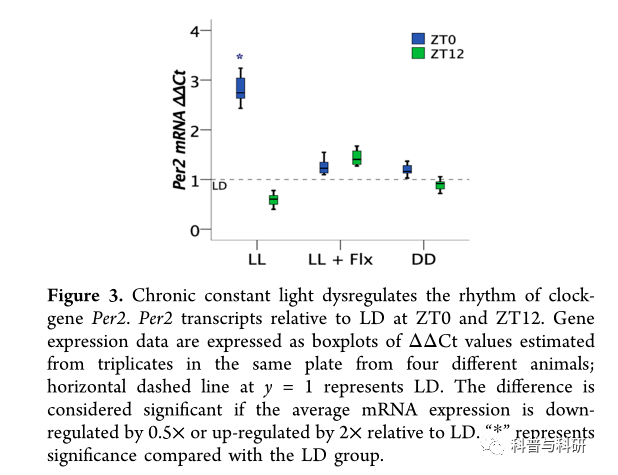
慢性恒定光失调昼夜节律的分子标记。Per2在SCN中响应光的提示重塑TTFL。在LD条件下,Per2的转录在健康大鼠的SCN中呈全向振荡,其谷值与主观的早晨一致,而顶相与主观的夜晚一致。恒定的光减弱了啮齿动物中Per2表达的节律并导致其翻译产物的组成性升高水平,PER2.25We我们使用qRT-PCR测量了在ZT0和ZT12的SCN中PER2转录物的表达。在ZT0,Ct > 2时,L1大鼠的Per2显著上调(图3)。相反,在ZT12,Per2转录物相对较少;然而,差异不显著,δδCt > 0.5(图3)。请注意,y = 1处的水平虚线代表LD。这一发现与以前的研究相一致,即与LD大鼠相比,在L1 大鼠中Per2基因的“平线”表达的振幅衰减在ZT0处为高,在T12处为低。25在恒定黑暗(DD)下,大鼠的Per2转录物水平与LD大鼠相当;然而,适度的变化可能归因于两组的昼夜节律相位差。此外,每日氟西汀治疗可防止持续光照(L1+Flx)下大鼠Per2表达的失调。L1+Flx大鼠的Per2转录物水平与ZT0和ZT12的LD大鼠相当(图3)。
SCN在细胞内氧化还原状态下表达自我维持的节律。氧化还原振荡通过一种非描述性机制调节其兴奋性,从而影响SCN的夹带。过氧化还原蛋白是氧化还原振荡的保守标记物。13我们使用蛋白质印迹分析估计了ZT0和ZT12大鼠SCN中过氧化还原蛋白-1 (PRX1)的水平。在ZT0,F(3,12) = 13.428,p = 0.0005,η2= 0.77时,发现光照条件对PRX1表达有显著影响;在ZT12,F(3,12) = 11.887,p = 0.001,η2= 0.748。多重比较显示,与LD相比,L1大鼠在ZT12的PRX1表达显著升高,但在ZT12的PRX 1表达没有显著升高(图4a)。相比之下,氟西汀治疗在ZT0时与LD和LL组相比,显著降低了LL + Flx大鼠SCN中PRX1的表达(图4a),但在ZT12时没有,LL对LL + Flx,p = 0.368。有趣的是,氟西汀治疗似乎逆转了持续光照下大鼠PRX1的节律(图4a)。
还观察到对PRX1表达百分比变化的显著影响,F(3,12) = 21.021,p = 0.0005,η2= 0.84(图4b)。L1大鼠的PRX1节律丧失,表现为表达的微小变化,与LD大鼠有显著差异(图4b)。有效防止了节奏的丧失;然而,氟西汀治疗逆转了节律,LL vs LL + Flx,p = 0.0005(图3)。氟西汀对中枢神经系统PRX1节律的影响值得进一步研究。
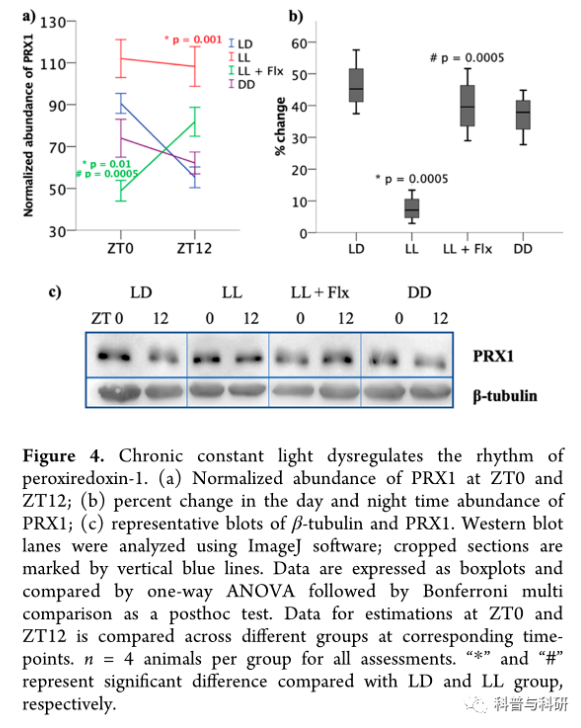
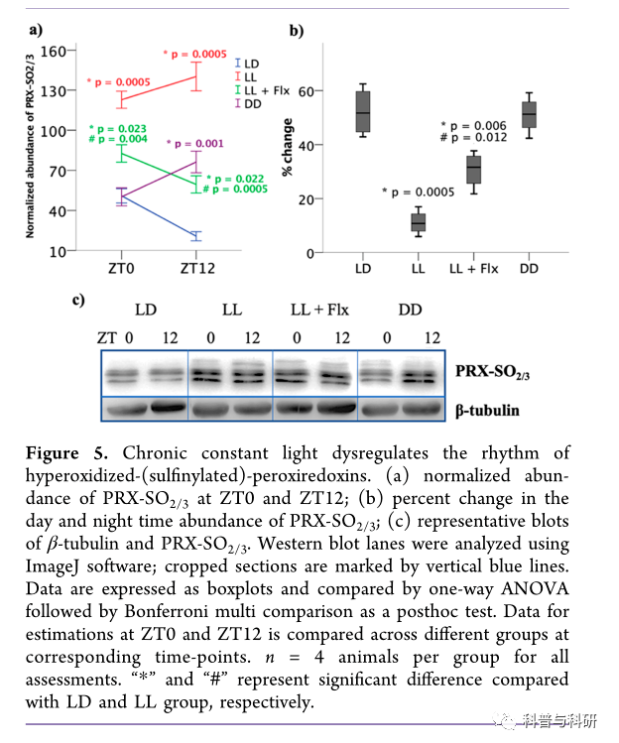
氧化过氧化还原蛋白的水平揭示了细胞的氧化状态,也表达了一种昼夜节律。13我们通过测量硫代过氧化还原蛋白(PRX-二氧化硫/3)在体内的表达来估计过氧化还原蛋白的过氧化程度。在ZT0,F(3,12) = 29.936,p = 0.0005,η2= 0.882时发现光照条件的显著影响;在ZT12,F(3,12) = 42.45,p = 0.0005,η2= 0.914。多重比较显示,在ZT0和ZT12时,L1大鼠中PRX-SO2/3的表达显著升高;和ZT12的DD大鼠(图5a)。
氟西汀治疗与LL大鼠相比,显著降低了两个时间点的PRXSO 2/3表达水平;然而,它不能完全稳定PRX二氧化硫/3水平,这一点在低剂量组和低剂量组之间有显著差异(图5a)。还观察到对PRX-SO2/3水平百分比变化的显著影响,F(3,12) = 30.546,p = 0.0005,η2= 0.884。与LD相比,LL大鼠的PRX-SO2/3水平的百分比变化非常低(图5b)。氟西汀治疗挽救了持续光照下大鼠PRX-SO2/3节律的丧失(图5b)。尽管DD大鼠与ZT12时的LD相比,PRX-SO2/3的水平有显著差异(图5a),但DD大鼠的prx-SO2/3水平为50%(图5b),与LD大鼠相当。研究结果表明,持续光照破坏了PRX1和PRX-SO2/3的节律;然而,其对PRX1的影响仅在ZT12显著,与在两个时间点发现的。
PRX-SO2/3表达的显著变化相反。这表明,与对PRX1的作用相比,恒定光对过氧化还原蛋白的氧化作用明显。数据进一步表明,尽管氟西汀治疗显著减弱了慢性恒定光对PRX代谢动力学的不利影响,但它并未稳定过氧化还原酶系统的节律。然而,氟西汀治疗有效地防止了恒定光对大鼠脊髓神经细胞中Per2表达的失调效应(图3)。有趣的是,Per2转录物的慢性上调被证明促进了小鼠的凋亡损伤和氧化应激。昼夜节律的转录和非转录标记之间的关系值得进一步研究。此外,昼夜节律的分子标记显示,与LD相比,DD大鼠的昼夜节律有中度差异,但差异不显著。因此,我们想强调的是,DD大鼠的昼夜节律可能是强健的,与LD大鼠的中度差异可能是由于相位差引起的。
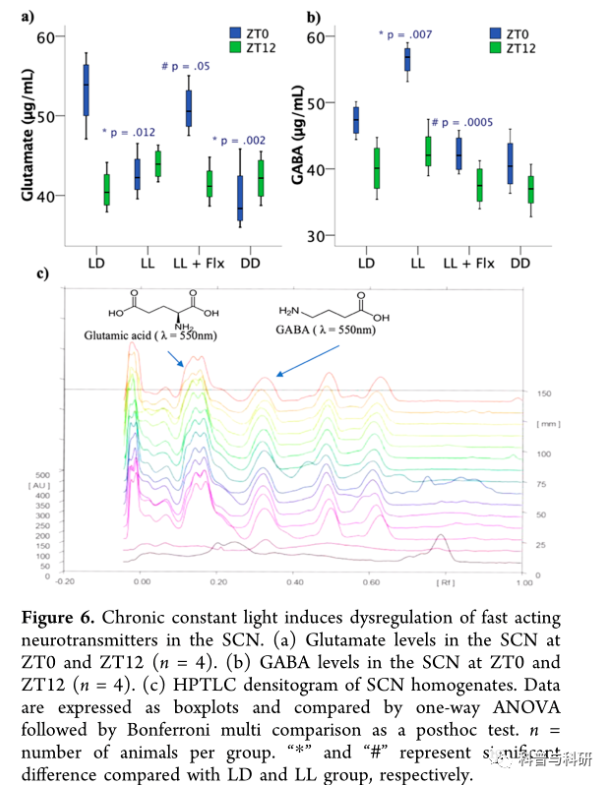
慢性恒定光诱导脊髓神经细胞的神经元失调。接下来,我们估计了白天和晚上快速反应神经递质、谷氨酸和γ-氨基丁酸(GABA)的水平。谷氨酸信号通过将光信号从视网膜传递到视交叉神经网络在昼夜节律的夹带中起着至关重要的作用。33然而,γ-氨基丁酸是视交叉神经网络的主要神经递质。本质上,SCN中的所有神经元都是γ-氨基丁酸能的。我们使用高效薄层色谱法估计了ZT0和ZT12时SCN中谷氨酸和γ-氨基丁酸的水平。在ZT0,F(3,12) = 11.675,p = 0.001,η2= 0.745时,观察到光照条件对谷氨酸水平的显著影响;但不在ZT12,F(3,12) = 1.205,p = 0.35。多重比较显示谷氨酸水平在L1和DD大鼠中显著降低,但在L1+Flx大鼠中与ZT0时的LD相比没有显著降低(图6a)。同样,在ZT0,F(3,12) = 21.234,p = 0.0005,η2= 0.841时,观察到光照条件对γ-氨基丁酸水平的显著影响;但不在ZT12,F(3,12) = 2.28,p = 0.131。多重比较显示,与ZT0时的乳酸脱氢酶相比,L1大鼠的γ-氨基丁酸水平显著增加(图6b)。然而,GABA水平在DD组(p = 0.067)或LL + Flx组(p = 0.267)与LD组相比没有显著差异。氟西汀治疗挽救了ZT0时SCN中γ-氨基丁酸的失调(图6b)。先前在重度抑郁症患者中观察到了氟西汀对循环中γ-氨基丁酸水平的类似下调作用。34A在ZT0时在DD大鼠中观察到谷氨酸水平的显著降低。DD大鼠谷氨酸水平的降低可能是由于绝对缺乏光刺激。SCN中的谷氨酸信号主要由光脉冲触发,对于DD大鼠来说,这种光提示是不存在的。有趣的是,我们发现L1大鼠在ZT0时γ-氨基丁酸水平激增。γ-氨基丁酸水平的升高可能意味着神经元的根本重塑。
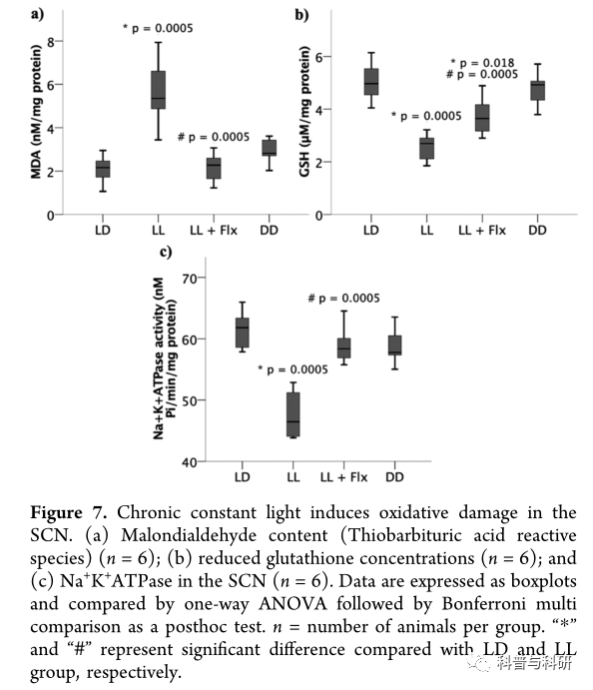
氧化应激可以被定义为活性氧产生压倒抗氧化防御的事件。在更高的水平上,氧化应激导致生物分子的不可逆修饰(脂质过氧化),这可能导致细胞功能的丧失。SCN中PRX-SO2/3水平的升高表明持续光照会破坏氧化还原节律并产生氧化应激(图5a)。因此,我们估计了大鼠脊髓神经细胞中氧化损伤的其他生物标志物。虽然过氧化还原蛋白是抵御活性氧的第一道防线,但谷胱甘肽是最有效的抗氧化蛋白质之一。还原型谷胱甘肽(GSH)分子在谷胱甘肽过氧化物酶的存在下被氧化,以螯合胞质溶胶中的活性氧,氧化应激的程度与生物样品中GSH的浓度成反比。硫代巴比妥酸活性物质的胞质水平是脂质过氧化程度的标志,并表示为生物样品中丙二醛(丙二醛)的浓度。36Na+K+ATPase是一种膜结合的离子转运蛋白,可逆着其电化学梯度将钠离子和K+离子转运穿过膜。钠钾三磷酸腺苷酶的最佳功能是维持神经元的静息电位。钠钾三磷酸腺苷酶活性低可能表明神经元无法从兴奋状态恢复。
丙二醛、谷胱甘肽和钠钾三磷酸腺苷酶活性用分光光度法测定。丙二醛、氟(3,20) = 17.933,p = 0.0005,η2 = 0.729;GSH,F(3,20) = 17.1p =0.0005,η2= 0.72。多项比较显示,与学习障碍大鼠相比,学习障碍大鼠的大脑皮质神经元中丙二醛水平显著升高,而在学习障碍大鼠(p = 0.879)和学习障碍+ Flx大鼠(p = 1)中未观察到显著差异(图7a)。与丙二醛形成对比的是,谷胱甘肽水平在大鼠脊髓神经细胞中显著降低,而在糖尿病大鼠中没有观察到显著差异。与糖尿病大鼠相比(图7b)。每日氟西汀治疗可防止L1+Flx大鼠脊髓神经细胞丙二醛的升高和谷胱甘肽水平的下降;然而,谷胱甘肽水平并没有完全恢复,这表明与LD大鼠有显著差异(图7a,b)。此外,钠钾三磷酸腺苷酶活性也表现出显著的影响,F(3,20) = 22.464,p = 0.0005 η2= 0.771。多重比较显示,在L1大鼠的SCN样品中,Pi的释放速率明显较低,这是通过每天服用氟西汀来预防的(图7c)。低的π释放率可能表明两种可能性:钠钾三磷酸腺苷酶的表达减少或钠钾三磷酸腺苷酶的酶活性降低。这些不同的结果可能导致从局部过度兴奋到去极化失活的症状,两者最终都会导致SCN中可兴奋神经元的功能障碍。总的来说,这些结果表明恒定的光诱导SCN中的神经元失调,表现为神经递质谷氨酸和γ-氨基丁酸水平的稳态失调;氧化应激;降低钠钾三磷酸腺苷酶活性。
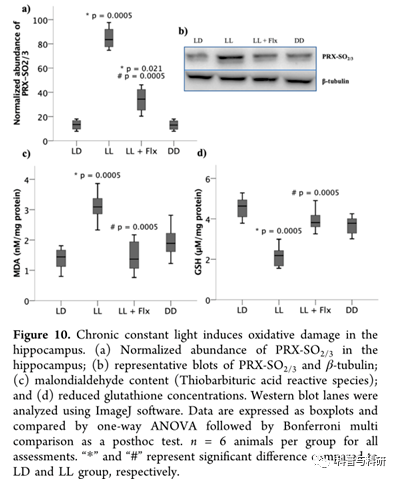
慢性持续光照损害认知表现。在恒定条件下暴露四个月后(在采集大脑进行生化分析前一个月),在封闭的场地中测量大鼠的自发运动活动,以排除运动症状对认知分析的影响。未观察到对大鼠自发运动活动的显著影响,F(3,36) = 0.463,p = 0.71(图8a)。在Y型迷宫上测量大鼠的自发交替和空间识别记忆。自发交替作为工作记忆的一种测量方法,揭示了光照条件的显著影响,F(3,36) = 28.567,p = 0.0005,η2= 0.704。多重比较表明,L1大鼠的交替评分明显低于LD大鼠,并且通过每日氟西汀治疗预防了损伤(图8b)。LD组和DD组大鼠的交替评分差异不显著,p = 0.105。此外,在测试过程中,通过在新手臂上花费的总时间测量的空间识别记忆也揭示了照明条件的显著影响,F(3,36) = 27.946,p = 0.0005,η2= 0.7(图8d)。与患有糖尿病的大鼠相比,患有糖尿病的大鼠在新的手臂上花费的时间要短得多。氟西汀的日常治疗防止了恒定光诱导的空间识别记忆缺陷(图8c)。接下来,我们测量了光照条件对老鼠在NORT的表现的影响。NORT的高辨别指数值表示对新对象的偏好,而零辨别指数值表示对新对象的零偏好。对大鼠的DI有显著影响,F(3,36) = 50.749,p = 0.0005,η2= 0.809。LL大鼠的阿迪值接近于零,多重比较显示LL大鼠和健康LD大鼠的DI存在显著差异(图8d)。相比之下,在DD(p = 0.058)和LL+Flx(p = 1)大鼠中,与LD相比,没有发现统计学上的显著差异。氟西汀治疗挽救了恒定光诱导的识别记忆缺陷(图8d)。此前已有研究表明,在不同的动物模型中,由昼夜节律性引起的认知缺陷通过抑制GABA信号传导而得到有效恢复。作者断言,SCN的GABA输出对记忆形成至关重要。据报道,氟西汀可使唐氏综合征小鼠模型中的γ-氨基丁酸释放、自发交替缺陷和海马突触可塑性正常化。根据这些报告,我们的结果表明,L1大鼠表现出工作和识别记忆缺陷(图8b,d),同时ZT0时SCN中γ-氨基丁酸水平升高(图6b),这是通过每天服用氟西汀预防的。由三个习得试验组成的水迷宫任务试验和由24个分离的探针试验用于评估习得学习和空间记忆回忆。
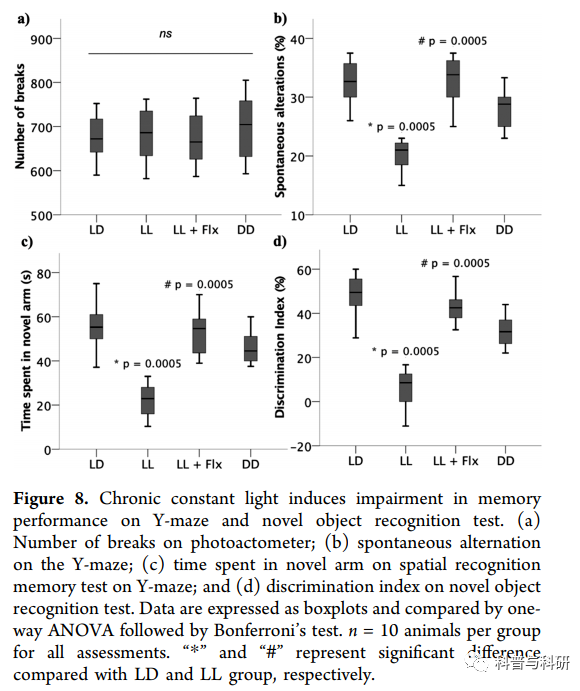
采集学习是通过比较采集试验中的逃逸潜伏期(到达隐藏平台的时间)来估计的。记忆回忆被测量为进入的潜伏期和在探测试验期间在目标象限中花费的总时间(停留时间)。采集试验中逃逸潜伏期的重复测量方差分析显示受试者内因素(时间)的显著影响,维尔克λ= 0.144,F(2,35) = 103.843,p < 0.001受试者内部和之间的因素(光照条件和时间),维尔克的λ= 0.614,F(2,35) = 3.217,p = 0.008。多重比较显示,学习障碍大鼠和学习障碍大鼠的逃避潜伏期有显著差异(图9a)。此外,在采集试验的最后一天,观察到光照条件对大鼠穿越距离的显著影响,F(3,36) = 32.840,p = 0.0005,η2= 0.749(图9b)。多重比较显示,在试验期间,L1大鼠比LD大鼠穿越的距离长得多(图9b)。这一发现与之前的一份报告相一致,该报告显示,即使压力大的动物扫过明显更长的路径,它们的逃避潜伏期也更长。作者断言,这种差异可能归因于触转(停留在墙壁附近)和使用简单的探索策略。39在目前的研究中,通过将恒定的光视为恒定的不可避免的应激源,可以更好地理解这种反应。有人认为,高水平的唤醒或压力会导致不稳定的注意力,这可能会阻碍有效的学习,40正如我们在实验中观察到的。
探针试验揭示了光照条件对记忆回忆指数的显著影响,即进入目标象限的潜伏期F(3,36) = 38.223,p = 0.0005,η2 = 0.761;停留时间F(3,36) = 44.668,p = 0.0005,η2= 0.788(图9d,e)。与LD组大鼠相比,LL组和DD组大鼠进入平台象限的时间明显更长(图9d)。此外,与DD大鼠相比,LL大鼠探索目标象限的时间明显短于LD大鼠(图9e)。每日氟西汀治疗可防止持续光照导致的空间记忆缺陷(图9)。这些发现与以前的报告一致,在以前的报告中,作者表明持续光照会导致啮齿动物的空间记忆缺陷,这可以通过每天服用氟西汀来挽救。然而,作者观察到在短期暴露于持续光照后的空间记忆损伤。我们以前也表明,在持续光照两个月之后,就会出现空间记忆缺陷,这种情况会持续四个月。这表明空间记忆缺陷不会因为补偿或适应而随着时间的推移而改善。啮齿动物在正常条件下表现出昼夜节律的记忆获得和回忆,并在24小时的恒定黑暗条件下持续。正如所料,我们研究中的DD大鼠比ll大鼠表现出更好的记忆获得和回忆。LL大鼠的不良表现可归因于节律的完全丧失。
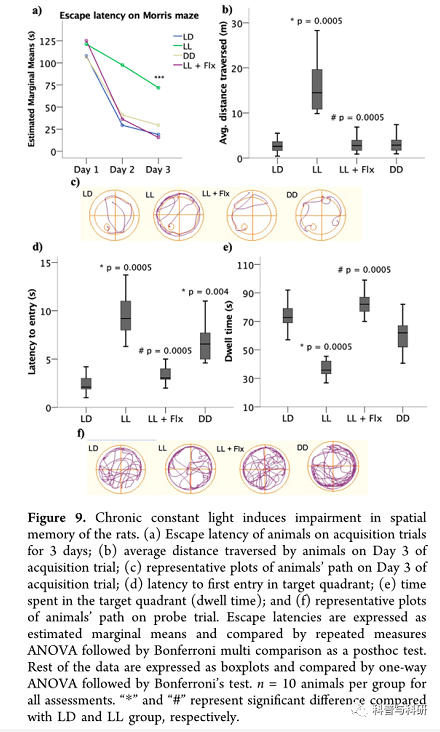
慢性持续光照诱导海马和周围组织的氧化损伤。根据观察到的认知缺陷,我们估计了大鼠海马和血浆中的氧化损伤标记物。海马中PRX-SO2/3的水平显示了光照条件和治疗的显著影响,F(3,20) = 70.787,p = 0.0005,η2= 0.947。多重比较显示,L1大鼠海马中的PRX-SO2/3水平显著升高,这种效应被每日氟西汀治疗有效地预防,尽管预防效应不是最大的,这与LD大鼠有显著差异(图10a)。此外,还观察到海马丙二醛水平的显著影响,F(3,20) = 15.355,p = 0.0005,η2 = 0.697;和谷胱甘肽水平,F(3,20) = 21.821,p = 0.0005,η2= 0.766。与脊髓神经细胞中的丙二醛和谷胱甘肽水平平行,多重比较显示,与学习障碍大鼠相比,学习障碍大鼠海马中的丙二醛水平显著升高,并且在学习障碍大鼠或学习障碍+ Flx大鼠中没有观察到显著差异,p = 1(图10c)。相比之下,低剂量组大鼠的谷胱甘肽水平显著降低,而在剂量组则无显著差异,p = 0.86或L1+Flx大鼠,p = 0.112,与LD相比(图10d)。每日氟西汀治疗可预防海马区的氧化损伤,表现为L1+Flx大鼠海马区丙二醛和谷胱甘肽水平的正常化(图10c,d)。此外,对大鼠外周组织损伤的血浆标志物进行了评估。乳酸脱氢酶水平显著升高,p = 0.009碱性磷酸酶,p = 0.005谷草转氨酶,p = 0.002和谷丙转氨酶,p = 0.002。
此外,血浆中中性粒细胞与淋巴细胞的比率(NLR)是慢性亚临床炎症的标志。此外,NLR值的增加表明外周存在与阿尔茨海默病相关的炎症,这是一个假定的鉴别诊断参数。44我们发现,与LD相比,LL大鼠的NLR值显著增加,p = 0.003(支持表S1)。总的来说,这些数据表明氧化损伤是广泛的,并且存在于暴露于恒定光的大鼠的大脑和外周组织中
慢性持续光照导致大鼠淀粉样蛋白功能障碍。过量的Aβ被认为是AD病理的核心,并作为AD的可靠指标。我们发现光照条件对海马中可溶性Aβ1-42水平有显著影响(F(3,20) = 54.365,p = 0.0005,η2= 0.891)。多重比较显示,LD大鼠和LL大鼠的可溶性aβ1-42水平存在显著差异(图11a)。与LD大鼠相比,在DD和LL + Flx大鼠中未观察到这种升高,p = 1。选择性5-羟色胺再摄取抑制剂在降低人和小鼠的Aβ水平方面显示出有希望的结果。45氟西汀治疗挽救了转基因AD小鼠的空间记忆缺陷,并显著降低了脑组织中可溶性Aβ的水平。根据这些报告,我们发现每天氟西汀治疗阻止了可溶性Aβ1-42肽水平的升高(图11a)并挽救了L1大鼠的空间记忆缺陷(图9)。此外,L1大鼠海马中Bace1转录物的表达显著上调,表达值的平均增加超过2倍,δδCt > 2(图11b)。在L1+Flx大鼠中没有观察到Bace1表达的显著上调。相对于学习障碍,在L1大鼠海马中可溶性Aβ1-42和Bace1转录物的水平中发现了强相关性(图11c)。接下来,我们评估了在包括海马体在内的SCN靶区广泛表达的Prokr2基因的表达。19Prokr2对于皮质和海马体中SCN介导的神经元激活以及昼夜节律行为的调节至关重要。
此外,大脑炎症和神经元损伤与PK2系统的活性增加有关。我们发现L1大鼠海马体中Prokr2转录物的显著上调,δδCt > 2(图12a),表明SCN介导的海马体神经元激活功能障碍,从而导致昼夜节律行为的失调,并促进神经元损伤。我们还评估了抗衰老基因sirtuin 1 (Sirt1)的表达,因为它具有双重作用。在阿尔茨海默病患者的大脑中,Sirt1的基因表达显著降低,并与症状的持续时间呈负相关。49此外,Sirt1深深嵌入昼夜节律钟。12 Sirt1的转录物和蛋白质水平在一天中几乎保持不变;然而,其脱乙酰酶活性振荡并直接影响时钟基因的振幅。氧化应激通过诱导微小核糖核酸的表达来抑制Sirt1的转录。我们的结果显示L1大鼠海马中Sirt1的表达显著降低,平均表达降低不到1/2倍,δδCt < 0.5(图12b)。氟西汀治疗阻止了Prokr2和Sirt1转录物的失调(图12a,b)。
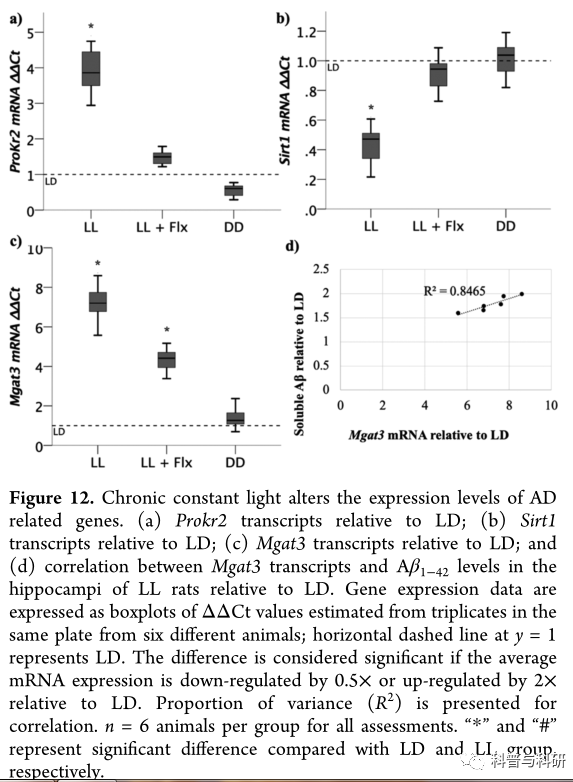
聚糖修饰稳定BACE1并防止其溶酶体降解,从而促进Aβ的产生。二分法GlcNAc对BACE1和APP具有选择性。54 GenT-III及其mRNA Mgat3在AD患者中过表达。二分法GlcNAc对BACE1的添加在氧化应激条件下加速,并且它稳定BACE1并促进其活性。小鼠中Mgat3基因的缺失证实了这一点,这导致BACE1在类似条件下的溶酶体快速降解。我们的结果显示L1大鼠海马中Mgat3转录显著上调,δδCt > 2(图12c)。Mgat3转录物的增加与L1大鼠相对于LD的异常高水平的可溶性Aβ1-42密切相关(图12d)。我们得出结论,持续光照导致的氧化应激导致Mgat3、Bace1和进一步的Aβ42的上调,可能通过BACE1蛋白的翻译后稳定而增强。此外,与其对Bace1转录物上调的预防作用相反(图11b),氟西汀治疗对L1大鼠的Mgat3转录物水平没有这种作用(图12c)。这表明氟西汀对Aβ1-42水平的保护作用(图11a)是由于Bace1转录的下调,而不是由于GnT-III对BACE1翻译后稳定的抑制。
总的来说,我们的发现表明慢性恒定光失调调节大鼠脊髓神经细胞中昼夜节律分子标记Per2、PRX1和PRX-SO2/3的表达。快速作用的兴奋性神经递质谷氨酸水平显著降低,可能是因为光脱敏,相反,快速作用的抑制性γ-氨基丁酸水平在ZT0时显著升高。老鼠在空间、识别和工作记忆任务上的表现也明显受损。最后,持续光照产生巨大的氧化应激,导致一系列分子Aβ体内平衡失调,Bace1、Mgat3和Prokr2上调,大鼠海马Sirt1in区下调。然而,在ZT5每天用氟西汀治疗可防止Per2、快速作用神经递质水平、氧化应激标记物、Aβ1-42和AD相关基因的失调,并挽救L1大鼠的认知障碍。先前的研究也将昼夜节律障碍引起的氧化应激与神经退行性变和AD联系起来。反过来,一旦淀粉样病变发生,病理性升高的Aβ水平可诱导昼夜节律时钟功能障碍。这种有害的反馈回路触发一连串不可逆的神经病理事件。
结论
由于光噪声、跨子午线旅行和轮班工作而导致的不合时宜的光暴露持续困扰着人类的昼夜节律。在这里,我们表明长期暴露在恒定的光下会诱导多种令人痛苦的分子途径,并为大鼠阿尔茨海默病的发病奠定基础。恒定的光失调昼夜节律时钟和神经递质信号,并在大鼠大脑中诱导氧化应激。持续光照的大鼠表现出淀粉样病变和阿尔茨海默病的特征。本文提出,在目标人群中优化昼夜节律时间的治疗努力对抑制阿尔茨海默病的流行具有很大的希望。我们的发现可能会鼓励未来的研究解开昼夜节律紊乱诱导的神经退行性疾病的相关途径。
科普与科研微信公众号,一个致力于传播科普资讯、分享科研资料及前言资讯的平台。本公众号每天更新科普知识、定期举办免费线上科研讲座、每周定期发布最前言文献翻译解读、发布当前最具有时效性的资讯、分享最具实用性的科研资料。同时,本公众号还举办一系列磁共振、脑电相关数据处理培训班。2021年,该团队预计在该公众号发布一款集磁共振、脑电、心理范式、机器学习、问卷为一体的数据处理软件包。