摘要
神经发育障碍,包括自闭症谱系障碍(ASD),是由核心行为障碍定义的;然而,个体的子集显示出一系列的胃肠异常。我们在母体免疫激活(MIA)小鼠模型中证明了胃肠屏障缺陷和微生物群的改变,这是已知的显示ASD特征的模型。用人类共生脆弱拟杆菌对MIA后代进行口服治疗可纠正肠道通透性,改变微生物组成,并改善沟通、刻板、焦虑样和感觉运动行为的缺陷。
MIA后代表现出改变的血清代谢组学特征,脆弱芽孢杆菌调节几种代谢物的水平。用MIA增加并由脆弱芽孢杆菌恢复的代谢物治疗新生小鼠会导致某些行为异常,这表明肠道细菌对宿主代谢组的影响会影响行为。综上所述,这些发现支持了ASD小鼠模型中肠道-微生物-大脑的联系,并确定了人类神经发育障碍中胃肠道和特殊行为症状的潜在益生菌疗法。
引言
神经发育障碍的特征是大脑发育受损以及行为、认知和/或身体异常。一些人在社交、沟通和/或强迫性活动方面有共同的行为异常。在这方面,最常见的是自闭症谱系障碍(ASD),这是一种严重的神经发育疾病,根据刻板行为的存在和严重程度以及语言和社会交往的缺陷进行诊断。截至2008年,美国报告的自闭症发生率已迅速上升至每88例分娩中有1例,这是一个重大的医疗和社会问题。
然而,治疗自闭症核心症状的疗法是有限的。尽管环境风险因素、免疫调节障碍和额外的外周干扰在ASD发病机制中的作用已引起了极大的关注,但对ASD的许多研究都集中在疾病的遗传、行为和神经方面。在ASD的几种共病中,胃肠不适尤其令人感兴趣,因为据报道其患病率较高和与症状严重程度的相关性。虽然ASD中胃肠症状的标准化诊断尚未明确,但临床和流行病学研究报告了胃肠动力改变和肠道通透性增加等异常情况。
此外,最近对14,000多名自闭症患者进行的多中心研究显示,与对照组相比,自闭症患者中炎症性肠病(IBD)和其他胃肠道疾病的患病率更高。其他神经系统疾病也有胃肠道异常的报告,包括雷特综合征人,脑瘫和重度抑郁症。这些胃肠道问题的原因尚不清楚,但一种可能性是它们可能与肠道细菌有关。事实上,微生物群的生物失调与多种人类疾病的发病机制有关,包括IBD病、肥胖症和心血管疾病,并且多项研究报告了ASD中肠道微生物群组成的改变。共生细菌影响各种复杂的行为,包括社交、情绪和焦虑样行为,并对小鼠的大脑发育和功能做出贡献和人类。肠道微生物群和大脑之间的长期相互作用是基于微生物的疗法治疗小鼠多发性硬化症和抑郁症症状的基础,以及报道的益生菌在治疗人类慢性疲劳综合征和心理困扰的情绪症状方面的功效。
基于对肠道-微生物系统连接的新认识,在小鼠模型中模拟ASD的一些行为特征是否也会导致胃肠道异常。几种遗传和/或环境风险因素的小鼠模型被用于研究自闭症。我们利用了母亲免疫激活(MIA)模型,该模型基于将母亲感染与后代自闭症风险增加联系起来的大型流行病学研究。许多研究将增加的房缺风险与家族性自身免疫性疾病联系起来和母体血液、胎盘和羊水中炎症因子水平升高。通过给怀孕的母鼠注射病毒模拟多聚体(I:C)来模拟小鼠的MIA,产生的后代表现出与ASD相关的核心沟通、社交和刻板损伤,以及常见的自闭症神经病理学——小脑浦肯野细胞的局部缺陷。
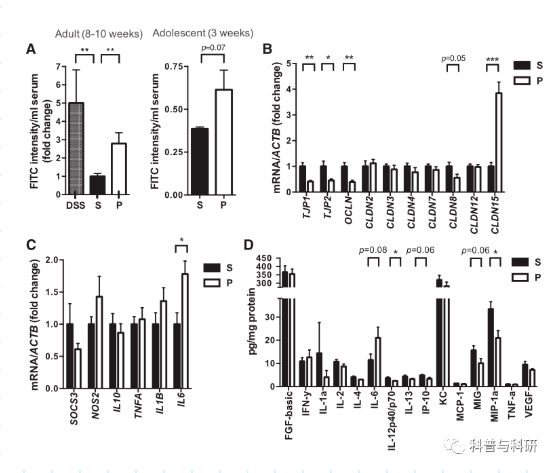
结果免疫激活母亲的后代表现出人类房缺的胃肠道症状据报道,房缺儿童的亚组表现出胃肠道异常,包括肠通透性增加或“漏肠”。我们发现,表现出许多ASD行为和神经病理学症状的成年MIA后代也具有肠屏障完整性的显著缺陷,这反映在find葡聚糖穿过肠上皮进入循环的易位增加(图1A,左)。这种与MIA相关的肠通透性增加类似于用葡聚糖硫酸钠(DSS)治疗的小鼠,其诱导实验性结肠炎(图1A,左)。肠完整性的缺陷在3周大的MIA后代中是可检测到的(图1A,右),表明这种异常是在生命早期建立的。
与漏肠表型一致,来自成年MIA后代的结肠包含TJP1、TJP2、OCLN和CLDN8的基因表达减少和CLDN15的表达增加(图1B)。在成年MIA后代的小肠中也观察到TJP1的表达缺陷(图S1A可在网上获得),表明肠屏障完整性的广泛缺陷。肠道通透性通常与免疫反应的改变有关。因此,来自成年MIA后代的结肠显示白细胞介素-6(IL-6)mRNA和蛋白质水平增加(图1C和1D),细胞因子/趋化因子IL-12p40/p70和MIP-1a水平降低(图1D)。MIA后代的小肠也表现出细胞因子/趋化因子谱的改变(图S1C)。根据苏木精-伊红染色切片对大体上皮形态的组织学检查评估,肠道细胞因子的变化不伴有明显的胃肠道病理(数据未显示)。总的来说,我们发现免疫激活母亲的成年后代表现出增加的肠道通透性和异常的肠道细胞因子谱。

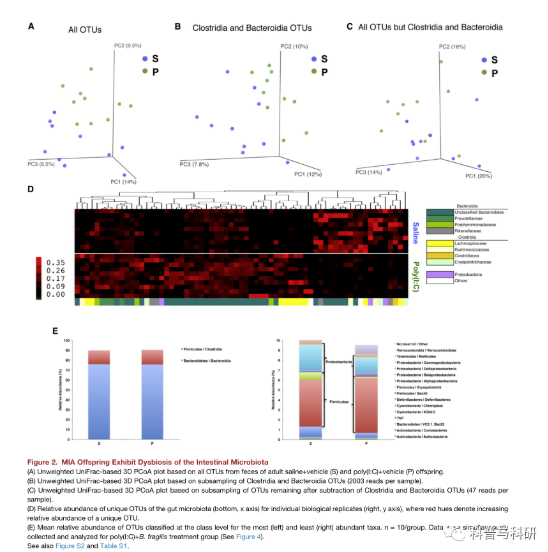
在自闭症谱系障碍个体中发现了与微生物群相关的异常,包括被破坏的群落组成,但重要的是要注意到,迄今为止缺乏明确的ASD相关微生物特征。为了评估MIA是否诱导微生物群改变,我们通过对从成年MIA或对照后代分离的样品进行16SrRNA基因测序来调查粪便细菌群。α多样性,即物种丰富度和均匀度,在对照和MIA后代之间没有显著差异,通过几个指数进行测量(图S2A和S2B)。相比之下,未加权的UniFrac分析(衡量微生物群落之间的系统发育相似程度)揭示了MIA对成年后代肠道微生物群的强烈影响(图2)。
通过主坐标分析(PCoA),MIA样本与对照组明显聚类,且在组成上有显著差异(表S3,ANOSIMR = 0.2829,p=0.0030),表明MIA子代和对照组之间肠道细菌的成员存在显著差异(图2A)。当梭状芽孢杆菌属和拟杆菌属的序列(约占总读数的90.1%)仅通过PCoA进行检测时,MIA对改变肠道微生物群的影响更加明显(R= 0.2331,p= 0.0070图2B),但当梭菌属和拟杆菌属序列被明确排除在所有其他细菌类别的多囊卵巢综合征之外时(R= 0.1051,p=0.0700图2C)。这表明梭菌属和拟杆菌属操作分类单位(OTUs)多样性的变化是MIA后代和对照之间肠道微生物群差异的主要驱动力。
在所有样本中检测到的1,474个OTUs中,有67个区分了不同的处理组,包括属于细菌科(松萝科、乳球菌科、丹毒杆菌科、产碱杆菌科、紫菜科、前骆驼科、千里光科)和未分类的拟杆菌科(图2D和表S1)。在这67个区别性OTUs(相对丰度:13.3%1.65%对照,15.93%0.62%MIA)中,19个在对照样品中更丰富,48个在MIA样品中更丰富。与多囊卵巢综合征的结果一致(图2A-2C),大多数区分多囊卵巢综合征后代和对照的外胚叶被归为类杆菌(45/67外胚叶或67.2%;12.02%1.62%对照,13.48%0.75% MIA)和梭菌(14/67OTUs或20.9%;1.00%0.25%对照,1.58%0.34%MIA)。
重要的是,梭菌的总体相对丰度没有显著差异(13.63%2.54%对14.44%2.84%;p= 0.8340)和拟杆菌(76.25%3.22%对76.22%3.46%;表明梭状芽孢杆菌和类杆菌OTUs成员的改变驱动了实验组之间肠道微生物群的主要变化。总的来说,我们发现MIA导致肠道微生物群的生物失调,主要是由梭菌属和类杆菌属细菌的特定OTU的变化引起的。梭状芽孢杆菌目中被分类为拉克诺皮科和鲁米诺球菌科的OTUs的变化平行选择了患有ASD的受试者粪便中梭状芽孢杆菌种类增加的报告。
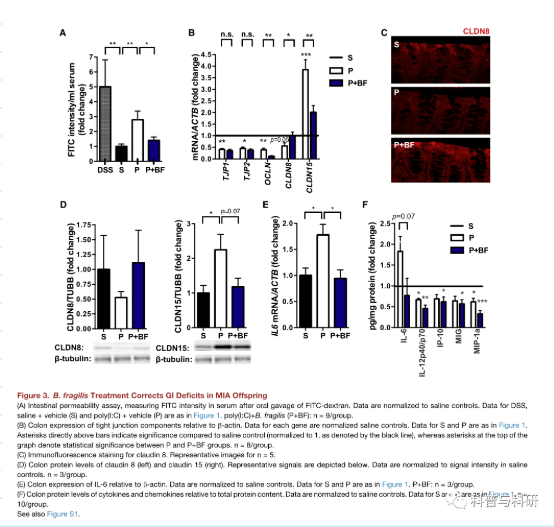
脆弱拟杆菌改善MIA子代肠道屏障完整性肠道微生物在肠道上皮的发育、维护和修复中起着重要作用。在小肠中没有观察到脆弱芽孢杆菌对紧密连接表达的影响(图S1B),这与类杆菌主要在结肠中发现的事实一致。最后,益生菌给药前胃肠道缺陷的存在(图1A,右)表明脆弱芽孢杆菌可能治疗而不是预防MIA后代的这种病理。B.脆弱的治疗也恢复了结肠白细胞介素-6基因和蛋白质水平的米娅相关的增加(图3E和3F)。MIA后代的结肠和小肠中其他细胞因子的水平都发生了改变(图1D和1C),但这些不受脆弱芽孢杆菌治疗的影响,揭示了对白介素-6的特异性。
我们进一步发现,重组IL-6治疗可以调节体内和体外结肠器官培养物中CLDN8和15的结肠水平(数据未显示),这表明脆弱芽孢杆菌介导的结肠IL-6水平的恢复可能是其对肠道通透性影响的基础。总的来说,这些发现表明脆弱芽孢杆菌对MIA后代的治疗改善了胃肠屏障完整性的缺陷,并纠正了紧密连接和细胞因子表达的改变。
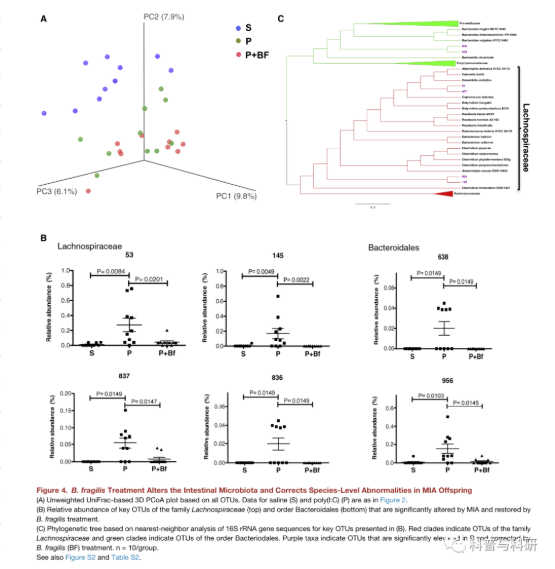
脆弱贝氏体治疗恢复MIA后代特定微生物群的变化脆弱贝氏体改善MIA后代胃肠道缺陷的发现促使我们检查其对肠道微生物群的影响。脆弱贝氏体通过PCoA治疗MIA后代后未观察到显著差异(ANOSIMR = 0.0060 p = 0.4470,表S3),在微生物群落丰富度(分布密度:p= 0.2980,观察物种:p= 0.5440)和均匀度(基尼系数:p= 0.6110,辛普森均匀度:p=0.5600,图4A、S2A和S2B),或相对丰富的阶级水平(图S2C)。然而,对区分成年MIA后代和对照的关键OTU的评估显示。碎片化处理显著改变了35个otu的水平(表S2)。
具体而言,用脆弱芽孢杆菌处理的MIA后代显示出67个OTU中的6个的相对丰度的显著恢复,所述OTU被发现区分MIA和对照后代(图4B和表S2),它们在分类学上被指定为未分类的拉克诺斯皮科类杆菌属和梭菌属(图4B和表S2)。值得注意的是,这些变化发生在脆弱芽孢杆菌没有持续定殖的情况下,而脆弱芽孢杆菌在从治疗的米亚后代分离的粪便和盲肠样本中仍然检测不到(图S2D和S2E)。由MIA改变并由脆弱芽孢杆菌处理恢复的OTUs的系统发育重建揭示了拟杆菌OTUs聚集在一起形成一个单系组,而拉克逊酵母科OTUs聚集成两个单系组(图4C)。
这一结果表明,尽管用脆弱芽孢杆菌治疗MIA后代可能不会导致持久的定居,但这种益生菌纠正了拉克诺斯皮科相关微生物特定群体以及未分类细菌素的相对丰度。总之,我们证明用脆弱乳杆菌治疗MIA后代可以改善共生微生物群中与MIA相关的特殊变化。
前脉冲抑制(PPI)任务是测量动物在受到低强度刺激(“前脉冲”)时,对声音(“脉冲”)的反应中抑制惊吓的能力。质子泵抑制剂的缺乏是感觉运动门控受损的一种衡量标准,在包括自闭症在内的几种神经发育障碍中均有观察到。对于5或15分贝的预脉冲,MIA后代表现出较低的PPI(图5B)。大理石掩埋试验测量了小鼠重复进行自然挖掘行为的倾向,这种行为不会受到焦虑的干扰。
与对照组相比,MIA后代显示出更多的定型大理石掩埋(图5C)。超声波发声用于测量小鼠的交流,其中不同类型和主题的呼叫在不同的社会范式中产生。MIA的后代表现出交流的缺陷,表现为对社会接触产生的超声波发声的数量和持续时间减少(图5D)。脆弱疗法改善MIA后代中与自闭症相关的行为异常(A)在野外探索试验中的焦虑样和运动行为。米娅的后代表现出社交能力的缺陷,或者偏好与一只新奇的鼠标而不是新奇的物体互动,以及社交偏好(社交新鲜感),或者偏好与一只不熟悉的鼠标而不是熟悉的鼠标互动(图5E和5F)。总之,MIA的后代表现出许多与ASD以及其他如焦虑和感觉运动门控缺陷有关的行为异常。
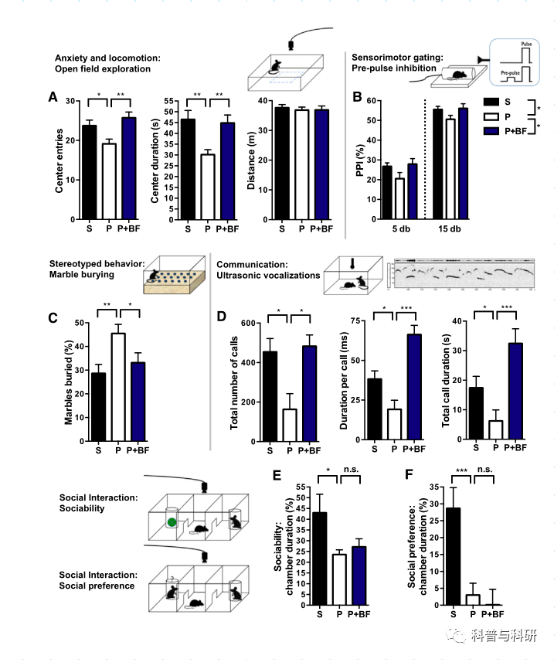

尽管脆弱贝氏体治疗的MIA后代表现出改善的交流、重复、焦虑样和感觉运动行为,但他们在社交和社会偏好方面仍有缺陷(图5E)。利培酮治疗CNTNAP2敲除小鼠也可选择性改善ASD相关行为,CNTNAP2敲除小鼠是ASD的一种遗传小鼠模型,其中沟通和重复但非社会性的行为得到纠正。这些数据表明,与其他行为相比,控制社会行为的回路或回路可塑性可能存在差异,脆弱芽孢杆菌的治疗可能在改善过程中调节特定的回路——最少的措施和可能的神经发育行为缺陷。有趣的是,对脆弱芽孢杆菌治疗MIA后代的行为改善与系统免疫的变化无关(图S3A-S3D),并且不依赖于多糖A(PSA),一种先前被脆弱芽孢杆菌鉴定为具有免疫调节作用的分子(图S3E)。
此外,行为的改善并不是脆弱芽孢杆菌特有的,因为多形拟杆菌的类似治疗也显著改善了MIA后代的焦虑样、重复性和交流行为(图S4)。这与我们的发现相一致,即脆弱芽孢杆菌治疗在胃肠道中没有明显的脆弱芽孢杆菌定殖的情况下改善了行为问题(图S2D和S2E),因此可能通过常驻微生物群组成的持续变化发挥作用(图4)。然而,细菌治疗有一定程度的特异性,因为施用粪肠球菌对MIA后代的焦虑样和重复行为没有影响(数据未显示)。
有趣的是,对脆弱芽孢杆菌治疗MIA后代的行为改善与系统免疫的变化无关(图S3A-S3D),并且不依赖于多糖A(PSA),一种先前被脆弱芽孢杆菌鉴定为具有免疫调节作用的分子(图S3E)。此外,行为的改善并不是脆弱芽孢杆菌特有的,因为多形拟杆菌的类似治疗也显著改善了MIA后代的焦虑样、重复性和交流行为(图S4)。这与我们的发现相一致,即脆弱芽孢杆菌治疗在胃肠道中没有明显的脆弱芽孢杆菌定殖的情况下改善了行为问题(图S2D和S2E),因此可能通过常驻微生物群组成的持续变化发挥作用(图4)。然而,细菌治疗有一定程度的特异性,因为施用粪肠球菌对MIA后代的焦虑样和重复行为没有影响(数据未显示)。
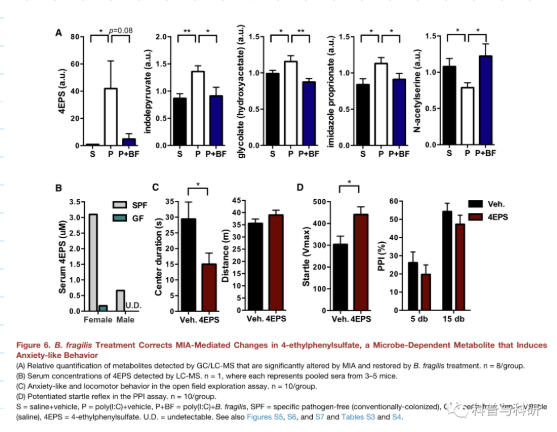
值得注意的是,将单一代谢物4EPS全身给药于原始野生型小鼠足以诱发类似于在MIA后代中观察到的焦虑样行为(图6C)。相对于经车辆处理的对照组,暴露于4EPS的小鼠在开阔场地中行进相当的距离,但在中央竞技场中花费的时间较少(图6C)。此外,在质子泵抑制剂试验中,4EPS处理的小鼠对非条件初级刺激的反应表现出增加的惊吓强度,但质子泵抑制剂没有显著变化(图6D),代表惊吓反射的焦虑相关增强。
讨论
我们证明了MIA小鼠模型表现出与ASD和其他神经发育障碍相关的行为症状,同时还显示出胃肠道完整性缺陷、共生微生物群的生物失调和血清代谢物的改变。至少其中一些改变类似于在ASD个体亚群中观察到的内表型。肠道通透性增加和微生物改变在几项关于ASD的独立研究中有报道;然而,这些发现受到一些报告的质疑,即病例和对照之间没有显著差异。据报道,在不同的研究中,自闭症患者胃肠道异常的患病率也有很大差异,从9%到91%不等。许多这样的研究都有方法上的局限性,包括不适当的实验控制、高样本异质性、小样本量和选择偏差。
因此,脆弱芽孢杆菌和改善肠道健康之间的相关性在小鼠和人类中都存在。与胃肠微生物在调节肠道通透性和代谢稳态中的作用一致,我们表明脆弱芽孢杆菌治疗纠正了似乎源于肠道的特定血清代谢物中MIA相关的变化,表明脆弱芽孢杆菌可以防止有害分子从胃肠道腔中泄漏。在对这一假设的概念验证测试中,我们揭示了微生物调节的代谢物4EPS,其在循环中由MIA升高,并由脆弱芽孢杆菌治疗恢复,足以诱导未成熟小鼠的焦虑样行为。这些数据表明,代谢组学的变化有助于自闭症相关行为异常的发生和/或持续。
注意事项
值得注意的是,脆弱芽孢杆菌治疗改善了MIA后代中异常的沟通、刻板印象、感觉运动和焦虑样行为,支持了肠脑连接在调节神经发育障碍中的新证据。共生细菌在调节行为中的作用得到了研究的支持,这些研究揭示了焦虑样、伤害感受性社会行为中GF和SPF小鼠之间的差异。绿色荧光小鼠在与突触功能和长时程增强相关的脑基因表达途径中也表现出广泛的微生物群依赖性变化。
此外,其他与ASD相关的非不可知行为,包括焦虑和PPI受损,通常在几种神经疾病中报告。不同疾病诊断的表型重叠表明,我们在肠道-微生物-大脑连接和基于微基础的行为治疗方面的发现可能广泛适用于各种疾病。我们提出了一个变革性的概念,即自闭症和其他可能的行为疾病是涉及肠道的潜在疾病,最终影响免疫、代谢和神经系统,微生物介导的治疗可能是这些神经发育障碍的安全有效的治疗方法。
科普与科研微信公众号,一个致力于传播科普资讯、分享科研资料及前言资讯的平台。本公众号每天更新科普知识、定期举办免费线上科研讲座、每周定期发布最前言文献翻译解读、发布当前最具有时效性的资讯、分享最具实用性的科研资料。同时,本公众号还举办一系列磁共振、脑电相关数据处理培训班。2021年,该团队预计在该公众号发布一款集磁共振、脑电、心理范式、机器学习、问卷为一体的数据处理软件包。