研究进展:阿尔茨海默病(AD)作为最常见的神经退行性疾病,其复杂的病理为开发改进的治疗和诊断工具带来了巨大的挑战。最近的研究表明可溶性Aβ寡聚体会导致AD患者和动物模型中的突触功能障碍和记忆丧失。尽管其确切病理机制仍不清楚,但更多的临床试验表明,靶向神经毒性可溶性Aβ寡聚体是减缓AD进展的更有效策略。因此,我们认为开发改进的治疗和诊断工具来检测和表征这些可溶性Aβ物种非常重要。然而目前大多数探针只能识别不溶性的、纤维状的Aβ物种,并且检测最具神经毒性的可溶性Aβ寡聚体的能力较差。已有报道的能够结合可溶性Aβ寡聚体的新型荧光染料中,这些分子的发现通常是通过高通量筛选或有限的结构-活性关系研究来实现的,没有合理设计可溶性Aβ寡聚体探针的通用方法。研究表明含有Aβ原纤维结合片段和针对其他AD病理如金属离子抑制、活性氧形成、神经炎症、和乙酰胆碱酯酶抑制的多功能化合物可能是AD治疗开发的潜在先导化合物。然而,迄今为止尚未开发出对可溶性Aβ寡聚体和靶标表现出明显亲和力的多功能化合物
解决方案:在此,本文报道了一种新型两亲性化合物LS-4的开发,该化合物通过将疏水性淀粉样蛋白原纤维结合片段与亲水性氮杂大环连接而产生,能够显著增加对各种淀粉样蛋白β (Aβ)肽聚集体的结合亲和力(图1)。所开发的化合物显示出不寻常的荧光开启和对Aβ聚集体的高结合亲和力,特别是对可溶性Aβ低聚物。相比之下,化合物Pre-LS-4只含有疏水性共轭芳族片段(图2),不含亲水性氮杂大环部分,对Aβ物质的结合亲和力显著降低。LS-4还表现出抗氧化性能,并能阻止Cu2+抗坏血酸氧化还原循环,从而导致活性氧的形成。
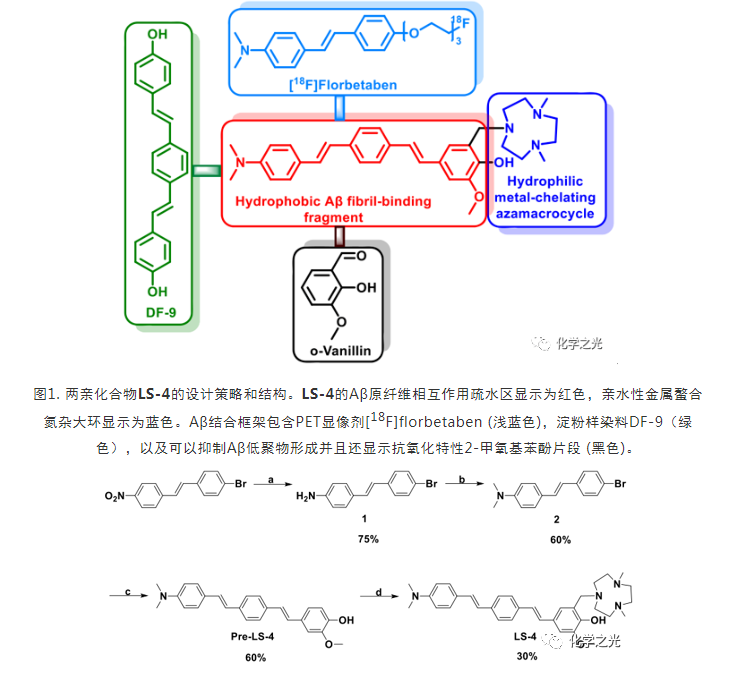
图2。 Pre-LS-4和LS-4a的合成
此外,在给予LS-4至5xFAD小鼠后,LS-4处理的脑切片的荧光成像显示,LS-4可以容易地穿透血脑屏障(BBB)并在体内与Aβ寡聚体结合,用Aβ寡聚体特异性抗体免疫染色证实了这一点。此外,与载体处理的5xFAD小鼠相比,用LS-4处理5xFAD小鼠显著减少了淀粉样斑块和相关磷酸化(p-tau)聚集体的数量,同时小胶质细胞的激活也减少了(图3)。此外,分子动力学模拟证实了在分子结构中引入亲水部分可以显著增强与Aβ肽种类的极性残基的静电相互作用的观察。最后,利用氮杂大环的强铜螯合特性,进行了一系列正电子发射断层扫描(PET)成像和生物分布研究,表明64Cu-LS-4复合物与淀粉样斑块结合,并且可以在5xFAD小鼠大脑中积累到比WT对照组明显更大的程度(图4)。总的来说,这些体外和体内研究表明,采用含有亲水性片段的两亲性分子连接到疏水性淀粉样原纤维结合片段的新策略可以增加这些化合物对可溶性Aβ寡聚体的结合亲和力,因此可以用于检测和调节AD中的可溶性Aβ种类。
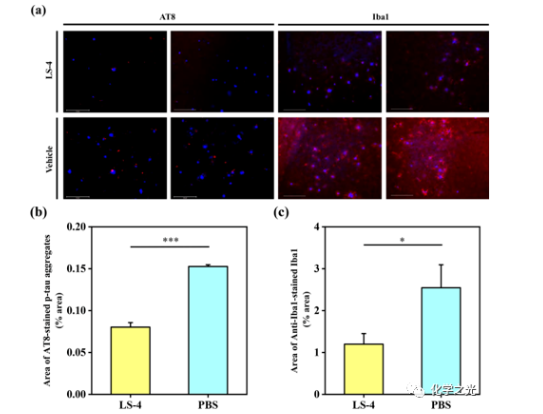 图3。 (A)用LS-4和载体处理的5xFAD小鼠的CF594-AT8和CF594-Iba1免疫染色脑切片的代表性荧光显微图像;(B)定量来自5xFAD小鼠的CF594-AT8免疫染色脑切片的面积;(C)定量来自5xFAD小鼠的CF594-Iba1免疫染色脑切片的面积。
图3。 (A)用LS-4和载体处理的5xFAD小鼠的CF594-AT8和CF594-Iba1免疫染色脑切片的代表性荧光显微图像;(B)定量来自5xFAD小鼠的CF594-AT8免疫染色脑切片的面积;(C)定量来自5xFAD小鼠的CF594-Iba1免疫染色脑切片的面积。
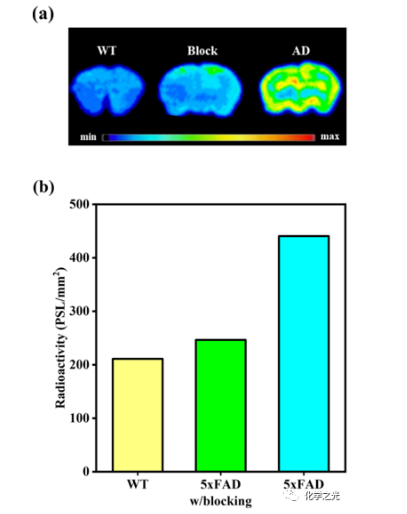
图4。 存在/不存在非放射性Aβ特异性阻断剂情况下,(A)WT和5xFAD小鼠脑切片的放射自显影图像;(B)WT和5xFAD小鼠脑切片的放射自显影图像的信号强度的定量
总结:本文报道了一种新型两亲性化合物LS-4的开发,LS-4对Aβ聚集体,尤其是可溶性Aβ寡聚体显示出不常见的荧光开启和高结合亲和力。体内外研究表明,采用包含连接到疏水性淀粉样原纤维结合片段的亲水性片段的两亲性分子的新策略可以增加这些化合物对可溶性和不溶性Aβ聚集体的结合亲和力,因此可以用于检测和调节AD中的各种Aβ物种。
参考文献:Liviu M。 Mirica, et al。 Amphiphilic Distyrylbenzene Derivatives as Potential Therapeutic and Imaging Agents for Soluble and Insoluble Amyloid β Aggregates in Alzheimer’s Disease。 J。 Am。 Chem。 Soc。 2021, DOI:10。1021/jacs。1c05470。
Aβ寡聚体显像-两亲性二苯乙烯基苯衍生物 | 阿尔茨海默病中可溶/不溶性淀粉样β聚集体的潜在治疗剂和显像剂
我要收藏
相关推荐
轻量化“数字孪生”3D引擎推动企业数字化转型发展

公司在 “数字孪生”核心支撑技术—3D轻量化领域已耕耘多年,形成了极具门槛的核心技术积累。截止目前,已为国内超过400家客户,涵盖制造业、工程建筑行业、高等院校,提供了3D轻量化产品及技术服务,应用于近500多个重大项目或系统平台建设。
主要产品与服务有:
(1) 3D/BIM/GIS轻量化融合引擎(WebGL/服务器端渲染);
(2) BIM/GIS施工管理平台;
(3) CAD图纸轻量化引擎(WebGL);
(4) 图模管理协同平台;
(5) 汇报演示系统;
(6) 图模查看工具;
(7) 3D可视化沙盘搭建系统;
(8) 搭建智慧工厂、化工、矿山、电力领域的3D设备模型交易平台。
领域:Web服务与集成软件
两性离子纤维素纳米纤维

纤维素纳米纤维作为一种天然的功能材料,近年来在制备、改性和应用方面已被大量的报道。纤维素纳米纤维作为一种绿色的功能材料,在油田钻采中具有非常巨大的应用潜力,然而目前最常见的纤维素纳米纤维在高盐环境中无法稳定存在,两性聚合物出色的耐盐原理为制备纤维素纳米纤维提供了新的思路。
项目通过表面修饰开发了一种纤维表面同时带有正离子和负离子集团的纤维素纳米纤维,即两性离子纤维素纳米纤维,两性离子纤维素纳米纤维的设计改变了TOCNF 在盐体系中无法适应的问题,为纤维素纳米纤维在油田钻采、海洋环境和污水处理等高盐环境中的应用提供了新的思路。
领域:新型纤维及复合材料制备技术
纸质卫生用品智能化再造

项目是基于物联⽹传感通信技术创新研发的智能护理产品。远距离监测使⽤者⼤⼩便情况、纸尿裤湿度温度、体位姿势,全天候贴⼼护⼠般提醒更换纸尿裤时间,为失能失禁⼈群提供⾼效准确的护理,是卧床护理领域的颠覆性转变。
通过可复用的夹带式/隐藏式智能传感器,一次性耗材的专用感应式成人/婴儿纸尿裤和监控APP,可以进行大小便识别、排泄超量通知 、穿戴超时提醒、湿度提醒 、翻身提醒、体温血氧心率等通知提醒,进行⽼⼈护理、妇幼护理、⽇常护理。
产品增加功能迭代规划:尿裤吸收量精确监测,数据曲线健康档案;单次尿量监测,24小时尿量曲线档案;血压血氧心率24h监测,建立历史健康档案;便尿生物标志物检测,疾病预警早筛等。
领域:其他
新型智能立体停车设备一体化解决方案

本项目为新型智能立体停车设备一体化解决方案,立体停车系统在传统机械立体停车库技术基础上,以多出入口、多通道的钢结构塔为载体,通过互联网将移动终端与立体停车库关联,通过先进的控制策略和调度系统将高效自动化机械与最优的停车路径结合,运用大数据分析对停取车潮汐现象、用户停车习惯等因素进行智能分析,实现停车策略动态化、自学习式管理,构建了一个具备安全、可靠、高效、智能、集约、便利设计全要素的新型立体停车库。
项目优势:专利技术,与现有设备差异化竞争;智能化程度更高;无需倒车,客户体验感佳;支持新能源汽车充电;应用场景广,可用于马路,河道,绿化带等;车型适配全,包括大型SUV。
领域:高端装备再制造技术
户外运动AR眼镜

公司是专注于AR眼镜领域的创新应用型企业。企业立足于科技与时尚领域,致力于为户外运动爱好者打造前所未有的动态空间视觉体验。高端、时尚、功能性强的AR眼镜,强调轻薄化设计、高清晰度显示⽰、大视场角和舒适的佩戴体验。突出产品市场元素,与品牌方合作,吸引追求个性化和时尚感的消费者。
领域:微电子系统技术
吸收自然能量,开启绿色冷源

公司是一家从事蒸发式制冷、数据中心节能、工 业余热利用等集系统研发、生产、销售、合同能源管理和售后服务为一体的高新技术企业。公司拥有五大系列产品,几十项发明和实用新型专利,专业的运营和工程服务团队,已成为中国联通、中国移动、 中国电信、中国广电等运营商的重要节能合作伙伴。间接蒸发式制冷产品包括直接蒸发/间接蒸发/多级间接蒸发/高温冷水机组/溶液调湿/金属芯体等全系列大中小型产品,定位于运营商定制化改造项目,市场潜力巨大。
领域:能源系统管理、优化与控制技术
接缝处理发展现状
接缝处理发展现状
接缝处理是指对材料之间的接缝进行加工和优化的过程,其主要目的是增强接缝的耐用性、美观性和功能性。接缝处理的方法和技术因应用场景和材料类型的不同而有所差异。
关键词:缝隙结构,影响因素,平整性,针对性,接缝处理
沥青层最大拉应变科研进展
沥青层最大拉应变科研进展
沥青层最大拉应变是一个关于沥青材料在受力情况下表现的重要参数。在路面结构中,沥青层在受到外力作用时,会产生应变,包括拉应变和压应变。最大拉应变是沥青层在拉伸过程中承受的最大应力变化量。沥青层的最大拉应变受到多种因素的影响,包括沥青材料的性质、沥青层的厚度、路面结构的设计以及外界荷载的作用等。因此,在路面工程设计和施工中,需要对沥青层的最大拉应变进行合理的计算和控制,以确保路面的安全性和耐久性。
关键词:拉应变,半刚性,有限元分析,ANSYS,沥青层最大拉应变
物候观察发展现状
物候观察发展现状
物候观察是一种对生物周期性现象与气候关系的研究和记录活动。这种观察是农耕文明的重要内容,与农业生产有直接的关联,甚至对政治、经济、文化等方面都有深远的影响。在进行物候观察时,首先需要选定一个合适的观测点。这个地点需要满足两个原则:一是地点要稳定,以便进行多年的连续观测;二是观测地点要有代表性,能够反映出当地的地形、土壤、植被等特征。选定观测点后,还需要详细记录地点的相关信息,如地名、生境、海拔、地形、位置以及土壤性质等,以便后续的分析和研究。
关键词:园艺,植物园,引种驯化,物候,世界各国,物候观察
复合式基层路面技术专利买卖交易
复合式基层路面技术专利买卖交易
复合式基层路面是指其基层由两种或多种不同类型和力学性质的结构层复合而成的路面。这种路面结构的设计旨在提高路面的承载能力、耐久性和抗水湿性能,同时降低维护成本。在复合式基层路面中,基层通常采用混凝土或沥青混凝土铺设,因其具有较高的抗压强度和较好的稳定性,可以给路面提供坚固的基础支撑。底层使用的是改性沥青混凝土或碎石等材料,其主要作用是承受车辆荷载并分散到基层,同时提供良好的排水性能,防止水分对路面结构的侵蚀。面层则通常采用耐磨层材料,如石砟、沥青等,以保证道路平整度和舒适性。
关键词:沥青混凝土,柔性材料,半刚性,半刚性基层,路面结构,复合式基层路面
平均增长系数法研发方向
平均增长系数法研发方向
平均增长系数法是一种用于预测未来出行分布或交通量分布的方法。该方法基于现状出行分布和各交通区的出行发生增长系数,通过计算起端和终端增长系数的平均值来推算未来的出行分布或交通量。具体来说,平均增长系数是出行的起端和终端增长系数的平均值。在预测未来的出行量时,可以使用以下公式:Tij^j=Tij^0×(Gi+Gj)/2,其中Tij^j表示i、j区间未来的出行量,Tij^0表示i、j区间现有的出行量,Gi表示i区的增长系数,Gj表示j区的增长系数。
关键词:系数法,出行分布,公交线路,OD,平均增长系数法
伸展构造样式技术的高校资源
伸展构造样式技术的高校资源
伸展构造样式是一种常见的地质构造样式,指的是地壳中岩石层在地质运动的作用下发生展伸的构造形态。这种构造样式在地球历史上普遍存在,对于地球科学的研究具有重要意义。伸展构造样式的形成是由于地壳内部的构造力学作用。当地壳中存在应力集中的地方,岩石层在受到压力的作用下发生断裂和展伸,形成伸展构造样式。这种构造样式通常表现为地壳的延展和拉伸,造成地壳的裂谷、断块和低陷等地质形态。
关键词:火山岩,展布,剖面,溱潼,剖面展布,伸展构造样式
城乡建设用地技术的高校资源
城乡建设用地技术的高校资源
城乡建设用地是人们生活、生产的主要场所,其特点在于相对聚集和面状分布,形态上区别于交通、水利、军事等线状或比较独立分布的建设用地。在最新的全国统一的土地利用分类系统中,城乡建设用地主要包括居民点和工矿用地中除盐田、特殊用地之外的其他用地,具体分为城镇用地和农村居民点用地两类。
关键词:结果表明,定量分析,城乡建设用地
浅褐色稃壳标记技术的高校资源
浅褐色稃壳标记技术的高校资源
“浅褐色稃壳标记”这个表述可能涉及植物学或农业领域,特别是在描述谷物或其他植物的种子外壳特征时。稃壳是禾本科植物颖果的壳,通常保护着种子。浅褐色则是对稃壳颜色的一种描述。如果这个术语用于科学研究或特定农业实践中,那么它可能有特定的含义或重要性。例如,它可能用于区分不同品种的谷物,或者用于追踪特定遗传特性的表现。
关键词:系选育,父本,光温敏核不育系,浅褐色,杂交,浅褐色稃壳标记
耦合熔融结晶制备高纯联苯的方法

本技术涉及一种从煤焦油回收洗油减压精馏后的富集联苯馏分制备高纯度联苯的方法。包括以下步骤:1、将液态...
行业:基础化学原料制造
天然健康减肥食品创制技术

人们对食品的需求已经从基本的“保障供给”向“营养健康”转变。果蔬的功效组分及其分子机制尚未阐明,从而...
行业:其他食品制造
聚丙烯系列疏水微孔膜

采用热致相分离(TIPS)方法通过制备聚丙烯系列疏水微孔膜材料,包括纯聚丙烯疏水微孔膜、聚丙烯/二氧...
行业:专用化学产品制造
风味硬质面包酥加工

该产品是在硬质面包的基础上研发而成的一款新型焙烤类休闲食品,为已授权国家发明专利产品。与现有技术相比...
行业:其他农副食品加工
海洋牌盐藻蓝莓软胶囊

视疲劳,是一种眼科常见病,由于人们长期使用电子产品、加班熬夜等不正常的生活规律,导致患视疲劳的人越来...
行业:生物药品制品制造
特种废水生态型混凝一级强化预处理与资源回收技术

天津科技大学海洋与环境学院环境工程课题组经过近七年的科学研究,成功开发了具有知识产权的、无毒生态型的...
行业:环境治理业

一种手机报警系统及方法
专利号:2014101339592
发明专利

一种微乳状有色金属脱模剂及其制备方法
专利号:2013103364382
发明专利

内燃螺栓扳手
专利号:2014102668205
发明专利

电动仿形钢轨打磨机
专利号:2014102675675
发明专利

一种免煮蕉芋粉
专利号:2014102056726
发明专利

轨枕螺栓涂油扳手
专利号:2014105526780
发明专利

项目招商
面向政府、园区提供专业项目招商服务,助力项目招引更便捷高效!
阅读数:50182

硬件世界
深耕硬件领域22年一起研究探讨硬件知识吧!
阅读数:604775

科易观点
专注技术转移十余年,如何让技术创新更为简单,问我吧!
阅读数:83672

华强电子产业研究所
电子产业成果转化与技术转移服务平台
阅读数:37238

CBG资讯
专业化学知识与经验共享平台,致力科研知识及经验的传递,欢迎来交流!
阅读数:978414

HOPE 创新生态平台
HOPE 创新生态平台 技术需求与直播活动发布
阅读数:57528

寿仁论科创
长期在科技系统工作,关于科技创新、政策法规、成果转化等,问我吧!
阅读数:177257

材料科学与工程
主要为大家分享最新材料资讯、基础知识、科研产业、考研求职等信息,欢迎交流!
阅读数:842881
-
科技项目申报系统
为地方科技项目的申报、立项、实施、变更和验收等提供信息化支撑,主要实现项目在线申报、合同签订、执行、变更、验收、审核、进度查看等功能,促进申报流程规范化、管理高效化、评审标准化、专家评审公平公正科学化
[政府园区]
-
企业创新能力画像
按照企业的规模、人才情况、知识产权、技术研发、成果转化等情况构建企业创新画像,为平台精准服务企业需求提供参考依据。
[政府园区]
-
双高招引活动及落地服务
基于地方产业发展需求,在全国范围精准挖选与地方产业相匹配的高层次人才、高技术项目资源,通过主题对接活动、重点项目考察等形式撮合地方招引部门与人才、项目的深度对接,促成高层次人才、高技术项目在地方落地。
[政府园区]
-
高校成果转化解决方案
促进高校、科研院所等的科技成果、技术能力向产业、企业进行转移转化与应用 服务对象:高等学校、科研院所、大型企业
[高校院所]
-
专精特新重点小巨人咨询申报
从工信部遴选的专精特新“小巨人”企业中择优选定;最高600万奖补
[企业服务]
-
科技成果评价
科技成果评价指对科研成果的工作质量、学术水平、实际应用和成熟程度等予以客观的、具体的、恰当的评价,并在国家科技成果登记系统完成登记,颁发成果登记证书。
[企业服务]