研究背景:三阴性乳腺癌(TNBC),一种预后非常差的乳腺癌亚型,严重威胁着女性的生命。由于TNBC的高度侵袭性限制了传统手术、放疗和化疗的有效性,因此迫切需要开发新的有效治疗方法。小干扰RNA (siRNA)介导的基因治疗,其通过特异性沉默致癌靶基因的表达而发挥作用,远优于传统药物,其低细胞毒性在肿瘤治疗中具有极大潜力。S100A4是与乳腺癌生长和转移密切相关的蛋白质之一,可以降解S100A4的mRNA并抑制相应蛋白质的表达,其表达缺陷限制了肿瘤的生长和转移。目前开发精确的肿瘤靶向和足够的siRNA递送工具仍然是高效基因治疗的挑战。为了实现精确的肿瘤靶向递送和出色的肿瘤治疗,在TME响应系统中,二氧化锰(MnO2)纳米颗粒可以作为特定药物递送的理想生物降解剂。将MnO2纳米粒子与siRNA结合可以构建一个在TNBC具有精确基因治疗潜力的递送载体。MnO2不仅作为siRNA基因传递的载体,还具有谷胱甘肽耗竭能力,可极大促进类芬顿效应,实现显著的GSH耗竭增强化学动力学疗法(CDT)。此外,利用MnO2的TME响应降解特性,还可以将其与荧光探针相结合,构建一个智能的TME可激活肿瘤定位纳米平台,这对TNBC的临床治疗具有重要意义。近年来,镧系元素荧光纳米探针由于其广泛的光谱可调范围和高灵敏度成像而被广泛开发和研究用于精确的肿瘤定位。将这种NIR-II荧光探针与MnO2结合,构建一种可以在肿瘤部位特异性激活的纳米探针,将是精确肿瘤定位的巨大进步。
解决方案:本文构建了基于二氧化锰涂覆的镧系元素纳米探针(ErNPs@ MnO2-siS100A4-RGD)的谷胱甘肽刺激响应纳米平台,用于与TNBC的CDT协同的高效siS100A4介导的精确基因治疗(图1)。与不含锰或RGD的其他纳米探针相比,ErNPs@MnO2-siS100A4-RGD表现出良好的生物相容性和优越的TNBC靶向效率。为了装载siRNA,首先在ErNPs@MnO2的表面修饰聚乙烯亚胺(PEI),通过静电吸收与siRNA连接。此外,Arg Gly Asp(RGD)多肽被修饰在制备的纳米颗粒的表面,其可以特异性结合在TNBC过表达的αvβ3蛋白,以确保纳米探针可以精确靶向肿瘤区域,以提高肿瘤富集。ErNPs@MnO2-siS100A4-RGD在肿瘤区域的纳米平台聚集并被肿瘤细胞内吞后,siRNA蛋白通过内体/溶酶体逃逸,以保护其不被降解。MnO2壳层可以被肿瘤区域中的GSH降解,同时精确释放siS100A4(图2),实现了智能的TME响应siRNA介导的基因治疗。同时,消耗谷胱甘肽后产生的Mn2+通过改善类芬顿反应,实现了对TNBC的类芬顿反应介导的CDT效应(图3)。随后,MnO2耗尽后将镧系元素纳米探针ErNPs暴露于NIR-II区的荧光发射下,实现精确的肿瘤定位。体内外结果均表明,该智能纳米平台具有较高的siRNA传递效率和谷胱甘肽响应的精确siRNA释放能力,与个体基因治疗相比,谷胱甘肽耗竭增强的CDT效应进一步增强了TNBC抑制,显示出优异的谷胱甘肽响应增强的NIR-II精确肿瘤成像治疗。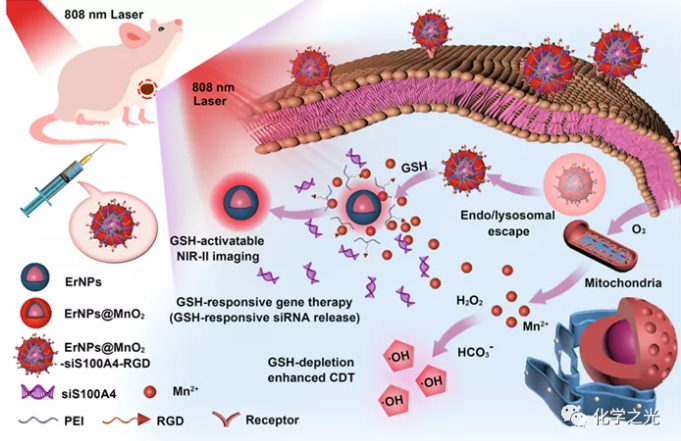 图1。 GSH刺激响应镧系掺杂NIR-II发光纳米探针与CDT协同TNBC精确基因治疗的原理图
图1。 GSH刺激响应镧系掺杂NIR-II发光纳米探针与CDT协同TNBC精确基因治疗的原理图
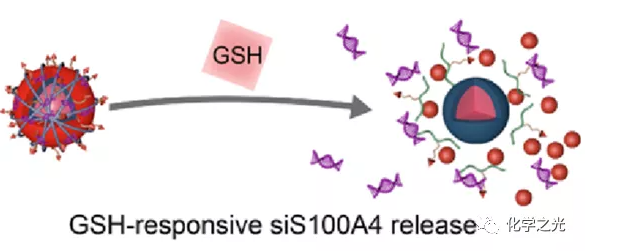
图2。 谷胱甘肽反应性siS100A4释放
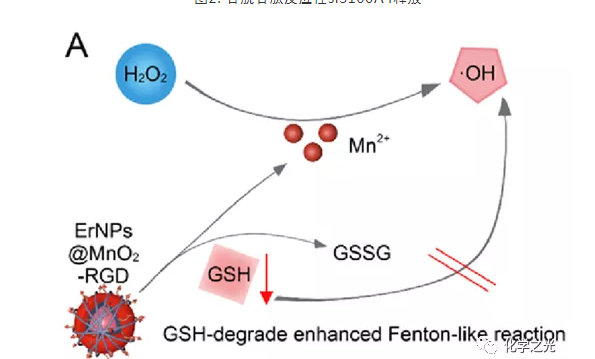
图3。 通过谷胱甘肽耗竭提高CDT效率原理
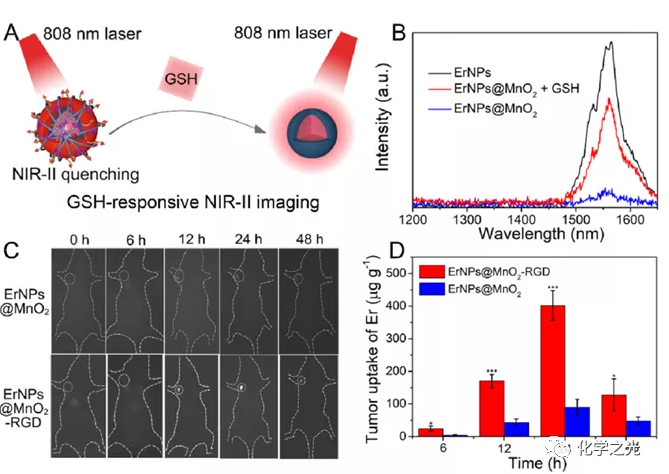
图 4。 谷胱甘肽响应的NIR-II成像
总结:本文成功设计并构建了一种新型GSH刺激响应型ErNPs@MnO2-siS100A4-RGD纳米平台,可被肿瘤区域过表达的GSH剥离,实现与CDT协同的精准肿瘤可视化siS100A4介导的高效基因治疗。基于二氧化锰的镧系元素纳米探针是一个有前途的平台,用于精确的肿瘤靶向刺激响应基因递送系统。
参考文献: Liang Song, Yun Zhang。 et al。 Smart Manganese Dioxide-Based Lanthanide Nanoprobes for Triple-Negative Breast Cancer Precise Gene Synergistic Chemodynamic Therapy。 ACS Appl。 Mater。 Interfaces。 2021。 DOI:org/10。1021/acsami。1c08927
基因治疗-智能二氧化锰基镧系纳米探针 | 三阴性乳腺癌精确基因协同化学动力学治疗
我要收藏
相关推荐
智教智学项目-综合型智能化的教育平台

公司是一家以软硬件开发、大数据运算、AI赋能、脑科学研究、神经学研究、生物研究、医学研究、农业科学研究以及自然科学研究为一体的智能型科技化的平台企业。
项目主要模式是以教学场景软硬件为切入口,全面建设数字化内容,结合数据分析、课堂软硬件设施全方位的为教师、学生、学校、家长、教委打造课前、课中、课后各个环节的综合信息化的教学监测与评估,同时家长通过手机端即可实习家校共育的同步。通过阶段性大数据的分析判断,推演出符合此阶段学生的生物特征、智力水平的教研模式,使得知识点的前后逻辑结构、每个知识点的输出时长、技巧、方法等的调整同步各个时代的学生的各项特征和水平。
项目优势:课堂教学稳定可控,备、教、辅、测、评教学环节全覆盖,与教育云平台资源互联互通。
领域:Web服务与集成软件
助力制造业数字化升级,工业元宇宙智慧化平台

通过数字孪生与人工智能算法技术,打造工业元宇宙智慧平台,为制造业提供数字化转型解决方案,集成数字工厂、工业元宇宙园区、元宇宙展会、工业三维示教系统、VR/AR解决方案等功能定制化建设。
工业元宇宙智慧化平台,以可视孪生基座,联动高性能数据,打造元动工业元宇宙智慧化平台,落地于多领域场景应用。产品优势:拥有高保真、高沉浸、高物理的渲染核心技术,采用世界领先的虚幻引擎进行底层拓展;首家在航空工业领域,提出数字智慧化解决方案,同时拥有制造业多领域数字化经验;率先将工业元宇宙落地,已有打造车企工业元宇宙厂区的案例;使用便捷、管理清晰、长效稳定,形成长效生产力工具,落地新经济对于企业的赋能。
领域:软件
一站式数字藏品资产管理平台 Web3.0时代入口级应用——数藏卡包

平台以数藏卡包为核心切入点,为千万级数字藏品爱好者提供一站式数字藏品资产管理服务,其中包括:跨平台查看资产、自动化高效流转等。在帮助广大藏家解决数字藏品资产管理繁琐问题的同时也实现可靠性、合规性强的数字资产流转。平台通过海量的藏品流转以及藏家流量来实现增值收益变现。
项目产品是一站式数字藏品资产管理平台解决方案,为藏家提供数字藏品聚合管理服务,一站式查看、管理多平台数字藏品;为藏家提供高效、自动化藏品流转,藏家安全、可靠、合规地实现藏品流转;为数字藏品发售平台提供代销服务,扶植中小平台,让优质数字藏品更多曝光;为更好匹配发售平台和IP,通过藏家众筹的方式做发售前调研,为双方合作提供数据支撑。
领域:Web服务与集成软件
吸收自然能量,开启绿色冷源

公司是一家从事蒸发式制冷、数据中心节能、工 业余热利用等集系统研发、生产、销售、合同能源管理和售后服务为一体的高新技术企业。公司拥有五大系列产品,几十项发明和实用新型专利,专业的运营和工程服务团队,已成为中国联通、中国移动、 中国电信、中国广电等运营商的重要节能合作伙伴。间接蒸发式制冷产品包括直接蒸发/间接蒸发/多级间接蒸发/高温冷水机组/溶液调湿/金属芯体等全系列大中小型产品,定位于运营商定制化改造项目,市场潜力巨大。
领域:能源系统管理、优化与控制技术
亚临界水解发酵饲料

项目以亚临界水解系统把有机物碳氢分子链打断,搭配专属发酵系统及功能肽,利用低价原料组合,形成高营养、易吸收的新型饲料。由于纤维素的多糖被部分取出,加上蛋白质和脂肪的营养分子细化,因此原料组合和成本结构发生剧烈改变。运用生物技术以精密发酵连结生物菌制程等现代生物技术,把各种动植物有机废弃物进行回收利用,能稳定制造符合饲料营养标准的低成本多肽发酵饲料,用于鸡、鸭、猪、鱼虾等禽畜类及水产类养殖,降低超过20%的饲料成本,大幅增加养殖户的获利能力及抗风险能力。
领域:农业生物技术
“TOC” 智动化工厂先行者【保密】

依托福耀玻璃、实达电脑、比亚迪、霍尼韦尔等工业大厂人才资源,以分布式前置仓为切入场景,聚焦新能源汽车供应链补链环节。项目将BOM由“物料管理”升级为“工艺包”管理,提升仓配效率,并由MRO根据时效性要求进行梯次仓配管理,降低采购隐形成本;整合本地第三方仓储供应商、本地五金店一条街资源,做标准化高效率的EDI仓和物理仓结合,更好为主机厂提供价值,降本增效;与MRO电商平台互补,用前置仓完成最后一公里覆盖,做末端服务;数据采集到EDI仓做分析,关注新能源车产业链未实现木地化配套的环节,用前置仓的方式发挥“补链”作用,构建围绕主机厂的“最后一公里供应链生态”。
领域:机器人
夹层软土技术的高校资源
夹层软土技术的高校资源
夹层软土,又称软弱夹层,是指坚硬岩层之间所夹的力学强度低、泥炭质含量高、遇水易软化、厚度较薄、延伸较远的软弱岩层。这种软弱夹层在岩体结构面中性质较差,对岩体变形和稳定件影响较大。软弱夹层的形成需要一定的物质条件和力学作用基础,通常由泥岩和粉砂岩软硬相间形成的沉积岩层结构,经过水、温度等外界因素的长期促进作用而形成。
关键词:软土,夹层,甬台温铁路,软土地基,夹层软土
资源监控发展现状
资源监控发展现状
该文设计出一种基于Client/Server分布式体系结构的局域网主机资源监控系统。文章首先介绍了系统各组成部分及功能,然后对系统实现过程中的关键技术进行阐述。实验证明,该系统的设计能有效的对局域网内各主机进行监控和管理,从而有效保护网内主机信息资源的安全性。
关键词:保护网,资源监控,体系结构,分布式
维修现状技术发展前景?
维修现状技术发展前景?
随着我国经济的不断发展,数控机床成为工业和制造业生产中不可缺少的设备,能够提高生产效率和精度,因数控机床是高精密设备,在使用中难免会发生故障,我国在维修数控机床方面较西方国家有很大差距,
关键词:提高生产效率,高精密,生产效率,维修现状
城乡经济互动产学研合作资源
城乡经济互动产学研合作资源
城乡经济互动是指在经济和社会发展的过程中,通过积极促进城乡人力、市场、信息、产业和文化等各种要素的流通,形成城乡之间全方位的沟通、联系、交流与互促机制。这种互动旨在在城乡购买力全面提高的基础上,逐步实现二者发展的动态平衡过程。城乡经济互动模式不是人的主观意识的产物,而是随着社会经济不断向前发展的必然结果,是社会经济发展到一定阶段的必然要求。
关键词:互动城乡经济,城乡经济互动,互动有利于,城乡经济,一体化
STL焦炉鼓风机三电一体化(EIC)的用途
STL焦炉鼓风机三电一体化(EIC)的用途
STL焦炉鼓风机三电一体化主要涉及到焦炉鼓风机的电气、仪表和控制三个方面的整合。这种整合旨在提高焦炉鼓风机的运行效率、安全性和可靠性,以满足焦炉生产的需求。
关键词:横河,STL,详细介绍,一体化,EIC,STL焦炉鼓风机
信息窃取技术哪里有?
信息窃取技术哪里有?
信息窃取是一种非法行为,通常涉及获取他人的个人信息、财务信息、密码等敏感数据,以用于欺诈或其他非法目的。这种行为不仅违反了个人隐私和数据保护的原则,也可能导致严重的后果,包括身份盗用、财务损失和法律追究。因此,我们应该高度重视信息安全和隐私保护,避免任何可能的信息窃取行为。这包括加强个人信息的保护、使用安全的网络和服务、定期更新软件和操作系统等措施。如果发现任何可疑的活动或受到信息窃取的威胁,应立即向相关机构报告并寻求帮助。
关键词:信息互动,网络社会,信息窃取
重组促胰岛素分泌素技术哪里有?
重组促胰岛素分泌素技术哪里有?
重组促胰岛素分泌素是一种通过基因重组技术生产的药物,旨在模拟人体生理性的胰高血糖素浓度,刺激胰腺β细胞释放胰岛素。它在糖尿病治疗中起着重要作用,主要用于控制血糖水平。在正常情况下,胰岛素是由胰腺中的胰岛β细胞合成并分泌的一种蛋白质激素。然而,当患有糖尿病时,胰岛素分泌功能可能存在缺陷,无法对血糖进行有效调节。因此,使用重组促胰岛素分泌素可以帮助刺激胰腺β细胞释放胰岛素,进而控制血糖水平。
关键词:统计学,胰岛素,生物活性,显著性,标定,重组促胰岛素分泌素
高低报警的用途
高低报警的用途
高低报警在多种领域中都有应用,特别是在涉及安全监测和警报系统的场合。在硫化氢监测仪中,高低报警值是指设定的两个不同的报警阈值,用于监测空气中硫化氢浓度的高和低水平。当硫化氢浓度超过高报警值时,监测仪会发出警报,提醒人们存在危险,这通常用于指示硫化氢浓度超过安全限制的情况,需要立即采取紧急措施。而当硫化氢浓度低于低报警值时,监测仪同样会发出警报,这通常用于指示硫化氢浓度接近安全限制的情况,此时需要采取预防措施。
关键词:RCC-E,变化范围,直流系统,放电曲线,核岛,高低报警
定向酶解生产系列乳蛋白水解物技术

本项目以酪蛋白、乳清蛋白以及牛乳蛋白作为原料,进行酶解制备低致敏性、易吸收的乳基配料。 项目制定了三...
行业:其他食品制造
风味硬质面包酥加工

该产品是在硬质面包的基础上研发而成的一款新型焙烤类休闲食品,为已授权国家发明专利产品。与现有技术相比...
行业:其他农副食品加工
红枣竹笋乳酸发酵果粒饮料

红枣竹笋植物乳杆菌乳酸发酵饮料是充分利用中国产量丰富的红枣、味道鲜美但不易保藏的竹笋所制得的饮料。虽...
行业:饮料制造
可产新型绿色重组抑菌剂的阳性毕赤酵母菌株构建技术

由抗生素引起的耐药性问题成为研究热点,寻找新型绿色的替代品成为迫在眉睫的任务。抗菌肽具有小分子量,广...
行业:生物药品制品制造
特种废水生态型混凝一级强化预处理与资源回收技术

天津科技大学海洋与环境学院环境工程课题组经过近七年的科学研究,成功开发了具有知识产权的、无毒生态型的...
行业:环境治理业
耦合熔融结晶制备高纯联苯的方法

本技术涉及一种从煤焦油回收洗油减压精馏后的富集联苯馏分制备高纯度联苯的方法。包括以下步骤:1、将液态...
行业:基础化学原料制造

一种高压线路遥控自动除雪器
专利号:201310099407X
发明专利

一种太阳能杀菌热水器
专利号:2014101710722
发明专利

一种带有自保护装置的洗衣机
专利号:2013107307092
发明专利

酸菜丝切丝机
专利号:2014103553834
发明专利

一种具有清洗装置的太阳能热水器
专利号:2014101343263
发明专利

一种手机报警系统及方法
专利号:2014101339592
发明专利

项目招商
面向政府、园区提供专业项目招商服务,助力项目招引更便捷高效!
阅读数:50165

硬件世界
深耕硬件领域22年一起研究探讨硬件知识吧!
阅读数:601342

科易观点
专注技术转移十余年,如何让技术创新更为简单,问我吧!
阅读数:83628

华强电子产业研究所
电子产业成果转化与技术转移服务平台
阅读数:37194

CBG资讯
专业化学知识与经验共享平台,致力科研知识及经验的传递,欢迎来交流!
阅读数:977369

HOPE 创新生态平台
HOPE 创新生态平台 技术需求与直播活动发布
阅读数:57461

寿仁论科创
长期在科技系统工作,关于科技创新、政策法规、成果转化等,问我吧!
阅读数:177084

材料科学与工程
主要为大家分享最新材料资讯、基础知识、科研产业、考研求职等信息,欢迎交流!
阅读数:842446
-
线上科技活动周系统
应用数据可视化技术,制作科技项目、科技成果、科技人才、典型案例等的科技活动周专题展示。
[政府园区]
-
科技特派员管理系统
科技特派员在线登记、日志填写、技术需求推送、业绩提交审核、推优评审的工作平台。
[政府园区]
-
揭榜挂帅系统
围绕产业关键核心技术和“卡脖子”技术难题,提供技术需求征集与榜单发布、揭榜与定帅、项目跟进与后续考核等科研项目组织过程的信息化支撑,支持促进揭榜挂帅工作开展。
[政府园区]
-
高校成果转化解决方案
促进高校、科研院所等的科技成果、技术能力向产业、企业进行转移转化与应用 服务对象:高等学校、科研院所、大型企业
[高校院所]
-
国家级企业技术中心申报
最高补贴300万,企业技术中心可享财政、税收、技术等全面扶持
[企业服务]
-
专精特新小巨人咨询申报
最高300万奖补,在企业技改项目、培育资助上能享受政策倾斜
[企业服务]