【写在前面】:本期推荐的是由澳门科技大学\中国科学院武汉病毒研究所\中山大学附属第一医院\首都儿科研究所\广东医科大学\广州中医药大学\澳门镜湖医院等研究团队发表于GUT(if23.059)的一篇文章,揭示人参多糖改变肠道菌群和犬尿氨酸/色氨酸比例,增强抗程序性细胞死亡1 /程序性细胞死亡配体1(anti-PD-1/PD-L1)免疫疗法的抗肿瘤作用。
【期刊简介】

图片源自杂志官网
GUT是肠胃病学和肝病学方面的国际领先期刊,在出版有关消化道,肝脏,胆道和胰腺的一流临床研究方面享有盛誉。在胃肠病学和肝病学的所有领域提供最新的,权威的,以临床为导向的报道。 定期发表的文章包括主要机构的文章,这些文章描述了可能在可预见的将来对临床实践产生影响的新型疾病机制以及诊断和治疗新的治疗策略。
选择性的OA期刊,审稿周期一般为1~3个月。版面费2,500 GBP。
【题目及作者信息】


【摘要】
设计思路:给同基因小鼠模型灌胃GPs和αPD-1mAb,通过粪便微生物菌群移植(FMT)和16S PacBio单分子实时(SMRT)测序评估联合治疗对肠道菌群的敏化抗肿瘤作用。为了评估免疫相关的代谢产物,对血浆样品进行了代谢组学分析。
结果:我们发现GPs通过增加微生物代谢产物戊酸和降低L-犬尿氨酸以及Kyn / Trp的比例来增加对αPD-1mAb的抗肿瘤反应,这有助于抑制调节性T细胞并在诱导后Teff细胞诱导联合治疗。此外,微生物分析表明,在临床上对PD-1阻滞剂的响应者中,副细菌副杆菌和寻常型细菌的含量高于未响应者。此外,联合疗法通过将肠道菌群从无反应者重塑成有反应者而使从六种无反应者接受FMT的小鼠对PD-1抑制剂的反应敏感。
结论:我们的结果表明,GPs与αPD-1mAb结合可能是使非小细胞肺癌患者对PD-1免疫治疗敏感的一种新策略。肠道菌群可用作预测抗PD-1免疫疗法反应的新型生物标志物。

图文摘要

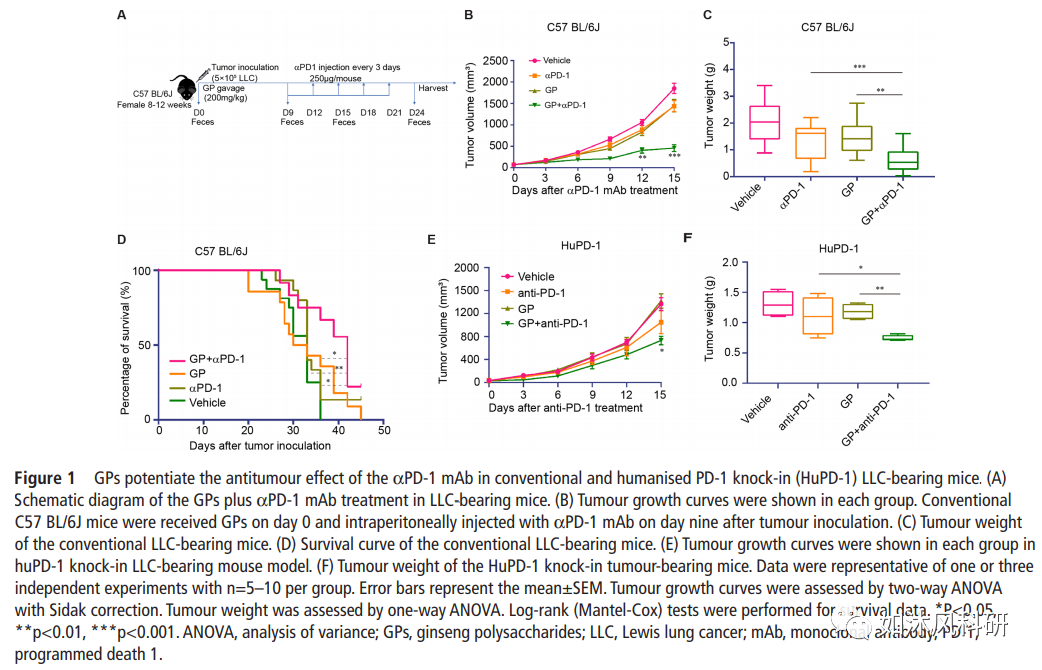
1.GP在常规和人源化PD-1敲入(HuPD-1)LLC的小鼠中增强了αPD-1mAb的抗肿瘤作用.

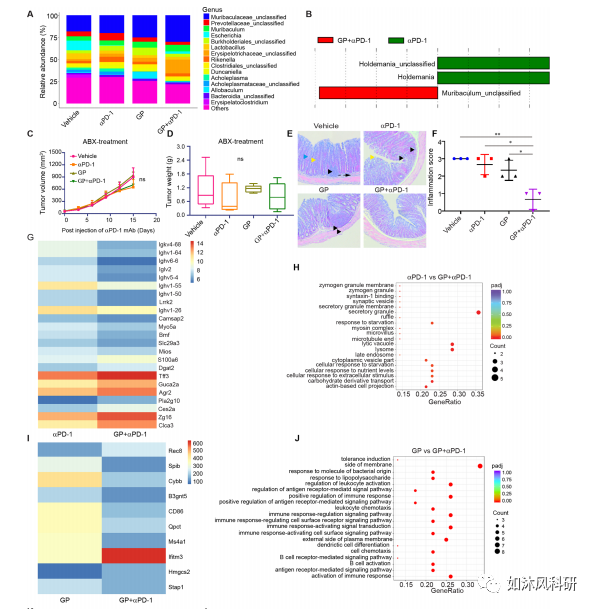

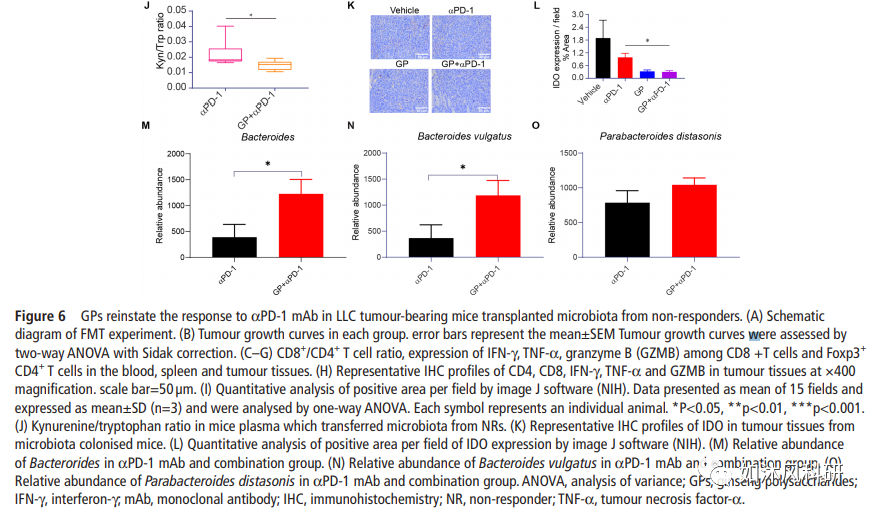
6.GPs恢复了从无反应者移植了微生物菌群的LLC荷瘤小鼠对αPD-1mAb的反应。

7.图文摘要:GPs与αPD-1mAb结合可通过恢复肠道菌群来提高反应率。
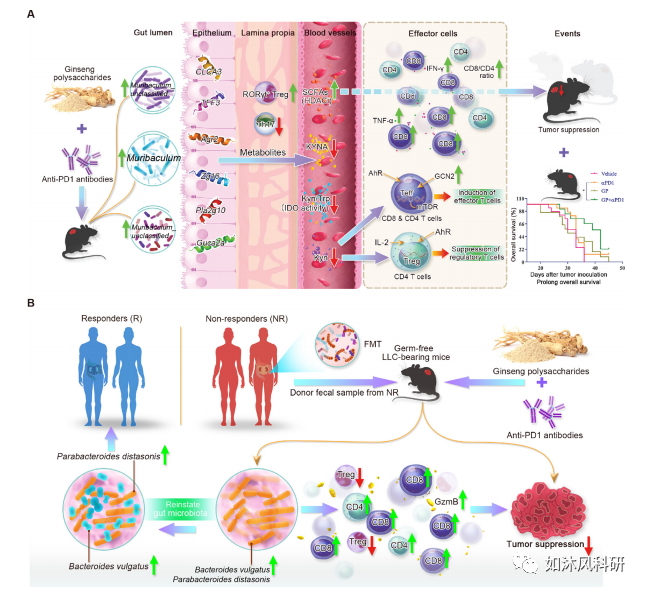
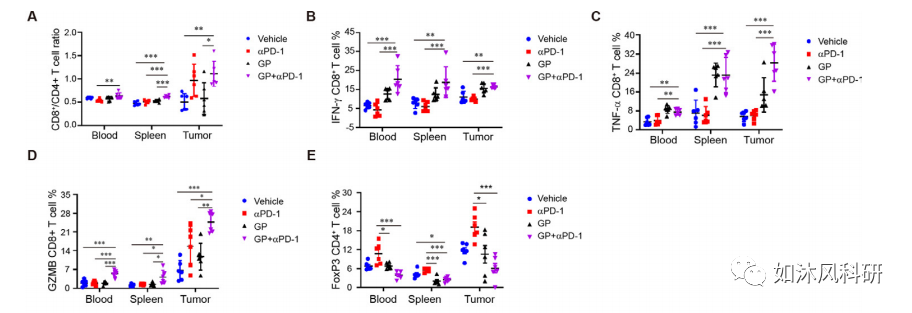
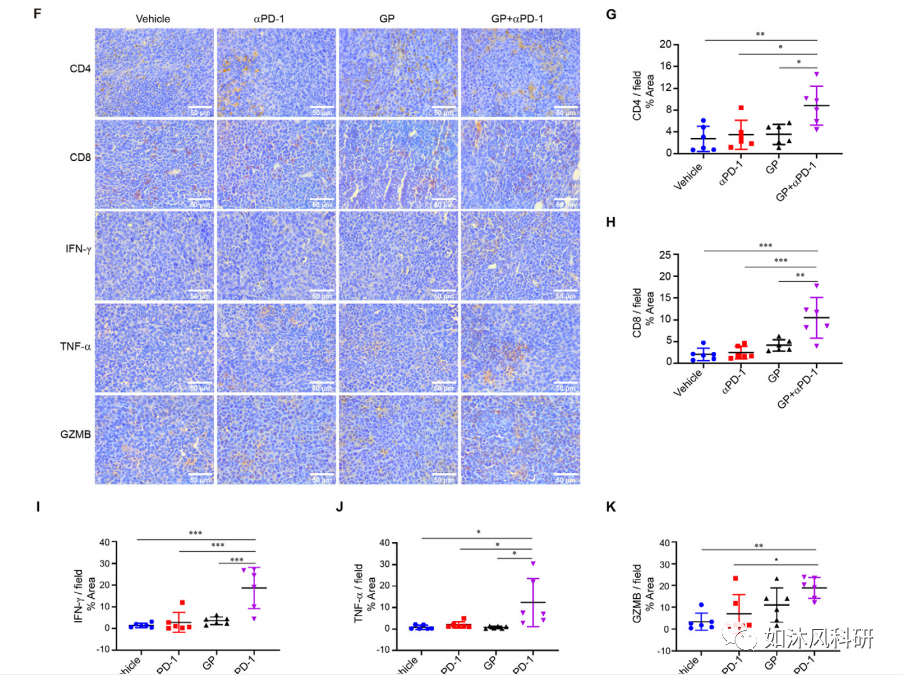
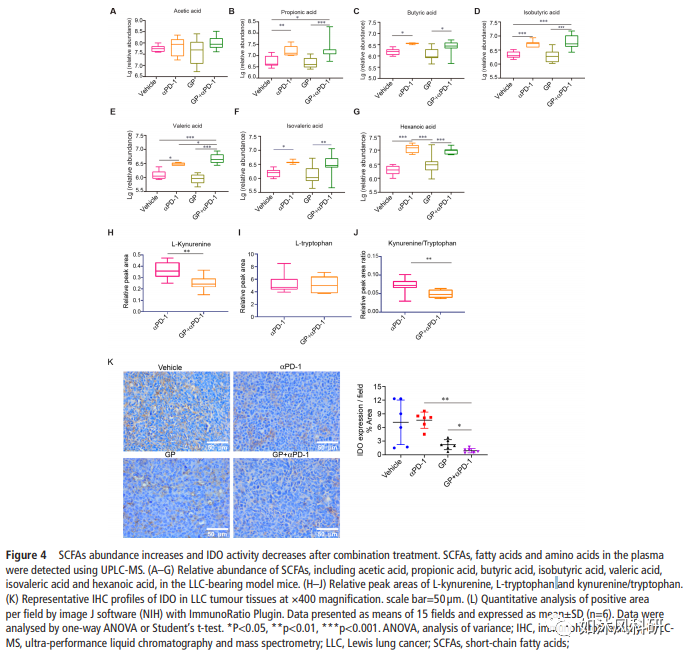
(A)GPs通过增强CD8 T细胞功能,增加IFN-γ和TNF-α的产生以及降低Treg在循环系统中的抑制作用来增强αPD-1mAb的抗肿瘤作用,这可以通过重塑肠道菌群来解决因此会影响色氨酸的代谢和SCFA。联合处理可增加含LLC小鼠的幽门螺杆菌的丰度。联合治疗上调了CLCA3,TFF3,AGR2,Zg16,Pla2g10和Guca2a等上皮保护基因的表达。代谢产物SFCA和犬尿氨酸进入血液循环系统并增强免疫功能,从而抑制了肿瘤的生长并延长了生存期。
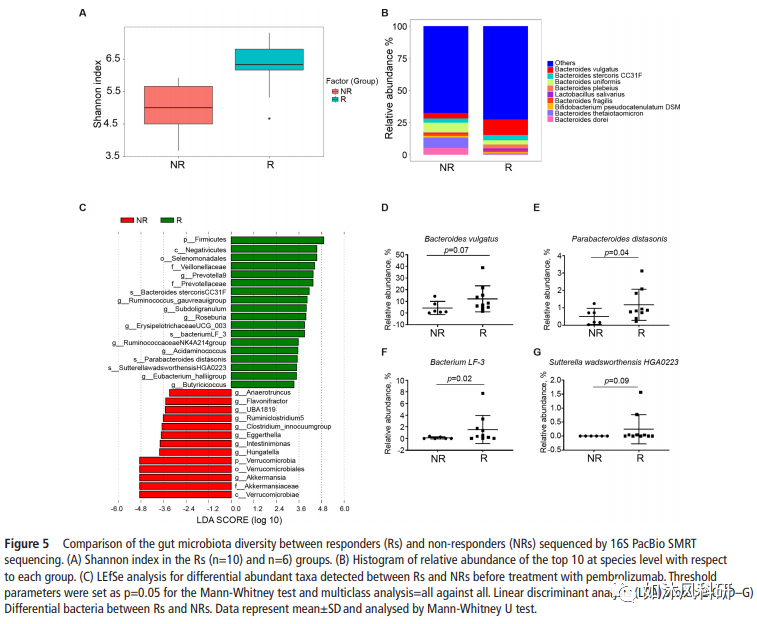
(B)联合疗法恢复了肠道菌群,这有助于将肠道菌群从无反应者恢复为反应者,从而增强了对αPD-1mAb的反应。通过16S SMRT测序发现,对pembrolizumab的应答者中,副细菌副杆菌和寻常型拟杆菌(Bacteroides vulgatus)含量较高。当通过粪便微生物群移植(FMT)将肠道微生物群从无反应者移植到无菌小鼠中,然后在定植后接种LLC肿瘤细胞时,对小鼠进行联合治疗。与αPD-1mAb和媒介物组相比,通过16S PacBio SMRT测序在组合组中发现了丰富的寻常型芽孢杆菌和排球假单胞菌。同时,联合疗法可通过增强CD8 + T细胞的功能,增加IFN-γ,TNF-α和颗粒酶B的产生并减少Treg细胞来显着抑制肿瘤的生长。