由于具有优良的代谢稳定性及药代动力学性质,苄基醚,尤其是结构复杂的苄基醚类化合物,是许多药物分子的重要基本骨架。毫无疑问,这类化合物的合成已引起化学家们的广泛关注(Scheme 1)。
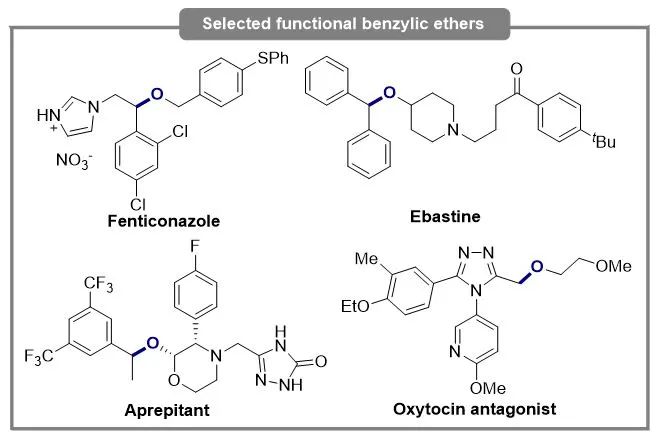
Scheme 1. Selected bioactive compounds that contain benzylic ethers functionality.
(来源:Org. Chem. Front.)
苄基碳氢键的烷氧基化,即在氧化还原条件下实现O-H和C-H键的交叉偶联反应无疑是合成此类化合物最直接有效的方法。然而,常规的此类方法由于较低的反应活性,通常需要将醇类底物用作大大过量的溶剂,这也极大地限制了此类反应的应用范围。近期,威斯康星大学的Yoon课题组发展一例可见光催化的选择性苄基碳氢键烷氧基化方法,高效地以2当量的醇类作为底物;然而,化学计量级的高氧化态铜(II)催化剂的使用使得其碳氢键底物仅限制于富电子芳杂环(Scheme 2a)。为了解决这一问题,威斯康星大学的Stahl课题组发展了一种铜/NFSI催化的苄基碳氢键烷氧基化方法,其独特的自由基传递机制可以使碳氢键底物同时适用于含有供电子基团和吸电子基团的底物(Scheme 2b)。然而,这种方法同样由于使用了高氧化性的铜(II)催化剂,导致反应中产生大量的酮类副产物,此类方法仍然有待发展。最近,嘉兴学院医学院刘石惠报道了一种可见光/镍共催化的苄基碳氢键烷氧基化方法,该方法表现出广泛的底物范围的同时还具有极高的区域选择性和化学选择性(Scheme 2c)。相关研究成果发表在Org. Chem. Front.上(DOI: 10.1039/D1QO01421H)。
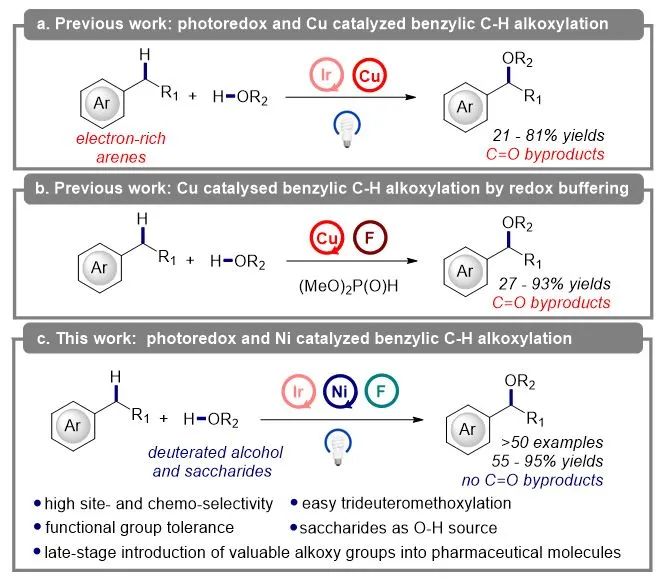
Scheme 2. C-H/O-H cross-coupling reactions of benzylic C-H bonds and alcohols via a radical relay pathway.
(来源:Org. Chem. Front.)
作者以1-乙基萘(1)和氘代甲醇(2a)作为模型底物进行研究。经过对光催化剂、镍催化剂、配体、氧化剂和溶剂等条件的大量筛选,确定反应的最佳条件为:1-乙基萘(1)和氘代甲醇(2a)在[Ir{dF(CF3)ppy}2(dtbbpy)]PF6,Ni(acac)2,bpy以及Selectfluor的条件下,在12 W Blue Leds, 40 ℃条件下反应24小时,以81%的收率得到产物3a(Table 1)。值得强调的是,该条件下并未观察到酮类副产物3’。
Table 1. Optimization studies for trideuteromethoxylation of benzylic C-H Bonds. A

a Conditions employed 12 W Blue Leds, 1 (0.5 mmol), 2a (2.5 mmol), [Ir{dF(CF3)ppy}2(dtbbpy)]PF6 (1 mol%), Ni(acac)2 (10 mol%), bpy (10 mol%), Selectfluor (1.0 mmol), CH3CN (2.5 mL), the reaction mixture was degassed via freeze pump thaw (× 3 times) and refilled with N2, 40 ℃ 24 h, unless otherwise noted; b Isolated yields were reported; c Yields were determined by 1H NMR using 1,3,5-trimethoxybenzene as an internal standard; d not detected.
(来源:Org. Chem. Front.)
得到最佳条件后,作者考察了该反应的普适性(Scheme 3)。各种取代的苄基碳氢键底物均表现出良好的适用性。
Scheme 3. Trideuteromethoxylation of various benzylic C-H substrates. a
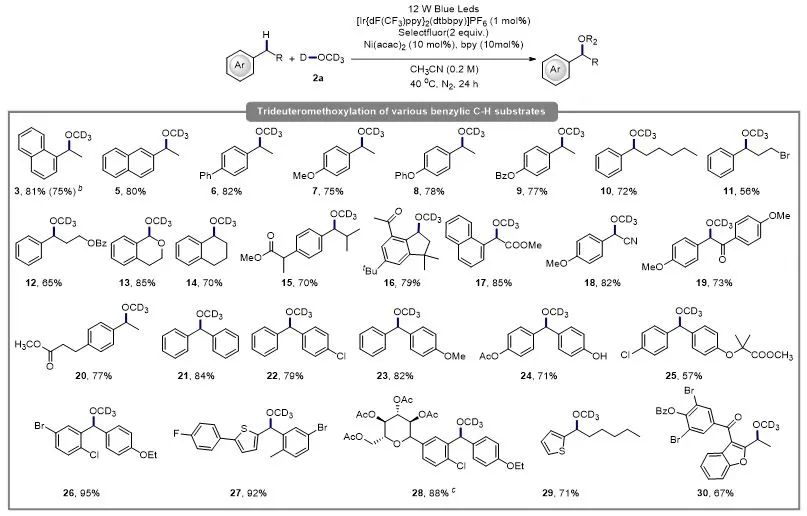
a Conditions employed 12 W Blue Leds, benzylic C-H substrate (0.5 mmol), 2a (2.5 mmol), [Ir{dF(CF3)ppy}2(dtbbpy)]PF6 (1 mol%), Ni(acac)2 (0.05 mmol), bpy (0.05 mmol), Selectfluor (1.0 mmol), CH3CN (2.5 mL), the reaction mixture was degassed via freeze pump thaw (× 3 times) and refilled with N2, 40 ℃, 24 h, isolated yields were reported, unless otherwise noted. b Performed on 10 mmol scale, 48 h. c Diastereomeric ratio (d.r.) determined using 1H NMR spectroscopy. 28, 1.09:1 d.r.
(来源:Org. Chem. Front.)
随后,作者考察了各种醇类底物的适用范围(Scheme 4)。各种醇类底物也都表现出较好的适用性。
Scheme 4. Reaction scope of various alcohols in benzylic C-H alkoxylation. a

a Conditions employed 12 W Blue Leds, 1 (0.5 mmol), alcohol (2.5 mmol), [Ir{dF(CF3)ppy}2(dtbbpy)]PF6 (1 mol%), Ni(acac)2 (10 mol%), bpy (10 mol%), Selectfluor (1.0 mmol), CH3CN (2.5 mL), the reaction mixture was degassed via freeze pump thaw (× 3 times) and refilled with N2, 40 ℃, 24 h, isolated yields were reported, unless otherwise noted; b Diastereomeric ratio (d.r.) determined using 1H NMR spectroscopy. 41, 1:1 d.r.; 42, 1.1:1 d.r.; 48, 1.2:1 d.r.; 50, 1:1 d.r.; 53, 1:1 d.r.; 54, 1.08:1 d.r.; 55, 1.2:1 d.r.; 56, 1.1:1 d.r.; 57, 1:1 d.r.; 58, 1:1 d.r.; 59, 1.13:1 d.r.
(来源:Org. Chem. Front.)
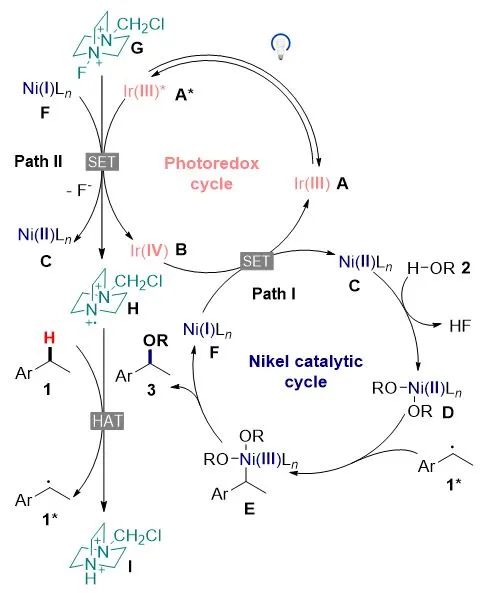
结合实验结果和相关文献,作者初步探索了反应机理(Scheme 5)。光催化剂(A)在光照条件下产生激发态的(A*),它将电子传递给Selecfluor(G),相应的生成氮正离子自由基(H)和氟负离子,氮正离子自由基(H)与化合物(1)之间发生氢原子转移(HAT)后生成相应的自由基(1*)。反应中的二价镍(C)与甲醇(2)配位生成中间体(D),中间体(D)可以快速捕获自由基(1*)进而生成中间体(E),中间体(E)经过还原消除得到产物(3)。
Scheme 5. Proposed mechanism for photoredox and nickel dual-catalyzed benzylic C-H alkoxylation.
(来源:Org. Chem. Front.)
总之,作者发展了一种可见光/镍共催化的苄基碳氢键烷氧基化方法。这种方法可以以中等至优异的产率合成结构多样的功能性苄基醚,具有很高的区域选择性和化学选择性。商业可得的氘代甲醇作为三氘甲氧基化源以及糖类化合物的顺利转化是本研究的亮点,这一方法为结构复杂的苄基醚类的合成提供了一种实用的新工具。
本文授权转载自微信公众号「CBG资讯」,未经许可谢绝二次转载,如需转载请联系C菌(微信号:chembeango101)