概论
在生物制药、结构研究、体外生物化学分析等很多应用中都需要进行蛋白质等生物分子纯化。蛋白质可以从组织中获取,亦或更经常的是从模式生物中过量表达获得,如细菌、酵母或哺乳动物细胞培养等。蛋白质纯化主要是根据它们理化性质的差异来从原料种进行分离纯化,其目的就是获得最多且高纯度的功能蛋白质。一个好的蛋白质的纯化过程必须要将其纯化工艺步骤优化至最少。
建立蛋白质纯化工艺时,最重要的是需要考虑纯化得到的蛋白质应能满足其后续应用要求。蛋白质的含量及纯度都必须满足应用要求。而且,因为后续应用需要的是保持良好折叠结构的活性蛋白质,因此蛋白质活性的相关信息也需要考虑。在纯化及后续的保存过程中,很多处理方法都会对蛋白质的性质产生影响,如蛋白质的去折叠、聚集、降解和失活等。制定详细计划,在最短时间内完成蛋白质纯化,并在最稳定的条件下进行保存才算是成功地完成了其整个纯化过程。

缓冲液的建立
每一步纯化过程中,蛋白质的溶液环境对其稳定性和活性的保持都非常关键。蛋白质应该保存在一个良好的缓冲液环境中,要避免突然的pH值变化,以其防止对蛋白质折叠状态、溶解性和活性造成不可逆的影响。
缓冲液是一种含有共轭酸/碱对的水溶液。缓冲液的pH值范围根据其pKa值决定。该pKa值定义为50%的分子为酸式结构,50%为碱式结构时的pH值 (图1)。
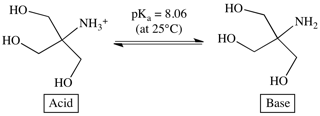
图 1. 含Tris碱及其酸式物的Tris缓冲液溶液。Tris 25°C的pKa值是8.06,表示当pH=8.06,50%的Tris是质子化(酸式结构),50%是去质子化(碱式结构)。
关于缓冲液的一个常规原则是,其pH值应保证在pKa值左右1个pH值单位范围内,从而保证其具有良好的缓冲能力。如此可以保证同时有足够的以酸式结构和碱式结构存在的分子在加入 H+ 或者 OH- 时可以将它们中和。这样,缓冲液就可以防止pH变化导致的蛋白质稳定性改变。
一种好的缓冲液应具备以下特征:
很多物质都可以用于生物缓冲液。最常使用的缓冲液成分通常具有接近中性的pKa值,可在生理pH值范围左右使用。表1列出了4种最常用的生物缓冲液、各自的pH值应用范围及各自可能对蛋白质纯化过程产生影响的优缺点。为保证足够的缓冲能力,这些缓冲液的浓度通常为20mM。
| 缓冲液 | pH范围 | 优缺点 |
|---|---|---|
| 磷酸缓冲液 | 5.8-8.0 |
|
| MOPS缓冲液 | 6.5-7.9 |
|
| HEPES缓冲液 | 6.8-8.2 |
|
| Tris缓冲液 | 7.5-9.0 |
|
表一:蛋白质纯化中最常用的生物缓冲液。缓冲液在一定pH值范围内可保持它们的缓冲能力,部分缓冲液成分会对某些层析过程或者分析实验造成影响。

溶液添加剂
除了一个合适的缓冲液体系,蛋白质纯化过程中——从溶菌到保存——所使用的溶液通常还含有很多其他对蛋白质纯度、稳定性和活性方面均具有一定作用的成分。
溶菌缓冲液和纯化工艺的前期步骤中常常会添加蛋白酶抑制剂以防止目标蛋白质被内源性蛋白酶酶解。而纯化工艺的后期一般不用再添加这些蛋白酶抑制剂,因为此时几乎所有的蛋白酶都已经从目标蛋白质分离出去。蛋白质的保存缓冲液中通常要添加金属螯合剂,如EDTA或EGTA。这些金属螯合剂与 Mg2+结合以防止目标蛋白质被所含的金属蛋白酶分解。还有一些其他的添加剂,主要是用来保护蛋白质不被破坏和增强其溶解性。
| 类型 | 功能 | 常用试剂 |
|---|---|---|
| 还原剂 | 防止氧化 |
|
| 蛋白酶抑制剂 | 防止内源性蛋白酶分解蛋白 |
|
| 金属螯合剂 | 使金属蛋白酶失活 |
|
| 精氨酸激酶 | 稳定蛋白质结构,增强溶解性 |
|
| 离子稳定剂 | 增强溶解性 | 盐类 (如NaCl、KCl、(NH4)2SO4 |
表二:蛋白质纯化中用于增强蛋白质稳定性的常用添加剂。
添加剂只在必要时才使用。可能需要多次尝试才能确定某些添加剂是否对一些特定蛋白质的纯化工艺有效。

其它因素
蛋白质纯化工艺中的其他因素也会对蛋白质的稳定性产生影响。对蛋白质的处理步骤越少越好,在最短时间内采用最少步骤的纯化工艺才能保证得到最高产率的活性蛋白质。而且,在整个纯化过程中,蛋白质最好都保持在低温状态。一般纯化过程都在4°C进行,因为这个温度既可以降低酶解速度(在含有蛋白酶的情况下),又可以保证蛋白质的结构完整性。

表达体系对蛋白纯化的影响
开始纯化蛋白前应先制备初始样品。真正进行蛋白纯化的操作之前,首要考虑是目的蛋白的来源。样品来源可为原始样品,例如肝脏,肌肉或脑组织。当前,更为常见的是从重组来源的样品纯化蛋白质。一些重要决定需要提前考虑以便优化后续的纯化。研究者需要考虑蛋白质的最终用途(例如治疗性生物药,酶测定,结构研究,抗体生成),因为这将决定最终蛋白质制备所需的量和纯度。尽管蛋白质表达的详细讨论超出本文范围,但是在这一点上仍有几个值得考虑的基本点,因为它们直接影响后续的蛋白纯化。
如果选择大肠杆菌表达系统,最终目的可溶性表达或包涵体形式,由于包涵体中有高丰度的重组蛋白,包涵体的分离本身构成了纯化的重要步骤; 这必须与溶解难易和随后包涵体中再折叠靶蛋白的难易以及可溶性蛋白的最终产量相平衡 [1] 。已经有许多工作优化了从包涵体中产生功能蛋白的产量 [2] 。
另一个考虑是是否靶向胞内或胞外(分泌的)表达。胞内表达需要将蛋白质从大量宿主细胞蛋白中纯化而来。相比之下,特别是当宿主细胞在无血清条件下生长时 [3] ,目标蛋白的有效分泌要求蛋白必须从少量分泌的宿主蛋白中纯化而来。

初始样品制备
无论目标蛋白的来源如何,作为纯化的初始步骤,原始样品的制备很重要。同时也需要考虑表达和纯化策略。
目标蛋白的胞外分泌可使用简单快速亲和纯化方案 [3] ;所需的唯一样品制备可能需要倾倒贴壁细胞的条件培养基或者低速离心以去除悬浮细胞。当然,制备过程的第一步亲和层析时可能需要加入蛋白酶抑制剂或者调节pH,但这些步骤简单易行。然而,如果第一步纯化样品步骤进行离子交换,样品则可能需要首先脱盐或者缓冲液置换。
如果靶蛋白在胞内表达,则细胞首先需要通过离心获取,然后用合适的裂解缓冲液重悬。如上所述,裂解缓冲液需要包含合适的缓冲液和其它添加剂以确保靶蛋白的最大稳定性。如果研究者在柱层析之前避免耗时的缓冲液置换步骤,则样品/裂解缓冲液的组成也需与随后的纯化步骤相适宜。
接下来,需要有效的细胞裂解方法。大肠杆菌可以通过弗氏压碎器裂解(尽管这种方法不容易规模化),超声或基于洗涤剂的裂解(有很多商业裂解试剂)。通过向裂解缓冲液中加入溶菌酶可以改善基于洗涤剂的裂解效率。基于洗涤剂的裂解非常温和,且不导致细菌DNA的显着切变。因此,为了降低样品粘度产生具有良好流动特性的样品,通常需要加入核酸酶孵育(高纯度制剂可商购) [4] 。
哺乳动物和昆虫细胞也可以通过超声或基于洗涤剂的方法裂解。如果核膜显着裂解,可能需要核酸酶处理降低样品粘度 [4] 。
一旦细胞(微生物/昆虫/哺乳动物)被裂解,通常需要离心或者微滤除去细胞碎片(通常在4℃下15000×g离心15分钟,或者用0.22-0.45um的膜组件过滤,以避免层析柱堵塞) [4] 。所得上清液即可开始用于靶蛋白的柱层析纯化。

参考资料