蛋白纯化过程中的缓冲液置换
为了确保蛋白质所在的缓冲体系和下游纯化过程的缓冲体系保持一致.也就是蛋白质所在环境的pH,盐浓度要和纯化过程的保持一致,以求最佳的纯化过程.确保蛋白质纯化过程中保持活性,提高纯化倍数,提高回收率,降低过程成本等。
蛋白所在缓冲液环境无法满足后续纯化时,就需要缓冲液置换。
1.分泌表达的蛋白,蛋白所在环境中培养基成分较多,影响后续工艺,此时就需要置换缓冲液,如SF9细胞分泌表达的his蛋白用NiSe plife FF(NTA)纯化时,因其培养基成分复杂,影响his蛋白和镍柱的结合或影响镍柱的性能,此时就需要缓冲液置换。
2.蛋白经离子交换层析及部分亲和层析如肝素亲和及金属螯合亲和层析后,在继续下一步离子层析时通常需要把上一步洗脱液中高浓度的盐去除掉,此时就要脱盐处理,脱盐处理的过程也是缓冲液置换的过程。
3.蛋白经离子交换层析及部分亲和层析后,在保存之前通常都要将缓冲体系中的盐降低到一定程度,此时也需要缓冲液置换。
4.包涵体蛋白用变性剂溶解后,在复性的过程中要将变性剂去除,这个过程也涉及到缓冲液置换。
缓冲液置换的常用方法主要有膜法(透析及超滤)和凝胶过滤层析两种方式。除此之外一些情况下也可以通过稀释的方式达到缓冲液的置换,如包涵体溶解后去变性剂的过程通常用稀释的方式去除变性剂,以此达到缓冲液置换的目的,去除变性剂完成蛋白复性。
1.透析法置换缓冲液
透析是利用半透性膜将蛋白质溶液包裹,沉浸在透析缓冲液中,由于缓冲液浓度低于膜内部的浓度,因此在半透膜上会发生物质交换;但蛋白质不能通过半透膜,只有盐离子等小分子物质可以通过;因此蛋白质溶液中的盐杂质就通过半透膜交换到外面了.

注:图片选自搜狗图片(透析示意图)
透析缓冲液的体积越大,小分子扩散的驱动力越大。我们一般推荐缓冲液和样品的体积比为100:1,最佳为500:1。当扩散速率降低,膜两侧溶液趋于平衡时,通过置换缓冲液,可维持小分子扩散驱动力和透析速率。我们一般推荐在12-24小时内,置换缓冲液2到3次,具体安排如下:
第一次缓冲液置换:透析开始后2-3小时
第二次缓冲液置换:透析开始后4-5小时
最后一次缓冲液置换:透析隔夜之前
透析法置换缓冲液,因周期较长,且需要大量的置换液,使其应用受到很大的限制,工业上用的较少,主要在实验室有部分仍在使用,实验室也逐渐被超滤管/超滤杯及凝胶过滤层析所替代。
2.凝胶过滤层析
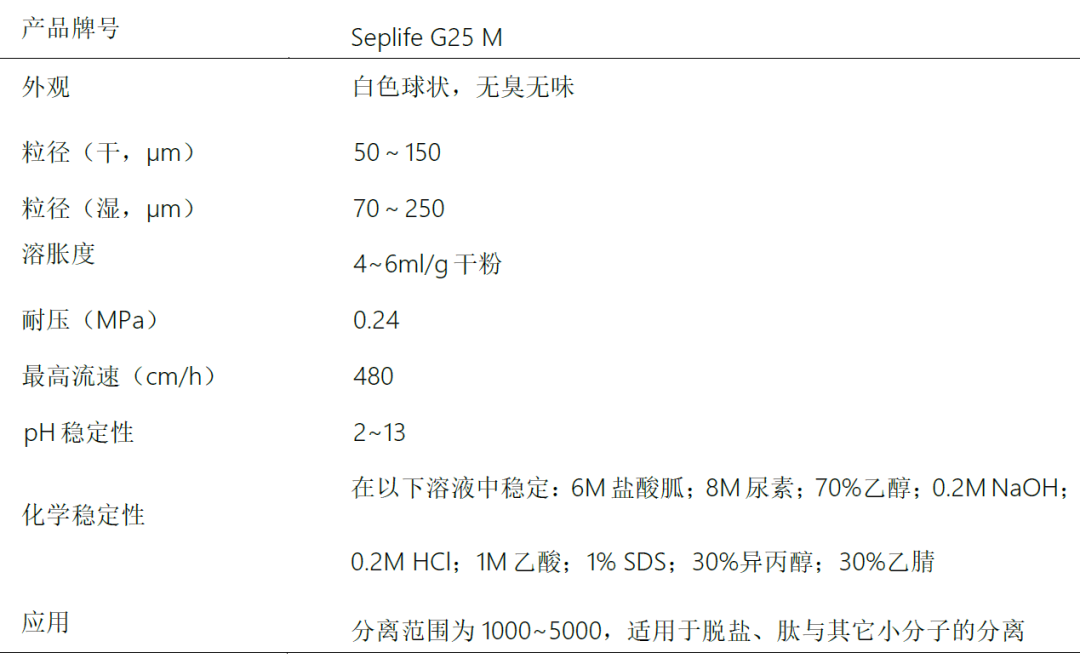
Seplife G-25 凝胶过滤介质广泛应用于生物大分子的脱盐和缓冲液置换,因其过程温和,被广泛应用到生物制药工艺中,特别是在离心交换及亲和后脱盐及缓冲液置换中应用普遍。
Seplife G-25性能参数
3.超滤
超滤法是一种膜滤法,它以多孔薄膜作为分离介质,依靠薄膜两侧压力差作为推动力来分离溶液中不同分子量的物质,从而起到脱盐浓缩作用提纯等作用的方法。它具有不存在相的转换、不需加热、能量消耗少、操作条件温和、不必添加化学试剂、不损坏热敏药物等优点。
超滤法从实验室微量处理的超滤管,小量处理的超滤杯,及工业上的超滤系统技术都比较成熟。
超滤又分为直压超滤和切向流过滤两种,目前工业上主要是切向流过滤为主,在脱盐及缓冲液置换中被广泛应用。
从左到右分别:超滤管,超滤杯,超滤膜包