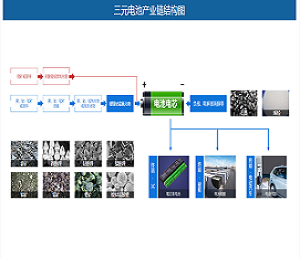
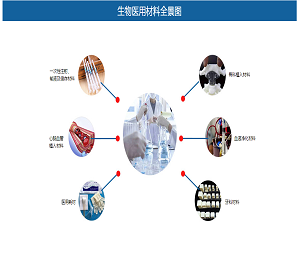
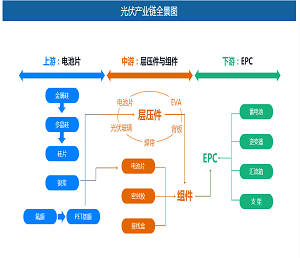
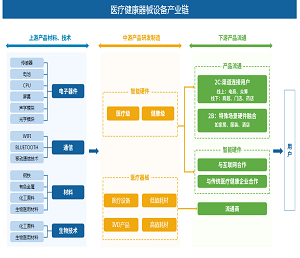
抗体药临床Ⅰ,Ⅱ期填料变更策略
通常,临床 I、II 期的工艺相对粗糙,未经仔细优化,一些主要步骤的工艺步骤例如离子层析(AC,CEX 和 AEX)可能不适合将来工业化生产。因此,需要在生产临床III期用药时对工艺进行变更优化,以保证将来工业生产的重现性、稳定性和可放大性。临床Ⅰ.Ⅱ期工艺优化使其更适用大规模商业化生产,这个阶段工艺优化过程中,填料种类,填料供应商都可以任意变更,此阶段填料变更,填料供应商变更只是工艺优化的一部分,不需要做变更样品申报等操作,比较简单。在这个阶段,填料国产化,只需将现有填料用国产等效或更优的填料替换即可。

抗体药商业化生产阶段填料变更策略
变更的原则
1.任何生产过程的改动都是以提高产品的安全性和有效性为基本出发点,在提高或至少不改变最初国家批准产品安全性和有效性的基础上进行相关改进。
2.拟进行生产过程变更的生产企业应向NMPA提出申请,并递交相关方案和资料,提供证明资料,说明该变更不引起产品质量的内在变化,由NMPA组织专家进行审查并确定变更的类型及应递交的相关材料。
3.抗体药工艺中填料变更属于中等变更。
填料变更操作过程
需要向商业化生产地的省级CDE提交以下资料:
1.变更说明:如进口填料变更为蓝晓科技填料
2.变更验证资料:如将进口填料变更为蓝晓科技Protein A Seplife Suno亲和填料,这个填料在工艺中的作用在工艺允许的范围内。
3.变更前后主要有效成分生物学变化的研究:如Protein A填料国产化后,IgG的生物活性研究报告。
4.变更前后3批生产规模产品质量分析资料,包括生产各关键阶段中间产品、原液及终产品的分析、检测及稳定性研究资料。如生产是1000L原液,Protein A填料变更后,在1000L原液这个规模做三批产品并提交这三排产品的质量分析资料。

FDA DMF备案rProtein A填料介绍

蓝晓科技rProtein A填料通过FDA DMF备案
蓝晓科技自主开发拥有专利的rProtein A系列蛋白A亲和填料于2022年7月14日通过美国FDA DMF备案(MF#:037326),成为国内为数不多的通过FDA DMF备案的国产填料供应商。这意味着使用蓝晓科技相关产品的客户,在向FDA提交进行新药注册的监管备案文件中可直接引用DMF备案资料,而无需再提供有关原料和辅料的具体信息。
rProtein A Seplife Suno/Suni是蓝晓科技应对抗体客户需求推出的Protein A亲和层析填料,以球形,高交联琼脂糖凝胶为基质,通过自主创新技术将耐碱性重组蛋白A键合到该基质上。可以特异性地与抗体的Fc区结合,用于抗体(单抗和多抗)的分离纯化,只需一步亲和层析,即可从腹水、血清或培养液等样品中得到高纯度的抗体。
具有以下特点
✔自主研发,品质保证,专利保证
✔高载量:5min保留时间载量80mg/ml
✔耐碱性好:耐受0.5M NaOH
✔完整的支持文件:RSF、DMF、MSDS、TSE/BSE
✔低配基脱落:小于 2 ppm
✔货期短,1-2周可以交

苏州蓝晓生物科技有限公司是蓝晓科技(股票代码:SZ 300487)全资子公司,依托蓝晓科技20多年在分离吸附材料领域丰富的经验和技术积累,在后疫情时代及药品集采的时代背景下应运而生。苏州蓝晓生物科技,在蓝晓科技雄厚资本的支持下,在蓝晓科技生命科学事业部数10年产品研发和技术积累的基础上,汇聚50多人的研发团队,提供从细胞培养及分离纯化到系统装置完整的解决方案,我们将全力助力生命科学及生物制药产业的高质量发展。