找到74项技术成果数据。
找技术 >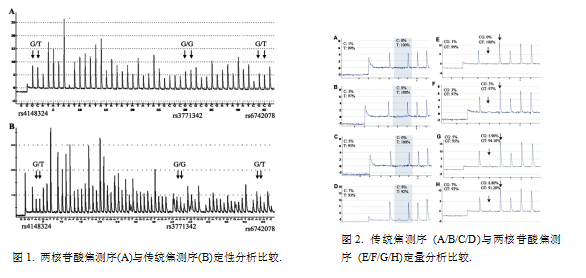
两核苷酸合成焦测序仪及其核酸体外诊断试剂盒
成熟度:通过中试
技术类型:-
应用行业:制造业
技术简介
两核苷酸合成焦测序仪依据于自主知识产权的两核苷酸合成测序原理(Analytica Chimica Acta, 2014,852,274-283),不仅可以替代现有进口焦测序仪的应用领域、并满足解决直接检测PCR 产物的单倍型等分子关联分析等需求、为“精准医疗”检测核酸标志物提供临床硬件支撑。 核酸体外诊断试剂盒依据两核苷酸合成测序具有更长测序长度、更低检测限等特点(Analytical and Bioanalytical Chemistry, 408(12),3113-3123),发展针对疾病诊断、个性化治疗中涉及核酸序列分子诊断而开发的试剂盒。核酸序列对象包括SNP,突变、插入、缺失,CpG甲基化,基因拷贝数等定性、定量分析;以及单倍型、菌种、病毒等。

戊型肝炎系列诊断试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
一、项目特点 戊肝诊断试剂质量提高的关键点在于病毒优势抗原决定簇的发现、基因工程再现、应用于试剂研制以及试剂性能的优化。本项目主要创新发明点在于:发现戊肝病毒优势构象性抗原决定簇,阐明其关键结构特征;发明能再现该抗原决定簇的基因工程抗原及其规模制备方法;研制出适用于诊断急性感染、既往感染和动物感染的三种试剂盒,实现产业化和国际化。项目已获得:3项7个授权发明专利;1项新药证书、1项新医疗器械注册证书、2项欧盟CE 证书、1项国家重点新产品证书; 获得2项欧盟CE认证。 二、技术成熟度 已经实现产业转化和市场化,并已拓展到欧洲市场。 三、应用范围 未知肝炎疾病的诊断。 四、投产条件和预期经济效益 满足免疫诊断试剂产品的生产,预计年销售额可达2000万元 五、合作方式 国内市场已有合作企业占据60以上的市场份额,现需要拓展欧盟以外的国际市场,有该资格的企业可以商谈合作方式。

登革病毒抗原系列检测试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
用途:登革热的早期检测产品类型:诊断试剂盒产登革病毒共有4个血清型,可引起典型登革热、登革出血热及登革休克综合征,广泛流行于热带和亚热带地区,据WHO估计,目前全球每年约有5千万到1亿人感染登革病毒,其中25万至50万人发展为登革出血热,每年约有24000人死亡,主要是儿童。国内外尚未有商品化的登革病毒抗原检测试剂盒。主要原因是很难获得特异性单克隆抗体,而我们的技术优势是具有成熟的单克隆抗体制备和特异性筛选以及诊断性抗体的质控标准化体系评价的技术平台,通过对“SARS冠状病毒抗原检测试剂盒”研发,在抗原免疫诊断试剂盒研发方面积累了丰富的经验。由于有较成熟的生产工艺,易规模化大量生产,故生产成本低;按目前国内外抗原诊断试剂盒行情,产品进入市场后零售价保守估计为1000元/盒(96份/盒),每盒应有900元的利润,销售超过10000万盒,成本可降到1%。如平均每年即可售出100000盒,销售额为:1000元/盒×100000=10000万元,扣除其他成本,利润在7000万元以上。产品的研制获得国家863计划的支持。开发进展阶段:已获得多株特异性的单克隆抗体,正在筛选抗体和检测抗体最佳组合。预计完成时间:企业参与的情况下,2007年年底送中国生物制品检定所进行三批成品检定,然后进行临床样品检定完成所规定的样品数,可上报申报资料,预计1年内可拿到批文预计研究经费:500万元合作方式:一次性转让、合作开发、技术入股等。

疟疾免疫层析检测试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
诊断试剂盒,用于疟疾筛查和诊断 。本项目以重组的恶性疟诊断靶抗原HRP-II为靶,制备相应单克隆抗体,经筛选配对,结合Dipstick-免疫胶体金技术建立了恶性疟的快速免疫层析检测方法,有较好的敏感性和特异性。新型诊断试剂盒大大提高恶性疟的诊断水平,有利于恶性疟的早期发现、早期治疗及疫情监控,为疟区/战场恶性疟的快速诊断和流行病学调查提供了新的有效手段。这种检测方法无需特殊设备,容易判读,产品成本比进口产品低,适合我国和发展中国家国情,易于在基层普及。产品在不影响检测效果的情况下,在材料及抗原、抗体制备方面降低了成本(不超过1元/条),市场价格较低(以3~5元计),不到进口同类产品的一半。因此在国内和国际市场上将有很强的的竞争力,尤其在非洲及东南亚的泰国、老挝、缅甸、越南、菲律宾、柬埔寨等国,目前疟疾仍很猖獗,如果能抢占这些市场,市场潜在价值可观。目前已获国家发明专利,诊断试纸条已试销至东南亚、非洲等一些疟疾流行猖獗的国家,获得较好的经济效益。恶性疟免疫层析诊断试剂盒在国内的报批工作正在进行中,已经对试剂盒进行了三批中试,临床试验已接近尾声,各项报批资料正在撰写中,预计年内可获得批准文号。恶性疟与间日疟同步诊断试剂盒的研制,已制备出单克隆抗体,筛选出抗原与抗体的最佳组合。研究时间1年,研究经费120万元。合作方式:一次性转让、合作开发、技术入股等

乙型肝炎病毒基因分型诊断试剂盒(PCR荧光法)
成熟度:-
技术类型:-
应用行业:制造业
技术简介
国内外学者从病毒学,流行病学和临床医学等方面对HBV基因型进行了大量研究,各基因型的地理性分布特点已基本明确,不同基因型的临床表现也得到了进一步的认识,而HBV基因型与HBV引起的临床疾病的进一步深入研究,必将对乙型肝炎患者的治疗管理提供更有指导性的价值;同时,随着对HBV基因型重要性不断的认识,它将极可能成为HBV感染日常临床诊治工作的一部分;HBV基因型也有于人们进一步理解HBV流行病学与人口迁移;也将对慢性乙型肝炎患者的治疗与管理个体化产生积极的作用。针对国内HBV基因型分布特点,确定研制开发乙型肝炎病毒B型、C型以及B/C混合型检测试剂盒。该产品基于TaqMan探针荧光PCR原理,设计一对涵盖八个HBV基因型的共有引物和B、C基因型特异性荧光探针,从而开发一个在多通道荧光PCR仪器上使用可检测乙型肝炎病毒B、C基因型及B/C混合型检测试剂盒;试剂盒使用dUTP和UNG酶,有效防止扩增产物的污染;该产品的优点在于一个反应中同时检测B型、C型以及B/C混合型,同时,根据检测结果可分析B/C混合型中B型、C型比例关系;操作简便。该产品符合核酸扩增类检测试剂的基本生产工艺,依据工艺配方配制成半成品,抽样检验合格后的半成品组合成成品,抽样完成检验。产品改进方面,首先增强试剂盒仪器兼容性;其次针对非B非C型HBV的型别鉴定,为进入海外市场作准备;再次建立外部标准曲线,提升产品的线性指标,实现分型同时对HBV进行定量。

循环miRNA生物标志物的鉴定及诊断试剂盒研发
成熟度:-
技术类型:-
应用行业:科学研究和技术服务业
技术简介
生物医药领域的原创性发现和基础研究的突破,是产生并发明核心技术与方法的重要基础。该项目“循环miRNA生物标志物的鉴定及诊断试剂盒研发”系列核心技术的发明就是在“循环miRNA”发现基础上,在“循环miRNA是疾病的分子标志物”原创性理论指导下产生的。在经典生物化学概念中,由于血淸/血浆等细胞外环境下存在高浓度RNA水解酶,RNA不能完整、稳定地存在,只存在无生物学功能和意义的核酸降解碎片。2007年,该项目组在国际上率先发现:动物和人的血清/血浆等体液中稳定存在完整的、高浓度、种类众多的miRNA,并能对抗酸、反复冻融及酶的降解。循环miRNA具有不同于经典RNA的理化特性,这个发现突破了生物化学的传统观念,开辟了“细胞外RNA”研宄和应用新领域。在分析2000余种循环miRNA在不同疾病中的表达谱后,发现疾病状态下循环miRNA存在特异性变化模式,提出“循环miRNA是疾病分子标志物”的理论观点。基于这个发现和相关理论研究,该项目组于2007年11月申请了国际上首个“循环miRNA”发明专利和PCT,率先提出了“血清/血浆miRNA”的概念,并发明和建立了一套涵盖循环RNA提取、高通量分析、精准定量的实验方法和技术手段。围绕“循环miRNA生物标志物的鉴定”,38项国际国内发明专利已授权。在10项代表性发明专利中,发明了低浓度循环miRNA深度测序及芯片检测的筛选方法;建立了特定循环miRNA组合的检测应用标准与归一化方法:鉴定并发明了胰腺癌、肝癌、食管癌、胃癌及肺癌的特异性循环miRNA表达谱及其作为生物标志物的筛选、测定、判定标准和方法,在上述发明核心技术的基础上,自主研发了国际上首个将循环miRNA作为生物标志物应用于临床的产品——胰腺癌血淸miRNA诊断试剂盒,准确率达88.05% (I、II期准确率为87.6%),并于2015年11月获得国家三类医疗器械注册证,为胰腺癌的早期诊断提供了更准确的新手段,获得临床单位普遍认可,2018年签约合同总金额共计4290万美。作为该项目的成果总结,与上述发明专利相关的10篇论文共被CA-Cancer J Clin、Nat Rev Drug Discov等期刊他引4216次;最高单篇他引2684次;7篇论文入选ESI Top 1%高被引论文:国际著名的MIT“Technology Review”为“血清/血浆miRNA是疾病标志物”的发现及发明的检测方法写了专题评论;国内外也有大量跟进研究,迄今关于“循环miRNA”及其应用的SCI综述已有1178篇,国内申请循环miRNA相关专利537项。这些数据均显示出国际国内学术界、产业界对该项目科学发现和理论及由此产生的发明技术的认可。项目完成人多次受邀撰写循环miRNA相关专题评述、研究前瞻及书籍,并多次被国际会议邀请作大会报告:同时通过科技部“973”项目“循环miRNA生物学功能及临床应用”等项目的立项和执行,带动了国际国内“循环miRNA”领域的相关研究。

耐多药结核病噬菌体快速诊断试剂盒研制
成熟度:-
技术类型:-
应用行业:卫生和社会工作
技术简介
该项目研制了耐多药结核病的噬菌体快速诊断试剂盒,可同时检测结核分枝杆菌临床分离株和/或肺结核患者痰标本对5种抗结核药物(利福平、链霉素、异烟肼、乙胺丁醇、吡嗪酰胺)的耐药性。全程只需3天时间,比常规方法缩短4~8周,与传统方法的诊断符合率达85%以上。该试剂盒可用于各级医院及卫生防疫单位。国内外无同类产品,市场需求巨大,可获得显著经济效益。

国际三代人类免疫缺陷病毒(HIV-1/2)抗体酶标法诊断试剂盒
成熟度:-
技术类型:-
应用行业:制造业
技术简介
被称为“世纪瘟疫”的艾滋病致死率极高,由于没有有效疫苗和药物防治而将成为较长时间内危害人类健康最为严重的传染性疾病。该项目旨在建立更加灵敏的双抗原夹心法HIV抗体检测试剂盒,缩短无知窗口期,对防止艾滋病的传播意义重大,属生物医学领域高新技术项目。该项目是河南省科技厅支持的重大科技攻关计划项目,它全面采用了分子生物学、细胞工程、基因工程等最新科技成果,突破了HIV抗原表达、标记的瓶颈问题,各项技术指标完全符合国家标准,与美国FDA批准的试剂同处国际先进水平,并具有以下特点:①包被采用独有的特异性基因工程嵌合抗原,同时捕获艾滋病病毒Ⅰ型和Ⅱ型抗体;②首次在大肠杆菌中表达出可溶性HIV重组抗原,用于标记;③采用独特的果胶酶表达系统,可大量表达抗原;④将原核表达的重组抗原和合成肽抗原与辣根过氧化物酶耦联成功;⑤采用特异的双抗原夹心法,可检测血清、血浆、唾液、脑脊液和血液制品等样品,应用范围广泛;⑥可检测IgG、IgM、IgA、IgD、IgE等多种抗体,提高了检出率;⑦缩短了无知窗口期,有利于早期发现HIV感染者;⑧采用独特稳定技术,实现效期内试剂质量始终稳定如一;⑨阳性对照无害化,避免了对人员和环境的潜在危害。该项目自研制成功以来,批批产品均通过了中国药品生物制品检定所的质量检定,并在卫生部艾滋病预防与控制中心、中国药品生物制品检定所、新疆维吾尔自治区防疫站等五家单位进行了临床考核和试用。与国际先进水平的产品平行对比,阳性符合率99.6%,阴性符合率99.8%,获得了考核单位的一致好评和充分肯定。该项目已通过国家药品监督管理局的新药审评,于2001年7月获国家二类新药证书和新药生产批文,国家行政保护8年。预计未来十年内仍不会有有效的艾滋病治疗药物和疫苗,在艾滋病加速蔓延之时,市场亟待新型检测试剂。该成果形成的产品设计先进、性能优越,投入市场后,将以显著优势替代原有二代产品,预计三年内可创产值15000万元,其间接经济效益和社会效益在140亿元/年以上,将为保障人民健康,保护改革开放成果和改善投资环境发挥巨大作用。

化学发光免疫诊断试剂盒
成熟度:-
技术类型:-
应用行业:制造业
技术简介
该研究突破了文献报道,改进了传统的持续发光型化学发光免疫分析技术,建立了稳定的化学发光免疫分析技术平台,使化学发光强度十分稳定,测定结果十分重复,解决了传统的持续发光型化学发光免疫分析难以在临床上应用和推广的技术难题,为其在临床上应用奠定了基础,填补了该领域的空白。该项目为我国提供了先进的临床免疫分析技术,促进了我国化学发光免疫分析技术的发展,具有先进性、创新性,在持续发光型化学发光免疫分析领域处于国际领先地位。

人丙型肝炎诊断试剂盒及疫苗
成熟度:-
技术类型:-
应用行业:科学研究和技术服务业
技术简介
人丙型肝炎是世界病毒性肝炎,其病症晚期可导致人体肝硬化和肝癌。目前目际上和国内已有诊断试剂生产。国内诊断试剂的生产主要是依赖进口丙肝病毒抗原,该校采用遗传工程技术已成功地表达和提纯了丙肝病毒的全长的囊膜抗原和全长的核心抗原,并利用这些抗原为材料已制成了诊断试剂盒。经卫生部药检所检测和临床试用其检出试剂盒。经卫生部药检所检测和临床试用其检出灵敏度稳定在98%,现正在申报批文。目前国际上尚无丙肝疫苗生产,但许多国家正在积极研制,该校利用丙肝病毒工程蛋白质已在试验动物体内诱导生产高滴度抗体,下步主要做动物保护性试验和临床试验,希望尽快研制成功丙肝疫苗造福于人类。丙肝诊断试剂主要用于血库、血制品、临床等方面。该试剂盒投产产值可逾亿元,中国有12亿人口,每年约有2000万新生婴儿出生,丙肝疫苗研制成功并投产,年产值可达数亿元。
找到74项技术成果数据。
找技术 >
两核苷酸合成焦测序仪及其核酸体外诊断试剂盒
成熟度:通过中试
技术类型:-
应用行业:制造业
技术简介
两核苷酸合成焦测序仪依据于自主知识产权的两核苷酸合成测序原理(Analytica Chimica Acta, 2014,852,274-283),不仅可以替代现有进口焦测序仪的应用领域、并满足解决直接检测PCR 产物的单倍型等分子关联分析等需求、为“精准医疗”检测核酸标志物提供临床硬件支撑。 核酸体外诊断试剂盒依据两核苷酸合成测序具有更长测序长度、更低检测限等特点(Analytical and Bioanalytical Chemistry, 408(12),3113-3123),发展针对疾病诊断、个性化治疗中涉及核酸序列分子诊断而开发的试剂盒。核酸序列对象包括SNP,突变、插入、缺失,CpG甲基化,基因拷贝数等定性、定量分析;以及单倍型、菌种、病毒等。

戊型肝炎系列诊断试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
一、项目特点 戊肝诊断试剂质量提高的关键点在于病毒优势抗原决定簇的发现、基因工程再现、应用于试剂研制以及试剂性能的优化。本项目主要创新发明点在于:发现戊肝病毒优势构象性抗原决定簇,阐明其关键结构特征;发明能再现该抗原决定簇的基因工程抗原及其规模制备方法;研制出适用于诊断急性感染、既往感染和动物感染的三种试剂盒,实现产业化和国际化。项目已获得:3项7个授权发明专利;1项新药证书、1项新医疗器械注册证书、2项欧盟CE 证书、1项国家重点新产品证书; 获得2项欧盟CE认证。 二、技术成熟度 已经实现产业转化和市场化,并已拓展到欧洲市场。 三、应用范围 未知肝炎疾病的诊断。 四、投产条件和预期经济效益 满足免疫诊断试剂产品的生产,预计年销售额可达2000万元 五、合作方式 国内市场已有合作企业占据60以上的市场份额,现需要拓展欧盟以外的国际市场,有该资格的企业可以商谈合作方式。

登革病毒抗原系列检测试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
用途:登革热的早期检测产品类型:诊断试剂盒产登革病毒共有4个血清型,可引起典型登革热、登革出血热及登革休克综合征,广泛流行于热带和亚热带地区,据WHO估计,目前全球每年约有5千万到1亿人感染登革病毒,其中25万至50万人发展为登革出血热,每年约有24000人死亡,主要是儿童。国内外尚未有商品化的登革病毒抗原检测试剂盒。主要原因是很难获得特异性单克隆抗体,而我们的技术优势是具有成熟的单克隆抗体制备和特异性筛选以及诊断性抗体的质控标准化体系评价的技术平台,通过对“SARS冠状病毒抗原检测试剂盒”研发,在抗原免疫诊断试剂盒研发方面积累了丰富的经验。由于有较成熟的生产工艺,易规模化大量生产,故生产成本低;按目前国内外抗原诊断试剂盒行情,产品进入市场后零售价保守估计为1000元/盒(96份/盒),每盒应有900元的利润,销售超过10000万盒,成本可降到1%。如平均每年即可售出100000盒,销售额为:1000元/盒×100000=10000万元,扣除其他成本,利润在7000万元以上。产品的研制获得国家863计划的支持。开发进展阶段:已获得多株特异性的单克隆抗体,正在筛选抗体和检测抗体最佳组合。预计完成时间:企业参与的情况下,2007年年底送中国生物制品检定所进行三批成品检定,然后进行临床样品检定完成所规定的样品数,可上报申报资料,预计1年内可拿到批文预计研究经费:500万元合作方式:一次性转让、合作开发、技术入股等。

疟疾免疫层析检测试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
诊断试剂盒,用于疟疾筛查和诊断 。本项目以重组的恶性疟诊断靶抗原HRP-II为靶,制备相应单克隆抗体,经筛选配对,结合Dipstick-免疫胶体金技术建立了恶性疟的快速免疫层析检测方法,有较好的敏感性和特异性。新型诊断试剂盒大大提高恶性疟的诊断水平,有利于恶性疟的早期发现、早期治疗及疫情监控,为疟区/战场恶性疟的快速诊断和流行病学调查提供了新的有效手段。这种检测方法无需特殊设备,容易判读,产品成本比进口产品低,适合我国和发展中国家国情,易于在基层普及。产品在不影响检测效果的情况下,在材料及抗原、抗体制备方面降低了成本(不超过1元/条),市场价格较低(以3~5元计),不到进口同类产品的一半。因此在国内和国际市场上将有很强的的竞争力,尤其在非洲及东南亚的泰国、老挝、缅甸、越南、菲律宾、柬埔寨等国,目前疟疾仍很猖獗,如果能抢占这些市场,市场潜在价值可观。目前已获国家发明专利,诊断试纸条已试销至东南亚、非洲等一些疟疾流行猖獗的国家,获得较好的经济效益。恶性疟免疫层析诊断试剂盒在国内的报批工作正在进行中,已经对试剂盒进行了三批中试,临床试验已接近尾声,各项报批资料正在撰写中,预计年内可获得批准文号。恶性疟与间日疟同步诊断试剂盒的研制,已制备出单克隆抗体,筛选出抗原与抗体的最佳组合。研究时间1年,研究经费120万元。合作方式:一次性转让、合作开发、技术入股等

乙型肝炎病毒基因分型诊断试剂盒(PCR荧光法)
成熟度:-
技术类型:-
应用行业:制造业
技术简介
国内外学者从病毒学,流行病学和临床医学等方面对HBV基因型进行了大量研究,各基因型的地理性分布特点已基本明确,不同基因型的临床表现也得到了进一步的认识,而HBV基因型与HBV引起的临床疾病的进一步深入研究,必将对乙型肝炎患者的治疗管理提供更有指导性的价值;同时,随着对HBV基因型重要性不断的认识,它将极可能成为HBV感染日常临床诊治工作的一部分;HBV基因型也有于人们进一步理解HBV流行病学与人口迁移;也将对慢性乙型肝炎患者的治疗与管理个体化产生积极的作用。针对国内HBV基因型分布特点,确定研制开发乙型肝炎病毒B型、C型以及B/C混合型检测试剂盒。该产品基于TaqMan探针荧光PCR原理,设计一对涵盖八个HBV基因型的共有引物和B、C基因型特异性荧光探针,从而开发一个在多通道荧光PCR仪器上使用可检测乙型肝炎病毒B、C基因型及B/C混合型检测试剂盒;试剂盒使用dUTP和UNG酶,有效防止扩增产物的污染;该产品的优点在于一个反应中同时检测B型、C型以及B/C混合型,同时,根据检测结果可分析B/C混合型中B型、C型比例关系;操作简便。该产品符合核酸扩增类检测试剂的基本生产工艺,依据工艺配方配制成半成品,抽样检验合格后的半成品组合成成品,抽样完成检验。产品改进方面,首先增强试剂盒仪器兼容性;其次针对非B非C型HBV的型别鉴定,为进入海外市场作准备;再次建立外部标准曲线,提升产品的线性指标,实现分型同时对HBV进行定量。

循环miRNA生物标志物的鉴定及诊断试剂盒研发
成熟度:-
技术类型:-
应用行业:科学研究和技术服务业
技术简介
生物医药领域的原创性发现和基础研究的突破,是产生并发明核心技术与方法的重要基础。该项目“循环miRNA生物标志物的鉴定及诊断试剂盒研发”系列核心技术的发明就是在“循环miRNA”发现基础上,在“循环miRNA是疾病的分子标志物”原创性理论指导下产生的。在经典生物化学概念中,由于血淸/血浆等细胞外环境下存在高浓度RNA水解酶,RNA不能完整、稳定地存在,只存在无生物学功能和意义的核酸降解碎片。2007年,该项目组在国际上率先发现:动物和人的血清/血浆等体液中稳定存在完整的、高浓度、种类众多的miRNA,并能对抗酸、反复冻融及酶的降解。循环miRNA具有不同于经典RNA的理化特性,这个发现突破了生物化学的传统观念,开辟了“细胞外RNA”研宄和应用新领域。在分析2000余种循环miRNA在不同疾病中的表达谱后,发现疾病状态下循环miRNA存在特异性变化模式,提出“循环miRNA是疾病分子标志物”的理论观点。基于这个发现和相关理论研究,该项目组于2007年11月申请了国际上首个“循环miRNA”发明专利和PCT,率先提出了“血清/血浆miRNA”的概念,并发明和建立了一套涵盖循环RNA提取、高通量分析、精准定量的实验方法和技术手段。围绕“循环miRNA生物标志物的鉴定”,38项国际国内发明专利已授权。在10项代表性发明专利中,发明了低浓度循环miRNA深度测序及芯片检测的筛选方法;建立了特定循环miRNA组合的检测应用标准与归一化方法:鉴定并发明了胰腺癌、肝癌、食管癌、胃癌及肺癌的特异性循环miRNA表达谱及其作为生物标志物的筛选、测定、判定标准和方法,在上述发明核心技术的基础上,自主研发了国际上首个将循环miRNA作为生物标志物应用于临床的产品——胰腺癌血淸miRNA诊断试剂盒,准确率达88.05% (I、II期准确率为87.6%),并于2015年11月获得国家三类医疗器械注册证,为胰腺癌的早期诊断提供了更准确的新手段,获得临床单位普遍认可,2018年签约合同总金额共计4290万美。作为该项目的成果总结,与上述发明专利相关的10篇论文共被CA-Cancer J Clin、Nat Rev Drug Discov等期刊他引4216次;最高单篇他引2684次;7篇论文入选ESI Top 1%高被引论文:国际著名的MIT“Technology Review”为“血清/血浆miRNA是疾病标志物”的发现及发明的检测方法写了专题评论;国内外也有大量跟进研究,迄今关于“循环miRNA”及其应用的SCI综述已有1178篇,国内申请循环miRNA相关专利537项。这些数据均显示出国际国内学术界、产业界对该项目科学发现和理论及由此产生的发明技术的认可。项目完成人多次受邀撰写循环miRNA相关专题评述、研究前瞻及书籍,并多次被国际会议邀请作大会报告:同时通过科技部“973”项目“循环miRNA生物学功能及临床应用”等项目的立项和执行,带动了国际国内“循环miRNA”领域的相关研究。

耐多药结核病噬菌体快速诊断试剂盒研制
成熟度:-
技术类型:-
应用行业:卫生和社会工作
技术简介
该项目研制了耐多药结核病的噬菌体快速诊断试剂盒,可同时检测结核分枝杆菌临床分离株和/或肺结核患者痰标本对5种抗结核药物(利福平、链霉素、异烟肼、乙胺丁醇、吡嗪酰胺)的耐药性。全程只需3天时间,比常规方法缩短4~8周,与传统方法的诊断符合率达85%以上。该试剂盒可用于各级医院及卫生防疫单位。国内外无同类产品,市场需求巨大,可获得显著经济效益。

国际三代人类免疫缺陷病毒(HIV-1/2)抗体酶标法诊断试剂盒
成熟度:-
技术类型:-
应用行业:制造业
技术简介
被称为“世纪瘟疫”的艾滋病致死率极高,由于没有有效疫苗和药物防治而将成为较长时间内危害人类健康最为严重的传染性疾病。该项目旨在建立更加灵敏的双抗原夹心法HIV抗体检测试剂盒,缩短无知窗口期,对防止艾滋病的传播意义重大,属生物医学领域高新技术项目。该项目是河南省科技厅支持的重大科技攻关计划项目,它全面采用了分子生物学、细胞工程、基因工程等最新科技成果,突破了HIV抗原表达、标记的瓶颈问题,各项技术指标完全符合国家标准,与美国FDA批准的试剂同处国际先进水平,并具有以下特点:①包被采用独有的特异性基因工程嵌合抗原,同时捕获艾滋病病毒Ⅰ型和Ⅱ型抗体;②首次在大肠杆菌中表达出可溶性HIV重组抗原,用于标记;③采用独特的果胶酶表达系统,可大量表达抗原;④将原核表达的重组抗原和合成肽抗原与辣根过氧化物酶耦联成功;⑤采用特异的双抗原夹心法,可检测血清、血浆、唾液、脑脊液和血液制品等样品,应用范围广泛;⑥可检测IgG、IgM、IgA、IgD、IgE等多种抗体,提高了检出率;⑦缩短了无知窗口期,有利于早期发现HIV感染者;⑧采用独特稳定技术,实现效期内试剂质量始终稳定如一;⑨阳性对照无害化,避免了对人员和环境的潜在危害。该项目自研制成功以来,批批产品均通过了中国药品生物制品检定所的质量检定,并在卫生部艾滋病预防与控制中心、中国药品生物制品检定所、新疆维吾尔自治区防疫站等五家单位进行了临床考核和试用。与国际先进水平的产品平行对比,阳性符合率99.6%,阴性符合率99.8%,获得了考核单位的一致好评和充分肯定。该项目已通过国家药品监督管理局的新药审评,于2001年7月获国家二类新药证书和新药生产批文,国家行政保护8年。预计未来十年内仍不会有有效的艾滋病治疗药物和疫苗,在艾滋病加速蔓延之时,市场亟待新型检测试剂。该成果形成的产品设计先进、性能优越,投入市场后,将以显著优势替代原有二代产品,预计三年内可创产值15000万元,其间接经济效益和社会效益在140亿元/年以上,将为保障人民健康,保护改革开放成果和改善投资环境发挥巨大作用。

化学发光免疫诊断试剂盒
成熟度:-
技术类型:-
应用行业:制造业
技术简介
该研究突破了文献报道,改进了传统的持续发光型化学发光免疫分析技术,建立了稳定的化学发光免疫分析技术平台,使化学发光强度十分稳定,测定结果十分重复,解决了传统的持续发光型化学发光免疫分析难以在临床上应用和推广的技术难题,为其在临床上应用奠定了基础,填补了该领域的空白。该项目为我国提供了先进的临床免疫分析技术,促进了我国化学发光免疫分析技术的发展,具有先进性、创新性,在持续发光型化学发光免疫分析领域处于国际领先地位。

人丙型肝炎诊断试剂盒及疫苗
成熟度:-
技术类型:-
应用行业:科学研究和技术服务业
技术简介
人丙型肝炎是世界病毒性肝炎,其病症晚期可导致人体肝硬化和肝癌。目前目际上和国内已有诊断试剂生产。国内诊断试剂的生产主要是依赖进口丙肝病毒抗原,该校采用遗传工程技术已成功地表达和提纯了丙肝病毒的全长的囊膜抗原和全长的核心抗原,并利用这些抗原为材料已制成了诊断试剂盒。经卫生部药检所检测和临床试用其检出试剂盒。经卫生部药检所检测和临床试用其检出灵敏度稳定在98%,现正在申报批文。目前国际上尚无丙肝疫苗生产,但许多国家正在积极研制,该校利用丙肝病毒工程蛋白质已在试验动物体内诱导生产高滴度抗体,下步主要做动物保护性试验和临床试验,希望尽快研制成功丙肝疫苗造福于人类。丙肝诊断试剂主要用于血库、血制品、临床等方面。该试剂盒投产产值可逾亿元,中国有12亿人口,每年约有2000万新生婴儿出生,丙肝疫苗研制成功并投产,年产值可达数亿元。
找到74项技术成果数据。
找技术 >
两核苷酸合成焦测序仪及其核酸体外诊断试剂盒
成熟度:通过中试
技术类型:-
应用行业:制造业
技术简介
两核苷酸合成焦测序仪依据于自主知识产权的两核苷酸合成测序原理(Analytica Chimica Acta, 2014,852,274-283),不仅可以替代现有进口焦测序仪的应用领域、并满足解决直接检测PCR 产物的单倍型等分子关联分析等需求、为“精准医疗”检测核酸标志物提供临床硬件支撑。 核酸体外诊断试剂盒依据两核苷酸合成测序具有更长测序长度、更低检测限等特点(Analytical and Bioanalytical Chemistry, 408(12),3113-3123),发展针对疾病诊断、个性化治疗中涉及核酸序列分子诊断而开发的试剂盒。核酸序列对象包括SNP,突变、插入、缺失,CpG甲基化,基因拷贝数等定性、定量分析;以及单倍型、菌种、病毒等。

戊型肝炎系列诊断试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
一、项目特点 戊肝诊断试剂质量提高的关键点在于病毒优势抗原决定簇的发现、基因工程再现、应用于试剂研制以及试剂性能的优化。本项目主要创新发明点在于:发现戊肝病毒优势构象性抗原决定簇,阐明其关键结构特征;发明能再现该抗原决定簇的基因工程抗原及其规模制备方法;研制出适用于诊断急性感染、既往感染和动物感染的三种试剂盒,实现产业化和国际化。项目已获得:3项7个授权发明专利;1项新药证书、1项新医疗器械注册证书、2项欧盟CE 证书、1项国家重点新产品证书; 获得2项欧盟CE认证。 二、技术成熟度 已经实现产业转化和市场化,并已拓展到欧洲市场。 三、应用范围 未知肝炎疾病的诊断。 四、投产条件和预期经济效益 满足免疫诊断试剂产品的生产,预计年销售额可达2000万元 五、合作方式 国内市场已有合作企业占据60以上的市场份额,现需要拓展欧盟以外的国际市场,有该资格的企业可以商谈合作方式。

登革病毒抗原系列检测试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
用途:登革热的早期检测产品类型:诊断试剂盒产登革病毒共有4个血清型,可引起典型登革热、登革出血热及登革休克综合征,广泛流行于热带和亚热带地区,据WHO估计,目前全球每年约有5千万到1亿人感染登革病毒,其中25万至50万人发展为登革出血热,每年约有24000人死亡,主要是儿童。国内外尚未有商品化的登革病毒抗原检测试剂盒。主要原因是很难获得特异性单克隆抗体,而我们的技术优势是具有成熟的单克隆抗体制备和特异性筛选以及诊断性抗体的质控标准化体系评价的技术平台,通过对“SARS冠状病毒抗原检测试剂盒”研发,在抗原免疫诊断试剂盒研发方面积累了丰富的经验。由于有较成熟的生产工艺,易规模化大量生产,故生产成本低;按目前国内外抗原诊断试剂盒行情,产品进入市场后零售价保守估计为1000元/盒(96份/盒),每盒应有900元的利润,销售超过10000万盒,成本可降到1%。如平均每年即可售出100000盒,销售额为:1000元/盒×100000=10000万元,扣除其他成本,利润在7000万元以上。产品的研制获得国家863计划的支持。开发进展阶段:已获得多株特异性的单克隆抗体,正在筛选抗体和检测抗体最佳组合。预计完成时间:企业参与的情况下,2007年年底送中国生物制品检定所进行三批成品检定,然后进行临床样品检定完成所规定的样品数,可上报申报资料,预计1年内可拿到批文预计研究经费:500万元合作方式:一次性转让、合作开发、技术入股等。

疟疾免疫层析检测试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
诊断试剂盒,用于疟疾筛查和诊断 。本项目以重组的恶性疟诊断靶抗原HRP-II为靶,制备相应单克隆抗体,经筛选配对,结合Dipstick-免疫胶体金技术建立了恶性疟的快速免疫层析检测方法,有较好的敏感性和特异性。新型诊断试剂盒大大提高恶性疟的诊断水平,有利于恶性疟的早期发现、早期治疗及疫情监控,为疟区/战场恶性疟的快速诊断和流行病学调查提供了新的有效手段。这种检测方法无需特殊设备,容易判读,产品成本比进口产品低,适合我国和发展中国家国情,易于在基层普及。产品在不影响检测效果的情况下,在材料及抗原、抗体制备方面降低了成本(不超过1元/条),市场价格较低(以3~5元计),不到进口同类产品的一半。因此在国内和国际市场上将有很强的的竞争力,尤其在非洲及东南亚的泰国、老挝、缅甸、越南、菲律宾、柬埔寨等国,目前疟疾仍很猖獗,如果能抢占这些市场,市场潜在价值可观。目前已获国家发明专利,诊断试纸条已试销至东南亚、非洲等一些疟疾流行猖獗的国家,获得较好的经济效益。恶性疟免疫层析诊断试剂盒在国内的报批工作正在进行中,已经对试剂盒进行了三批中试,临床试验已接近尾声,各项报批资料正在撰写中,预计年内可获得批准文号。恶性疟与间日疟同步诊断试剂盒的研制,已制备出单克隆抗体,筛选出抗原与抗体的最佳组合。研究时间1年,研究经费120万元。合作方式:一次性转让、合作开发、技术入股等

乙型肝炎病毒基因分型诊断试剂盒(PCR荧光法)
成熟度:-
技术类型:-
应用行业:制造业
技术简介
国内外学者从病毒学,流行病学和临床医学等方面对HBV基因型进行了大量研究,各基因型的地理性分布特点已基本明确,不同基因型的临床表现也得到了进一步的认识,而HBV基因型与HBV引起的临床疾病的进一步深入研究,必将对乙型肝炎患者的治疗管理提供更有指导性的价值;同时,随着对HBV基因型重要性不断的认识,它将极可能成为HBV感染日常临床诊治工作的一部分;HBV基因型也有于人们进一步理解HBV流行病学与人口迁移;也将对慢性乙型肝炎患者的治疗与管理个体化产生积极的作用。针对国内HBV基因型分布特点,确定研制开发乙型肝炎病毒B型、C型以及B/C混合型检测试剂盒。该产品基于TaqMan探针荧光PCR原理,设计一对涵盖八个HBV基因型的共有引物和B、C基因型特异性荧光探针,从而开发一个在多通道荧光PCR仪器上使用可检测乙型肝炎病毒B、C基因型及B/C混合型检测试剂盒;试剂盒使用dUTP和UNG酶,有效防止扩增产物的污染;该产品的优点在于一个反应中同时检测B型、C型以及B/C混合型,同时,根据检测结果可分析B/C混合型中B型、C型比例关系;操作简便。该产品符合核酸扩增类检测试剂的基本生产工艺,依据工艺配方配制成半成品,抽样检验合格后的半成品组合成成品,抽样完成检验。产品改进方面,首先增强试剂盒仪器兼容性;其次针对非B非C型HBV的型别鉴定,为进入海外市场作准备;再次建立外部标准曲线,提升产品的线性指标,实现分型同时对HBV进行定量。

循环miRNA生物标志物的鉴定及诊断试剂盒研发
成熟度:-
技术类型:-
应用行业:科学研究和技术服务业
技术简介
生物医药领域的原创性发现和基础研究的突破,是产生并发明核心技术与方法的重要基础。该项目“循环miRNA生物标志物的鉴定及诊断试剂盒研发”系列核心技术的发明就是在“循环miRNA”发现基础上,在“循环miRNA是疾病的分子标志物”原创性理论指导下产生的。在经典生物化学概念中,由于血淸/血浆等细胞外环境下存在高浓度RNA水解酶,RNA不能完整、稳定地存在,只存在无生物学功能和意义的核酸降解碎片。2007年,该项目组在国际上率先发现:动物和人的血清/血浆等体液中稳定存在完整的、高浓度、种类众多的miRNA,并能对抗酸、反复冻融及酶的降解。循环miRNA具有不同于经典RNA的理化特性,这个发现突破了生物化学的传统观念,开辟了“细胞外RNA”研宄和应用新领域。在分析2000余种循环miRNA在不同疾病中的表达谱后,发现疾病状态下循环miRNA存在特异性变化模式,提出“循环miRNA是疾病分子标志物”的理论观点。基于这个发现和相关理论研究,该项目组于2007年11月申请了国际上首个“循环miRNA”发明专利和PCT,率先提出了“血清/血浆miRNA”的概念,并发明和建立了一套涵盖循环RNA提取、高通量分析、精准定量的实验方法和技术手段。围绕“循环miRNA生物标志物的鉴定”,38项国际国内发明专利已授权。在10项代表性发明专利中,发明了低浓度循环miRNA深度测序及芯片检测的筛选方法;建立了特定循环miRNA组合的检测应用标准与归一化方法:鉴定并发明了胰腺癌、肝癌、食管癌、胃癌及肺癌的特异性循环miRNA表达谱及其作为生物标志物的筛选、测定、判定标准和方法,在上述发明核心技术的基础上,自主研发了国际上首个将循环miRNA作为生物标志物应用于临床的产品——胰腺癌血淸miRNA诊断试剂盒,准确率达88.05% (I、II期准确率为87.6%),并于2015年11月获得国家三类医疗器械注册证,为胰腺癌的早期诊断提供了更准确的新手段,获得临床单位普遍认可,2018年签约合同总金额共计4290万美。作为该项目的成果总结,与上述发明专利相关的10篇论文共被CA-Cancer J Clin、Nat Rev Drug Discov等期刊他引4216次;最高单篇他引2684次;7篇论文入选ESI Top 1%高被引论文:国际著名的MIT“Technology Review”为“血清/血浆miRNA是疾病标志物”的发现及发明的检测方法写了专题评论;国内外也有大量跟进研究,迄今关于“循环miRNA”及其应用的SCI综述已有1178篇,国内申请循环miRNA相关专利537项。这些数据均显示出国际国内学术界、产业界对该项目科学发现和理论及由此产生的发明技术的认可。项目完成人多次受邀撰写循环miRNA相关专题评述、研究前瞻及书籍,并多次被国际会议邀请作大会报告:同时通过科技部“973”项目“循环miRNA生物学功能及临床应用”等项目的立项和执行,带动了国际国内“循环miRNA”领域的相关研究。

耐多药结核病噬菌体快速诊断试剂盒研制
成熟度:-
技术类型:-
应用行业:卫生和社会工作
技术简介
该项目研制了耐多药结核病的噬菌体快速诊断试剂盒,可同时检测结核分枝杆菌临床分离株和/或肺结核患者痰标本对5种抗结核药物(利福平、链霉素、异烟肼、乙胺丁醇、吡嗪酰胺)的耐药性。全程只需3天时间,比常规方法缩短4~8周,与传统方法的诊断符合率达85%以上。该试剂盒可用于各级医院及卫生防疫单位。国内外无同类产品,市场需求巨大,可获得显著经济效益。

国际三代人类免疫缺陷病毒(HIV-1/2)抗体酶标法诊断试剂盒
成熟度:-
技术类型:-
应用行业:制造业
技术简介
被称为“世纪瘟疫”的艾滋病致死率极高,由于没有有效疫苗和药物防治而将成为较长时间内危害人类健康最为严重的传染性疾病。该项目旨在建立更加灵敏的双抗原夹心法HIV抗体检测试剂盒,缩短无知窗口期,对防止艾滋病的传播意义重大,属生物医学领域高新技术项目。该项目是河南省科技厅支持的重大科技攻关计划项目,它全面采用了分子生物学、细胞工程、基因工程等最新科技成果,突破了HIV抗原表达、标记的瓶颈问题,各项技术指标完全符合国家标准,与美国FDA批准的试剂同处国际先进水平,并具有以下特点:①包被采用独有的特异性基因工程嵌合抗原,同时捕获艾滋病病毒Ⅰ型和Ⅱ型抗体;②首次在大肠杆菌中表达出可溶性HIV重组抗原,用于标记;③采用独特的果胶酶表达系统,可大量表达抗原;④将原核表达的重组抗原和合成肽抗原与辣根过氧化物酶耦联成功;⑤采用特异的双抗原夹心法,可检测血清、血浆、唾液、脑脊液和血液制品等样品,应用范围广泛;⑥可检测IgG、IgM、IgA、IgD、IgE等多种抗体,提高了检出率;⑦缩短了无知窗口期,有利于早期发现HIV感染者;⑧采用独特稳定技术,实现效期内试剂质量始终稳定如一;⑨阳性对照无害化,避免了对人员和环境的潜在危害。该项目自研制成功以来,批批产品均通过了中国药品生物制品检定所的质量检定,并在卫生部艾滋病预防与控制中心、中国药品生物制品检定所、新疆维吾尔自治区防疫站等五家单位进行了临床考核和试用。与国际先进水平的产品平行对比,阳性符合率99.6%,阴性符合率99.8%,获得了考核单位的一致好评和充分肯定。该项目已通过国家药品监督管理局的新药审评,于2001年7月获国家二类新药证书和新药生产批文,国家行政保护8年。预计未来十年内仍不会有有效的艾滋病治疗药物和疫苗,在艾滋病加速蔓延之时,市场亟待新型检测试剂。该成果形成的产品设计先进、性能优越,投入市场后,将以显著优势替代原有二代产品,预计三年内可创产值15000万元,其间接经济效益和社会效益在140亿元/年以上,将为保障人民健康,保护改革开放成果和改善投资环境发挥巨大作用。

化学发光免疫诊断试剂盒
成熟度:-
技术类型:-
应用行业:制造业
技术简介
该研究突破了文献报道,改进了传统的持续发光型化学发光免疫分析技术,建立了稳定的化学发光免疫分析技术平台,使化学发光强度十分稳定,测定结果十分重复,解决了传统的持续发光型化学发光免疫分析难以在临床上应用和推广的技术难题,为其在临床上应用奠定了基础,填补了该领域的空白。该项目为我国提供了先进的临床免疫分析技术,促进了我国化学发光免疫分析技术的发展,具有先进性、创新性,在持续发光型化学发光免疫分析领域处于国际领先地位。

人丙型肝炎诊断试剂盒及疫苗
成熟度:-
技术类型:-
应用行业:科学研究和技术服务业
技术简介
人丙型肝炎是世界病毒性肝炎,其病症晚期可导致人体肝硬化和肝癌。目前目际上和国内已有诊断试剂生产。国内诊断试剂的生产主要是依赖进口丙肝病毒抗原,该校采用遗传工程技术已成功地表达和提纯了丙肝病毒的全长的囊膜抗原和全长的核心抗原,并利用这些抗原为材料已制成了诊断试剂盒。经卫生部药检所检测和临床试用其检出试剂盒。经卫生部药检所检测和临床试用其检出灵敏度稳定在98%,现正在申报批文。目前国际上尚无丙肝疫苗生产,但许多国家正在积极研制,该校利用丙肝病毒工程蛋白质已在试验动物体内诱导生产高滴度抗体,下步主要做动物保护性试验和临床试验,希望尽快研制成功丙肝疫苗造福于人类。丙肝诊断试剂主要用于血库、血制品、临床等方面。该试剂盒投产产值可逾亿元,中国有12亿人口,每年约有2000万新生婴儿出生,丙肝疫苗研制成功并投产,年产值可达数亿元。
找到74项技术成果数据。
找技术 >
两核苷酸合成焦测序仪及其核酸体外诊断试剂盒
成熟度:通过中试
技术类型:-
应用行业:制造业
技术简介
两核苷酸合成焦测序仪依据于自主知识产权的两核苷酸合成测序原理(Analytica Chimica Acta, 2014,852,274-283),不仅可以替代现有进口焦测序仪的应用领域、并满足解决直接检测PCR 产物的单倍型等分子关联分析等需求、为“精准医疗”检测核酸标志物提供临床硬件支撑。 核酸体外诊断试剂盒依据两核苷酸合成测序具有更长测序长度、更低检测限等特点(Analytical and Bioanalytical Chemistry, 408(12),3113-3123),发展针对疾病诊断、个性化治疗中涉及核酸序列分子诊断而开发的试剂盒。核酸序列对象包括SNP,突变、插入、缺失,CpG甲基化,基因拷贝数等定性、定量分析;以及单倍型、菌种、病毒等。

戊型肝炎系列诊断试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
一、项目特点 戊肝诊断试剂质量提高的关键点在于病毒优势抗原决定簇的发现、基因工程再现、应用于试剂研制以及试剂性能的优化。本项目主要创新发明点在于:发现戊肝病毒优势构象性抗原决定簇,阐明其关键结构特征;发明能再现该抗原决定簇的基因工程抗原及其规模制备方法;研制出适用于诊断急性感染、既往感染和动物感染的三种试剂盒,实现产业化和国际化。项目已获得:3项7个授权发明专利;1项新药证书、1项新医疗器械注册证书、2项欧盟CE 证书、1项国家重点新产品证书; 获得2项欧盟CE认证。 二、技术成熟度 已经实现产业转化和市场化,并已拓展到欧洲市场。 三、应用范围 未知肝炎疾病的诊断。 四、投产条件和预期经济效益 满足免疫诊断试剂产品的生产,预计年销售额可达2000万元 五、合作方式 国内市场已有合作企业占据60以上的市场份额,现需要拓展欧盟以外的国际市场,有该资格的企业可以商谈合作方式。

登革病毒抗原系列检测试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
用途:登革热的早期检测产品类型:诊断试剂盒产登革病毒共有4个血清型,可引起典型登革热、登革出血热及登革休克综合征,广泛流行于热带和亚热带地区,据WHO估计,目前全球每年约有5千万到1亿人感染登革病毒,其中25万至50万人发展为登革出血热,每年约有24000人死亡,主要是儿童。国内外尚未有商品化的登革病毒抗原检测试剂盒。主要原因是很难获得特异性单克隆抗体,而我们的技术优势是具有成熟的单克隆抗体制备和特异性筛选以及诊断性抗体的质控标准化体系评价的技术平台,通过对“SARS冠状病毒抗原检测试剂盒”研发,在抗原免疫诊断试剂盒研发方面积累了丰富的经验。由于有较成熟的生产工艺,易规模化大量生产,故生产成本低;按目前国内外抗原诊断试剂盒行情,产品进入市场后零售价保守估计为1000元/盒(96份/盒),每盒应有900元的利润,销售超过10000万盒,成本可降到1%。如平均每年即可售出100000盒,销售额为:1000元/盒×100000=10000万元,扣除其他成本,利润在7000万元以上。产品的研制获得国家863计划的支持。开发进展阶段:已获得多株特异性的单克隆抗体,正在筛选抗体和检测抗体最佳组合。预计完成时间:企业参与的情况下,2007年年底送中国生物制品检定所进行三批成品检定,然后进行临床样品检定完成所规定的样品数,可上报申报资料,预计1年内可拿到批文预计研究经费:500万元合作方式:一次性转让、合作开发、技术入股等。

疟疾免疫层析检测试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
诊断试剂盒,用于疟疾筛查和诊断 。本项目以重组的恶性疟诊断靶抗原HRP-II为靶,制备相应单克隆抗体,经筛选配对,结合Dipstick-免疫胶体金技术建立了恶性疟的快速免疫层析检测方法,有较好的敏感性和特异性。新型诊断试剂盒大大提高恶性疟的诊断水平,有利于恶性疟的早期发现、早期治疗及疫情监控,为疟区/战场恶性疟的快速诊断和流行病学调查提供了新的有效手段。这种检测方法无需特殊设备,容易判读,产品成本比进口产品低,适合我国和发展中国家国情,易于在基层普及。产品在不影响检测效果的情况下,在材料及抗原、抗体制备方面降低了成本(不超过1元/条),市场价格较低(以3~5元计),不到进口同类产品的一半。因此在国内和国际市场上将有很强的的竞争力,尤其在非洲及东南亚的泰国、老挝、缅甸、越南、菲律宾、柬埔寨等国,目前疟疾仍很猖獗,如果能抢占这些市场,市场潜在价值可观。目前已获国家发明专利,诊断试纸条已试销至东南亚、非洲等一些疟疾流行猖獗的国家,获得较好的经济效益。恶性疟免疫层析诊断试剂盒在国内的报批工作正在进行中,已经对试剂盒进行了三批中试,临床试验已接近尾声,各项报批资料正在撰写中,预计年内可获得批准文号。恶性疟与间日疟同步诊断试剂盒的研制,已制备出单克隆抗体,筛选出抗原与抗体的最佳组合。研究时间1年,研究经费120万元。合作方式:一次性转让、合作开发、技术入股等

乙型肝炎病毒基因分型诊断试剂盒(PCR荧光法)
成熟度:-
技术类型:-
应用行业:制造业
技术简介
国内外学者从病毒学,流行病学和临床医学等方面对HBV基因型进行了大量研究,各基因型的地理性分布特点已基本明确,不同基因型的临床表现也得到了进一步的认识,而HBV基因型与HBV引起的临床疾病的进一步深入研究,必将对乙型肝炎患者的治疗管理提供更有指导性的价值;同时,随着对HBV基因型重要性不断的认识,它将极可能成为HBV感染日常临床诊治工作的一部分;HBV基因型也有于人们进一步理解HBV流行病学与人口迁移;也将对慢性乙型肝炎患者的治疗与管理个体化产生积极的作用。针对国内HBV基因型分布特点,确定研制开发乙型肝炎病毒B型、C型以及B/C混合型检测试剂盒。该产品基于TaqMan探针荧光PCR原理,设计一对涵盖八个HBV基因型的共有引物和B、C基因型特异性荧光探针,从而开发一个在多通道荧光PCR仪器上使用可检测乙型肝炎病毒B、C基因型及B/C混合型检测试剂盒;试剂盒使用dUTP和UNG酶,有效防止扩增产物的污染;该产品的优点在于一个反应中同时检测B型、C型以及B/C混合型,同时,根据检测结果可分析B/C混合型中B型、C型比例关系;操作简便。该产品符合核酸扩增类检测试剂的基本生产工艺,依据工艺配方配制成半成品,抽样检验合格后的半成品组合成成品,抽样完成检验。产品改进方面,首先增强试剂盒仪器兼容性;其次针对非B非C型HBV的型别鉴定,为进入海外市场作准备;再次建立外部标准曲线,提升产品的线性指标,实现分型同时对HBV进行定量。

循环miRNA生物标志物的鉴定及诊断试剂盒研发
成熟度:-
技术类型:-
应用行业:科学研究和技术服务业
技术简介
生物医药领域的原创性发现和基础研究的突破,是产生并发明核心技术与方法的重要基础。该项目“循环miRNA生物标志物的鉴定及诊断试剂盒研发”系列核心技术的发明就是在“循环miRNA”发现基础上,在“循环miRNA是疾病的分子标志物”原创性理论指导下产生的。在经典生物化学概念中,由于血淸/血浆等细胞外环境下存在高浓度RNA水解酶,RNA不能完整、稳定地存在,只存在无生物学功能和意义的核酸降解碎片。2007年,该项目组在国际上率先发现:动物和人的血清/血浆等体液中稳定存在完整的、高浓度、种类众多的miRNA,并能对抗酸、反复冻融及酶的降解。循环miRNA具有不同于经典RNA的理化特性,这个发现突破了生物化学的传统观念,开辟了“细胞外RNA”研宄和应用新领域。在分析2000余种循环miRNA在不同疾病中的表达谱后,发现疾病状态下循环miRNA存在特异性变化模式,提出“循环miRNA是疾病分子标志物”的理论观点。基于这个发现和相关理论研究,该项目组于2007年11月申请了国际上首个“循环miRNA”发明专利和PCT,率先提出了“血清/血浆miRNA”的概念,并发明和建立了一套涵盖循环RNA提取、高通量分析、精准定量的实验方法和技术手段。围绕“循环miRNA生物标志物的鉴定”,38项国际国内发明专利已授权。在10项代表性发明专利中,发明了低浓度循环miRNA深度测序及芯片检测的筛选方法;建立了特定循环miRNA组合的检测应用标准与归一化方法:鉴定并发明了胰腺癌、肝癌、食管癌、胃癌及肺癌的特异性循环miRNA表达谱及其作为生物标志物的筛选、测定、判定标准和方法,在上述发明核心技术的基础上,自主研发了国际上首个将循环miRNA作为生物标志物应用于临床的产品——胰腺癌血淸miRNA诊断试剂盒,准确率达88.05% (I、II期准确率为87.6%),并于2015年11月获得国家三类医疗器械注册证,为胰腺癌的早期诊断提供了更准确的新手段,获得临床单位普遍认可,2018年签约合同总金额共计4290万美。作为该项目的成果总结,与上述发明专利相关的10篇论文共被CA-Cancer J Clin、Nat Rev Drug Discov等期刊他引4216次;最高单篇他引2684次;7篇论文入选ESI Top 1%高被引论文:国际著名的MIT“Technology Review”为“血清/血浆miRNA是疾病标志物”的发现及发明的检测方法写了专题评论;国内外也有大量跟进研究,迄今关于“循环miRNA”及其应用的SCI综述已有1178篇,国内申请循环miRNA相关专利537项。这些数据均显示出国际国内学术界、产业界对该项目科学发现和理论及由此产生的发明技术的认可。项目完成人多次受邀撰写循环miRNA相关专题评述、研究前瞻及书籍,并多次被国际会议邀请作大会报告:同时通过科技部“973”项目“循环miRNA生物学功能及临床应用”等项目的立项和执行,带动了国际国内“循环miRNA”领域的相关研究。

耐多药结核病噬菌体快速诊断试剂盒研制
成熟度:-
技术类型:-
应用行业:卫生和社会工作
技术简介
该项目研制了耐多药结核病的噬菌体快速诊断试剂盒,可同时检测结核分枝杆菌临床分离株和/或肺结核患者痰标本对5种抗结核药物(利福平、链霉素、异烟肼、乙胺丁醇、吡嗪酰胺)的耐药性。全程只需3天时间,比常规方法缩短4~8周,与传统方法的诊断符合率达85%以上。该试剂盒可用于各级医院及卫生防疫单位。国内外无同类产品,市场需求巨大,可获得显著经济效益。

国际三代人类免疫缺陷病毒(HIV-1/2)抗体酶标法诊断试剂盒
成熟度:-
技术类型:-
应用行业:制造业
技术简介
被称为“世纪瘟疫”的艾滋病致死率极高,由于没有有效疫苗和药物防治而将成为较长时间内危害人类健康最为严重的传染性疾病。该项目旨在建立更加灵敏的双抗原夹心法HIV抗体检测试剂盒,缩短无知窗口期,对防止艾滋病的传播意义重大,属生物医学领域高新技术项目。该项目是河南省科技厅支持的重大科技攻关计划项目,它全面采用了分子生物学、细胞工程、基因工程等最新科技成果,突破了HIV抗原表达、标记的瓶颈问题,各项技术指标完全符合国家标准,与美国FDA批准的试剂同处国际先进水平,并具有以下特点:①包被采用独有的特异性基因工程嵌合抗原,同时捕获艾滋病病毒Ⅰ型和Ⅱ型抗体;②首次在大肠杆菌中表达出可溶性HIV重组抗原,用于标记;③采用独特的果胶酶表达系统,可大量表达抗原;④将原核表达的重组抗原和合成肽抗原与辣根过氧化物酶耦联成功;⑤采用特异的双抗原夹心法,可检测血清、血浆、唾液、脑脊液和血液制品等样品,应用范围广泛;⑥可检测IgG、IgM、IgA、IgD、IgE等多种抗体,提高了检出率;⑦缩短了无知窗口期,有利于早期发现HIV感染者;⑧采用独特稳定技术,实现效期内试剂质量始终稳定如一;⑨阳性对照无害化,避免了对人员和环境的潜在危害。该项目自研制成功以来,批批产品均通过了中国药品生物制品检定所的质量检定,并在卫生部艾滋病预防与控制中心、中国药品生物制品检定所、新疆维吾尔自治区防疫站等五家单位进行了临床考核和试用。与国际先进水平的产品平行对比,阳性符合率99.6%,阴性符合率99.8%,获得了考核单位的一致好评和充分肯定。该项目已通过国家药品监督管理局的新药审评,于2001年7月获国家二类新药证书和新药生产批文,国家行政保护8年。预计未来十年内仍不会有有效的艾滋病治疗药物和疫苗,在艾滋病加速蔓延之时,市场亟待新型检测试剂。该成果形成的产品设计先进、性能优越,投入市场后,将以显著优势替代原有二代产品,预计三年内可创产值15000万元,其间接经济效益和社会效益在140亿元/年以上,将为保障人民健康,保护改革开放成果和改善投资环境发挥巨大作用。

化学发光免疫诊断试剂盒
成熟度:-
技术类型:-
应用行业:制造业
技术简介
该研究突破了文献报道,改进了传统的持续发光型化学发光免疫分析技术,建立了稳定的化学发光免疫分析技术平台,使化学发光强度十分稳定,测定结果十分重复,解决了传统的持续发光型化学发光免疫分析难以在临床上应用和推广的技术难题,为其在临床上应用奠定了基础,填补了该领域的空白。该项目为我国提供了先进的临床免疫分析技术,促进了我国化学发光免疫分析技术的发展,具有先进性、创新性,在持续发光型化学发光免疫分析领域处于国际领先地位。

人丙型肝炎诊断试剂盒及疫苗
成熟度:-
技术类型:-
应用行业:科学研究和技术服务业
技术简介
人丙型肝炎是世界病毒性肝炎,其病症晚期可导致人体肝硬化和肝癌。目前目际上和国内已有诊断试剂生产。国内诊断试剂的生产主要是依赖进口丙肝病毒抗原,该校采用遗传工程技术已成功地表达和提纯了丙肝病毒的全长的囊膜抗原和全长的核心抗原,并利用这些抗原为材料已制成了诊断试剂盒。经卫生部药检所检测和临床试用其检出试剂盒。经卫生部药检所检测和临床试用其检出灵敏度稳定在98%,现正在申报批文。目前国际上尚无丙肝疫苗生产,但许多国家正在积极研制,该校利用丙肝病毒工程蛋白质已在试验动物体内诱导生产高滴度抗体,下步主要做动物保护性试验和临床试验,希望尽快研制成功丙肝疫苗造福于人类。丙肝诊断试剂主要用于血库、血制品、临床等方面。该试剂盒投产产值可逾亿元,中国有12亿人口,每年约有2000万新生婴儿出生,丙肝疫苗研制成功并投产,年产值可达数亿元。
找到74项技术成果数据。
找技术 >
两核苷酸合成焦测序仪及其核酸体外诊断试剂盒
成熟度:通过中试
技术类型:-
应用行业:制造业
技术简介
两核苷酸合成焦测序仪依据于自主知识产权的两核苷酸合成测序原理(Analytica Chimica Acta, 2014,852,274-283),不仅可以替代现有进口焦测序仪的应用领域、并满足解决直接检测PCR 产物的单倍型等分子关联分析等需求、为“精准医疗”检测核酸标志物提供临床硬件支撑。 核酸体外诊断试剂盒依据两核苷酸合成测序具有更长测序长度、更低检测限等特点(Analytical and Bioanalytical Chemistry, 408(12),3113-3123),发展针对疾病诊断、个性化治疗中涉及核酸序列分子诊断而开发的试剂盒。核酸序列对象包括SNP,突变、插入、缺失,CpG甲基化,基因拷贝数等定性、定量分析;以及单倍型、菌种、病毒等。

戊型肝炎系列诊断试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
一、项目特点 戊肝诊断试剂质量提高的关键点在于病毒优势抗原决定簇的发现、基因工程再现、应用于试剂研制以及试剂性能的优化。本项目主要创新发明点在于:发现戊肝病毒优势构象性抗原决定簇,阐明其关键结构特征;发明能再现该抗原决定簇的基因工程抗原及其规模制备方法;研制出适用于诊断急性感染、既往感染和动物感染的三种试剂盒,实现产业化和国际化。项目已获得:3项7个授权发明专利;1项新药证书、1项新医疗器械注册证书、2项欧盟CE 证书、1项国家重点新产品证书; 获得2项欧盟CE认证。 二、技术成熟度 已经实现产业转化和市场化,并已拓展到欧洲市场。 三、应用范围 未知肝炎疾病的诊断。 四、投产条件和预期经济效益 满足免疫诊断试剂产品的生产,预计年销售额可达2000万元 五、合作方式 国内市场已有合作企业占据60以上的市场份额,现需要拓展欧盟以外的国际市场,有该资格的企业可以商谈合作方式。

登革病毒抗原系列检测试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
用途:登革热的早期检测产品类型:诊断试剂盒产登革病毒共有4个血清型,可引起典型登革热、登革出血热及登革休克综合征,广泛流行于热带和亚热带地区,据WHO估计,目前全球每年约有5千万到1亿人感染登革病毒,其中25万至50万人发展为登革出血热,每年约有24000人死亡,主要是儿童。国内外尚未有商品化的登革病毒抗原检测试剂盒。主要原因是很难获得特异性单克隆抗体,而我们的技术优势是具有成熟的单克隆抗体制备和特异性筛选以及诊断性抗体的质控标准化体系评价的技术平台,通过对“SARS冠状病毒抗原检测试剂盒”研发,在抗原免疫诊断试剂盒研发方面积累了丰富的经验。由于有较成熟的生产工艺,易规模化大量生产,故生产成本低;按目前国内外抗原诊断试剂盒行情,产品进入市场后零售价保守估计为1000元/盒(96份/盒),每盒应有900元的利润,销售超过10000万盒,成本可降到1%。如平均每年即可售出100000盒,销售额为:1000元/盒×100000=10000万元,扣除其他成本,利润在7000万元以上。产品的研制获得国家863计划的支持。开发进展阶段:已获得多株特异性的单克隆抗体,正在筛选抗体和检测抗体最佳组合。预计完成时间:企业参与的情况下,2007年年底送中国生物制品检定所进行三批成品检定,然后进行临床样品检定完成所规定的样品数,可上报申报资料,预计1年内可拿到批文预计研究经费:500万元合作方式:一次性转让、合作开发、技术入股等。

疟疾免疫层析检测试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
诊断试剂盒,用于疟疾筛查和诊断 。本项目以重组的恶性疟诊断靶抗原HRP-II为靶,制备相应单克隆抗体,经筛选配对,结合Dipstick-免疫胶体金技术建立了恶性疟的快速免疫层析检测方法,有较好的敏感性和特异性。新型诊断试剂盒大大提高恶性疟的诊断水平,有利于恶性疟的早期发现、早期治疗及疫情监控,为疟区/战场恶性疟的快速诊断和流行病学调查提供了新的有效手段。这种检测方法无需特殊设备,容易判读,产品成本比进口产品低,适合我国和发展中国家国情,易于在基层普及。产品在不影响检测效果的情况下,在材料及抗原、抗体制备方面降低了成本(不超过1元/条),市场价格较低(以3~5元计),不到进口同类产品的一半。因此在国内和国际市场上将有很强的的竞争力,尤其在非洲及东南亚的泰国、老挝、缅甸、越南、菲律宾、柬埔寨等国,目前疟疾仍很猖獗,如果能抢占这些市场,市场潜在价值可观。目前已获国家发明专利,诊断试纸条已试销至东南亚、非洲等一些疟疾流行猖獗的国家,获得较好的经济效益。恶性疟免疫层析诊断试剂盒在国内的报批工作正在进行中,已经对试剂盒进行了三批中试,临床试验已接近尾声,各项报批资料正在撰写中,预计年内可获得批准文号。恶性疟与间日疟同步诊断试剂盒的研制,已制备出单克隆抗体,筛选出抗原与抗体的最佳组合。研究时间1年,研究经费120万元。合作方式:一次性转让、合作开发、技术入股等

乙型肝炎病毒基因分型诊断试剂盒(PCR荧光法)
成熟度:-
技术类型:-
应用行业:制造业
技术简介
国内外学者从病毒学,流行病学和临床医学等方面对HBV基因型进行了大量研究,各基因型的地理性分布特点已基本明确,不同基因型的临床表现也得到了进一步的认识,而HBV基因型与HBV引起的临床疾病的进一步深入研究,必将对乙型肝炎患者的治疗管理提供更有指导性的价值;同时,随着对HBV基因型重要性不断的认识,它将极可能成为HBV感染日常临床诊治工作的一部分;HBV基因型也有于人们进一步理解HBV流行病学与人口迁移;也将对慢性乙型肝炎患者的治疗与管理个体化产生积极的作用。针对国内HBV基因型分布特点,确定研制开发乙型肝炎病毒B型、C型以及B/C混合型检测试剂盒。该产品基于TaqMan探针荧光PCR原理,设计一对涵盖八个HBV基因型的共有引物和B、C基因型特异性荧光探针,从而开发一个在多通道荧光PCR仪器上使用可检测乙型肝炎病毒B、C基因型及B/C混合型检测试剂盒;试剂盒使用dUTP和UNG酶,有效防止扩增产物的污染;该产品的优点在于一个反应中同时检测B型、C型以及B/C混合型,同时,根据检测结果可分析B/C混合型中B型、C型比例关系;操作简便。该产品符合核酸扩增类检测试剂的基本生产工艺,依据工艺配方配制成半成品,抽样检验合格后的半成品组合成成品,抽样完成检验。产品改进方面,首先增强试剂盒仪器兼容性;其次针对非B非C型HBV的型别鉴定,为进入海外市场作准备;再次建立外部标准曲线,提升产品的线性指标,实现分型同时对HBV进行定量。

循环miRNA生物标志物的鉴定及诊断试剂盒研发
成熟度:-
技术类型:-
应用行业:科学研究和技术服务业
技术简介
生物医药领域的原创性发现和基础研究的突破,是产生并发明核心技术与方法的重要基础。该项目“循环miRNA生物标志物的鉴定及诊断试剂盒研发”系列核心技术的发明就是在“循环miRNA”发现基础上,在“循环miRNA是疾病的分子标志物”原创性理论指导下产生的。在经典生物化学概念中,由于血淸/血浆等细胞外环境下存在高浓度RNA水解酶,RNA不能完整、稳定地存在,只存在无生物学功能和意义的核酸降解碎片。2007年,该项目组在国际上率先发现:动物和人的血清/血浆等体液中稳定存在完整的、高浓度、种类众多的miRNA,并能对抗酸、反复冻融及酶的降解。循环miRNA具有不同于经典RNA的理化特性,这个发现突破了生物化学的传统观念,开辟了“细胞外RNA”研宄和应用新领域。在分析2000余种循环miRNA在不同疾病中的表达谱后,发现疾病状态下循环miRNA存在特异性变化模式,提出“循环miRNA是疾病分子标志物”的理论观点。基于这个发现和相关理论研究,该项目组于2007年11月申请了国际上首个“循环miRNA”发明专利和PCT,率先提出了“血清/血浆miRNA”的概念,并发明和建立了一套涵盖循环RNA提取、高通量分析、精准定量的实验方法和技术手段。围绕“循环miRNA生物标志物的鉴定”,38项国际国内发明专利已授权。在10项代表性发明专利中,发明了低浓度循环miRNA深度测序及芯片检测的筛选方法;建立了特定循环miRNA组合的检测应用标准与归一化方法:鉴定并发明了胰腺癌、肝癌、食管癌、胃癌及肺癌的特异性循环miRNA表达谱及其作为生物标志物的筛选、测定、判定标准和方法,在上述发明核心技术的基础上,自主研发了国际上首个将循环miRNA作为生物标志物应用于临床的产品——胰腺癌血淸miRNA诊断试剂盒,准确率达88.05% (I、II期准确率为87.6%),并于2015年11月获得国家三类医疗器械注册证,为胰腺癌的早期诊断提供了更准确的新手段,获得临床单位普遍认可,2018年签约合同总金额共计4290万美。作为该项目的成果总结,与上述发明专利相关的10篇论文共被CA-Cancer J Clin、Nat Rev Drug Discov等期刊他引4216次;最高单篇他引2684次;7篇论文入选ESI Top 1%高被引论文:国际著名的MIT“Technology Review”为“血清/血浆miRNA是疾病标志物”的发现及发明的检测方法写了专题评论;国内外也有大量跟进研究,迄今关于“循环miRNA”及其应用的SCI综述已有1178篇,国内申请循环miRNA相关专利537项。这些数据均显示出国际国内学术界、产业界对该项目科学发现和理论及由此产生的发明技术的认可。项目完成人多次受邀撰写循环miRNA相关专题评述、研究前瞻及书籍,并多次被国际会议邀请作大会报告:同时通过科技部“973”项目“循环miRNA生物学功能及临床应用”等项目的立项和执行,带动了国际国内“循环miRNA”领域的相关研究。

耐多药结核病噬菌体快速诊断试剂盒研制
成熟度:-
技术类型:-
应用行业:卫生和社会工作
技术简介
该项目研制了耐多药结核病的噬菌体快速诊断试剂盒,可同时检测结核分枝杆菌临床分离株和/或肺结核患者痰标本对5种抗结核药物(利福平、链霉素、异烟肼、乙胺丁醇、吡嗪酰胺)的耐药性。全程只需3天时间,比常规方法缩短4~8周,与传统方法的诊断符合率达85%以上。该试剂盒可用于各级医院及卫生防疫单位。国内外无同类产品,市场需求巨大,可获得显著经济效益。

国际三代人类免疫缺陷病毒(HIV-1/2)抗体酶标法诊断试剂盒
成熟度:-
技术类型:-
应用行业:制造业
技术简介
被称为“世纪瘟疫”的艾滋病致死率极高,由于没有有效疫苗和药物防治而将成为较长时间内危害人类健康最为严重的传染性疾病。该项目旨在建立更加灵敏的双抗原夹心法HIV抗体检测试剂盒,缩短无知窗口期,对防止艾滋病的传播意义重大,属生物医学领域高新技术项目。该项目是河南省科技厅支持的重大科技攻关计划项目,它全面采用了分子生物学、细胞工程、基因工程等最新科技成果,突破了HIV抗原表达、标记的瓶颈问题,各项技术指标完全符合国家标准,与美国FDA批准的试剂同处国际先进水平,并具有以下特点:①包被采用独有的特异性基因工程嵌合抗原,同时捕获艾滋病病毒Ⅰ型和Ⅱ型抗体;②首次在大肠杆菌中表达出可溶性HIV重组抗原,用于标记;③采用独特的果胶酶表达系统,可大量表达抗原;④将原核表达的重组抗原和合成肽抗原与辣根过氧化物酶耦联成功;⑤采用特异的双抗原夹心法,可检测血清、血浆、唾液、脑脊液和血液制品等样品,应用范围广泛;⑥可检测IgG、IgM、IgA、IgD、IgE等多种抗体,提高了检出率;⑦缩短了无知窗口期,有利于早期发现HIV感染者;⑧采用独特稳定技术,实现效期内试剂质量始终稳定如一;⑨阳性对照无害化,避免了对人员和环境的潜在危害。该项目自研制成功以来,批批产品均通过了中国药品生物制品检定所的质量检定,并在卫生部艾滋病预防与控制中心、中国药品生物制品检定所、新疆维吾尔自治区防疫站等五家单位进行了临床考核和试用。与国际先进水平的产品平行对比,阳性符合率99.6%,阴性符合率99.8%,获得了考核单位的一致好评和充分肯定。该项目已通过国家药品监督管理局的新药审评,于2001年7月获国家二类新药证书和新药生产批文,国家行政保护8年。预计未来十年内仍不会有有效的艾滋病治疗药物和疫苗,在艾滋病加速蔓延之时,市场亟待新型检测试剂。该成果形成的产品设计先进、性能优越,投入市场后,将以显著优势替代原有二代产品,预计三年内可创产值15000万元,其间接经济效益和社会效益在140亿元/年以上,将为保障人民健康,保护改革开放成果和改善投资环境发挥巨大作用。

化学发光免疫诊断试剂盒
成熟度:-
技术类型:-
应用行业:制造业
技术简介
该研究突破了文献报道,改进了传统的持续发光型化学发光免疫分析技术,建立了稳定的化学发光免疫分析技术平台,使化学发光强度十分稳定,测定结果十分重复,解决了传统的持续发光型化学发光免疫分析难以在临床上应用和推广的技术难题,为其在临床上应用奠定了基础,填补了该领域的空白。该项目为我国提供了先进的临床免疫分析技术,促进了我国化学发光免疫分析技术的发展,具有先进性、创新性,在持续发光型化学发光免疫分析领域处于国际领先地位。

人丙型肝炎诊断试剂盒及疫苗
成熟度:-
技术类型:-
应用行业:科学研究和技术服务业
技术简介
人丙型肝炎是世界病毒性肝炎,其病症晚期可导致人体肝硬化和肝癌。目前目际上和国内已有诊断试剂生产。国内诊断试剂的生产主要是依赖进口丙肝病毒抗原,该校采用遗传工程技术已成功地表达和提纯了丙肝病毒的全长的囊膜抗原和全长的核心抗原,并利用这些抗原为材料已制成了诊断试剂盒。经卫生部药检所检测和临床试用其检出试剂盒。经卫生部药检所检测和临床试用其检出灵敏度稳定在98%,现正在申报批文。目前国际上尚无丙肝疫苗生产,但许多国家正在积极研制,该校利用丙肝病毒工程蛋白质已在试验动物体内诱导生产高滴度抗体,下步主要做动物保护性试验和临床试验,希望尽快研制成功丙肝疫苗造福于人类。丙肝诊断试剂主要用于血库、血制品、临床等方面。该试剂盒投产产值可逾亿元,中国有12亿人口,每年约有2000万新生婴儿出生,丙肝疫苗研制成功并投产,年产值可达数亿元。
找到74项技术成果数据。
找技术 >
两核苷酸合成焦测序仪及其核酸体外诊断试剂盒
成熟度:通过中试
技术类型:-
应用行业:制造业
技术简介
两核苷酸合成焦测序仪依据于自主知识产权的两核苷酸合成测序原理(Analytica Chimica Acta, 2014,852,274-283),不仅可以替代现有进口焦测序仪的应用领域、并满足解决直接检测PCR 产物的单倍型等分子关联分析等需求、为“精准医疗”检测核酸标志物提供临床硬件支撑。 核酸体外诊断试剂盒依据两核苷酸合成测序具有更长测序长度、更低检测限等特点(Analytical and Bioanalytical Chemistry, 408(12),3113-3123),发展针对疾病诊断、个性化治疗中涉及核酸序列分子诊断而开发的试剂盒。核酸序列对象包括SNP,突变、插入、缺失,CpG甲基化,基因拷贝数等定性、定量分析;以及单倍型、菌种、病毒等。

戊型肝炎系列诊断试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
一、项目特点 戊肝诊断试剂质量提高的关键点在于病毒优势抗原决定簇的发现、基因工程再现、应用于试剂研制以及试剂性能的优化。本项目主要创新发明点在于:发现戊肝病毒优势构象性抗原决定簇,阐明其关键结构特征;发明能再现该抗原决定簇的基因工程抗原及其规模制备方法;研制出适用于诊断急性感染、既往感染和动物感染的三种试剂盒,实现产业化和国际化。项目已获得:3项7个授权发明专利;1项新药证书、1项新医疗器械注册证书、2项欧盟CE 证书、1项国家重点新产品证书; 获得2项欧盟CE认证。 二、技术成熟度 已经实现产业转化和市场化,并已拓展到欧洲市场。 三、应用范围 未知肝炎疾病的诊断。 四、投产条件和预期经济效益 满足免疫诊断试剂产品的生产,预计年销售额可达2000万元 五、合作方式 国内市场已有合作企业占据60以上的市场份额,现需要拓展欧盟以外的国际市场,有该资格的企业可以商谈合作方式。

登革病毒抗原系列检测试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
用途:登革热的早期检测产品类型:诊断试剂盒产登革病毒共有4个血清型,可引起典型登革热、登革出血热及登革休克综合征,广泛流行于热带和亚热带地区,据WHO估计,目前全球每年约有5千万到1亿人感染登革病毒,其中25万至50万人发展为登革出血热,每年约有24000人死亡,主要是儿童。国内外尚未有商品化的登革病毒抗原检测试剂盒。主要原因是很难获得特异性单克隆抗体,而我们的技术优势是具有成熟的单克隆抗体制备和特异性筛选以及诊断性抗体的质控标准化体系评价的技术平台,通过对“SARS冠状病毒抗原检测试剂盒”研发,在抗原免疫诊断试剂盒研发方面积累了丰富的经验。由于有较成熟的生产工艺,易规模化大量生产,故生产成本低;按目前国内外抗原诊断试剂盒行情,产品进入市场后零售价保守估计为1000元/盒(96份/盒),每盒应有900元的利润,销售超过10000万盒,成本可降到1%。如平均每年即可售出100000盒,销售额为:1000元/盒×100000=10000万元,扣除其他成本,利润在7000万元以上。产品的研制获得国家863计划的支持。开发进展阶段:已获得多株特异性的单克隆抗体,正在筛选抗体和检测抗体最佳组合。预计完成时间:企业参与的情况下,2007年年底送中国生物制品检定所进行三批成品检定,然后进行临床样品检定完成所规定的样品数,可上报申报资料,预计1年内可拿到批文预计研究经费:500万元合作方式:一次性转让、合作开发、技术入股等。

疟疾免疫层析检测试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
诊断试剂盒,用于疟疾筛查和诊断 。本项目以重组的恶性疟诊断靶抗原HRP-II为靶,制备相应单克隆抗体,经筛选配对,结合Dipstick-免疫胶体金技术建立了恶性疟的快速免疫层析检测方法,有较好的敏感性和特异性。新型诊断试剂盒大大提高恶性疟的诊断水平,有利于恶性疟的早期发现、早期治疗及疫情监控,为疟区/战场恶性疟的快速诊断和流行病学调查提供了新的有效手段。这种检测方法无需特殊设备,容易判读,产品成本比进口产品低,适合我国和发展中国家国情,易于在基层普及。产品在不影响检测效果的情况下,在材料及抗原、抗体制备方面降低了成本(不超过1元/条),市场价格较低(以3~5元计),不到进口同类产品的一半。因此在国内和国际市场上将有很强的的竞争力,尤其在非洲及东南亚的泰国、老挝、缅甸、越南、菲律宾、柬埔寨等国,目前疟疾仍很猖獗,如果能抢占这些市场,市场潜在价值可观。目前已获国家发明专利,诊断试纸条已试销至东南亚、非洲等一些疟疾流行猖獗的国家,获得较好的经济效益。恶性疟免疫层析诊断试剂盒在国内的报批工作正在进行中,已经对试剂盒进行了三批中试,临床试验已接近尾声,各项报批资料正在撰写中,预计年内可获得批准文号。恶性疟与间日疟同步诊断试剂盒的研制,已制备出单克隆抗体,筛选出抗原与抗体的最佳组合。研究时间1年,研究经费120万元。合作方式:一次性转让、合作开发、技术入股等

乙型肝炎病毒基因分型诊断试剂盒(PCR荧光法)
成熟度:-
技术类型:-
应用行业:制造业
技术简介
国内外学者从病毒学,流行病学和临床医学等方面对HBV基因型进行了大量研究,各基因型的地理性分布特点已基本明确,不同基因型的临床表现也得到了进一步的认识,而HBV基因型与HBV引起的临床疾病的进一步深入研究,必将对乙型肝炎患者的治疗管理提供更有指导性的价值;同时,随着对HBV基因型重要性不断的认识,它将极可能成为HBV感染日常临床诊治工作的一部分;HBV基因型也有于人们进一步理解HBV流行病学与人口迁移;也将对慢性乙型肝炎患者的治疗与管理个体化产生积极的作用。针对国内HBV基因型分布特点,确定研制开发乙型肝炎病毒B型、C型以及B/C混合型检测试剂盒。该产品基于TaqMan探针荧光PCR原理,设计一对涵盖八个HBV基因型的共有引物和B、C基因型特异性荧光探针,从而开发一个在多通道荧光PCR仪器上使用可检测乙型肝炎病毒B、C基因型及B/C混合型检测试剂盒;试剂盒使用dUTP和UNG酶,有效防止扩增产物的污染;该产品的优点在于一个反应中同时检测B型、C型以及B/C混合型,同时,根据检测结果可分析B/C混合型中B型、C型比例关系;操作简便。该产品符合核酸扩增类检测试剂的基本生产工艺,依据工艺配方配制成半成品,抽样检验合格后的半成品组合成成品,抽样完成检验。产品改进方面,首先增强试剂盒仪器兼容性;其次针对非B非C型HBV的型别鉴定,为进入海外市场作准备;再次建立外部标准曲线,提升产品的线性指标,实现分型同时对HBV进行定量。

循环miRNA生物标志物的鉴定及诊断试剂盒研发
成熟度:-
技术类型:-
应用行业:科学研究和技术服务业
技术简介
生物医药领域的原创性发现和基础研究的突破,是产生并发明核心技术与方法的重要基础。该项目“循环miRNA生物标志物的鉴定及诊断试剂盒研发”系列核心技术的发明就是在“循环miRNA”发现基础上,在“循环miRNA是疾病的分子标志物”原创性理论指导下产生的。在经典生物化学概念中,由于血淸/血浆等细胞外环境下存在高浓度RNA水解酶,RNA不能完整、稳定地存在,只存在无生物学功能和意义的核酸降解碎片。2007年,该项目组在国际上率先发现:动物和人的血清/血浆等体液中稳定存在完整的、高浓度、种类众多的miRNA,并能对抗酸、反复冻融及酶的降解。循环miRNA具有不同于经典RNA的理化特性,这个发现突破了生物化学的传统观念,开辟了“细胞外RNA”研宄和应用新领域。在分析2000余种循环miRNA在不同疾病中的表达谱后,发现疾病状态下循环miRNA存在特异性变化模式,提出“循环miRNA是疾病分子标志物”的理论观点。基于这个发现和相关理论研究,该项目组于2007年11月申请了国际上首个“循环miRNA”发明专利和PCT,率先提出了“血清/血浆miRNA”的概念,并发明和建立了一套涵盖循环RNA提取、高通量分析、精准定量的实验方法和技术手段。围绕“循环miRNA生物标志物的鉴定”,38项国际国内发明专利已授权。在10项代表性发明专利中,发明了低浓度循环miRNA深度测序及芯片检测的筛选方法;建立了特定循环miRNA组合的检测应用标准与归一化方法:鉴定并发明了胰腺癌、肝癌、食管癌、胃癌及肺癌的特异性循环miRNA表达谱及其作为生物标志物的筛选、测定、判定标准和方法,在上述发明核心技术的基础上,自主研发了国际上首个将循环miRNA作为生物标志物应用于临床的产品——胰腺癌血淸miRNA诊断试剂盒,准确率达88.05% (I、II期准确率为87.6%),并于2015年11月获得国家三类医疗器械注册证,为胰腺癌的早期诊断提供了更准确的新手段,获得临床单位普遍认可,2018年签约合同总金额共计4290万美。作为该项目的成果总结,与上述发明专利相关的10篇论文共被CA-Cancer J Clin、Nat Rev Drug Discov等期刊他引4216次;最高单篇他引2684次;7篇论文入选ESI Top 1%高被引论文:国际著名的MIT“Technology Review”为“血清/血浆miRNA是疾病标志物”的发现及发明的检测方法写了专题评论;国内外也有大量跟进研究,迄今关于“循环miRNA”及其应用的SCI综述已有1178篇,国内申请循环miRNA相关专利537项。这些数据均显示出国际国内学术界、产业界对该项目科学发现和理论及由此产生的发明技术的认可。项目完成人多次受邀撰写循环miRNA相关专题评述、研究前瞻及书籍,并多次被国际会议邀请作大会报告:同时通过科技部“973”项目“循环miRNA生物学功能及临床应用”等项目的立项和执行,带动了国际国内“循环miRNA”领域的相关研究。

耐多药结核病噬菌体快速诊断试剂盒研制
成熟度:-
技术类型:-
应用行业:卫生和社会工作
技术简介
该项目研制了耐多药结核病的噬菌体快速诊断试剂盒,可同时检测结核分枝杆菌临床分离株和/或肺结核患者痰标本对5种抗结核药物(利福平、链霉素、异烟肼、乙胺丁醇、吡嗪酰胺)的耐药性。全程只需3天时间,比常规方法缩短4~8周,与传统方法的诊断符合率达85%以上。该试剂盒可用于各级医院及卫生防疫单位。国内外无同类产品,市场需求巨大,可获得显著经济效益。

国际三代人类免疫缺陷病毒(HIV-1/2)抗体酶标法诊断试剂盒
成熟度:-
技术类型:-
应用行业:制造业
技术简介
被称为“世纪瘟疫”的艾滋病致死率极高,由于没有有效疫苗和药物防治而将成为较长时间内危害人类健康最为严重的传染性疾病。该项目旨在建立更加灵敏的双抗原夹心法HIV抗体检测试剂盒,缩短无知窗口期,对防止艾滋病的传播意义重大,属生物医学领域高新技术项目。该项目是河南省科技厅支持的重大科技攻关计划项目,它全面采用了分子生物学、细胞工程、基因工程等最新科技成果,突破了HIV抗原表达、标记的瓶颈问题,各项技术指标完全符合国家标准,与美国FDA批准的试剂同处国际先进水平,并具有以下特点:①包被采用独有的特异性基因工程嵌合抗原,同时捕获艾滋病病毒Ⅰ型和Ⅱ型抗体;②首次在大肠杆菌中表达出可溶性HIV重组抗原,用于标记;③采用独特的果胶酶表达系统,可大量表达抗原;④将原核表达的重组抗原和合成肽抗原与辣根过氧化物酶耦联成功;⑤采用特异的双抗原夹心法,可检测血清、血浆、唾液、脑脊液和血液制品等样品,应用范围广泛;⑥可检测IgG、IgM、IgA、IgD、IgE等多种抗体,提高了检出率;⑦缩短了无知窗口期,有利于早期发现HIV感染者;⑧采用独特稳定技术,实现效期内试剂质量始终稳定如一;⑨阳性对照无害化,避免了对人员和环境的潜在危害。该项目自研制成功以来,批批产品均通过了中国药品生物制品检定所的质量检定,并在卫生部艾滋病预防与控制中心、中国药品生物制品检定所、新疆维吾尔自治区防疫站等五家单位进行了临床考核和试用。与国际先进水平的产品平行对比,阳性符合率99.6%,阴性符合率99.8%,获得了考核单位的一致好评和充分肯定。该项目已通过国家药品监督管理局的新药审评,于2001年7月获国家二类新药证书和新药生产批文,国家行政保护8年。预计未来十年内仍不会有有效的艾滋病治疗药物和疫苗,在艾滋病加速蔓延之时,市场亟待新型检测试剂。该成果形成的产品设计先进、性能优越,投入市场后,将以显著优势替代原有二代产品,预计三年内可创产值15000万元,其间接经济效益和社会效益在140亿元/年以上,将为保障人民健康,保护改革开放成果和改善投资环境发挥巨大作用。

化学发光免疫诊断试剂盒
成熟度:-
技术类型:-
应用行业:制造业
技术简介
该研究突破了文献报道,改进了传统的持续发光型化学发光免疫分析技术,建立了稳定的化学发光免疫分析技术平台,使化学发光强度十分稳定,测定结果十分重复,解决了传统的持续发光型化学发光免疫分析难以在临床上应用和推广的技术难题,为其在临床上应用奠定了基础,填补了该领域的空白。该项目为我国提供了先进的临床免疫分析技术,促进了我国化学发光免疫分析技术的发展,具有先进性、创新性,在持续发光型化学发光免疫分析领域处于国际领先地位。

人丙型肝炎诊断试剂盒及疫苗
成熟度:-
技术类型:-
应用行业:科学研究和技术服务业
技术简介
人丙型肝炎是世界病毒性肝炎,其病症晚期可导致人体肝硬化和肝癌。目前目际上和国内已有诊断试剂生产。国内诊断试剂的生产主要是依赖进口丙肝病毒抗原,该校采用遗传工程技术已成功地表达和提纯了丙肝病毒的全长的囊膜抗原和全长的核心抗原,并利用这些抗原为材料已制成了诊断试剂盒。经卫生部药检所检测和临床试用其检出试剂盒。经卫生部药检所检测和临床试用其检出灵敏度稳定在98%,现正在申报批文。目前国际上尚无丙肝疫苗生产,但许多国家正在积极研制,该校利用丙肝病毒工程蛋白质已在试验动物体内诱导生产高滴度抗体,下步主要做动物保护性试验和临床试验,希望尽快研制成功丙肝疫苗造福于人类。丙肝诊断试剂主要用于血库、血制品、临床等方面。该试剂盒投产产值可逾亿元,中国有12亿人口,每年约有2000万新生婴儿出生,丙肝疫苗研制成功并投产,年产值可达数亿元。
找到74项技术成果数据。
找技术 >
两核苷酸合成焦测序仪及其核酸体外诊断试剂盒
成熟度:通过中试
技术类型:-
应用行业:制造业
技术简介
两核苷酸合成焦测序仪依据于自主知识产权的两核苷酸合成测序原理(Analytica Chimica Acta, 2014,852,274-283),不仅可以替代现有进口焦测序仪的应用领域、并满足解决直接检测PCR 产物的单倍型等分子关联分析等需求、为“精准医疗”检测核酸标志物提供临床硬件支撑。 核酸体外诊断试剂盒依据两核苷酸合成测序具有更长测序长度、更低检测限等特点(Analytical and Bioanalytical Chemistry, 408(12),3113-3123),发展针对疾病诊断、个性化治疗中涉及核酸序列分子诊断而开发的试剂盒。核酸序列对象包括SNP,突变、插入、缺失,CpG甲基化,基因拷贝数等定性、定量分析;以及单倍型、菌种、病毒等。

戊型肝炎系列诊断试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
一、项目特点 戊肝诊断试剂质量提高的关键点在于病毒优势抗原决定簇的发现、基因工程再现、应用于试剂研制以及试剂性能的优化。本项目主要创新发明点在于:发现戊肝病毒优势构象性抗原决定簇,阐明其关键结构特征;发明能再现该抗原决定簇的基因工程抗原及其规模制备方法;研制出适用于诊断急性感染、既往感染和动物感染的三种试剂盒,实现产业化和国际化。项目已获得:3项7个授权发明专利;1项新药证书、1项新医疗器械注册证书、2项欧盟CE 证书、1项国家重点新产品证书; 获得2项欧盟CE认证。 二、技术成熟度 已经实现产业转化和市场化,并已拓展到欧洲市场。 三、应用范围 未知肝炎疾病的诊断。 四、投产条件和预期经济效益 满足免疫诊断试剂产品的生产,预计年销售额可达2000万元 五、合作方式 国内市场已有合作企业占据60以上的市场份额,现需要拓展欧盟以外的国际市场,有该资格的企业可以商谈合作方式。

登革病毒抗原系列检测试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
用途:登革热的早期检测产品类型:诊断试剂盒产登革病毒共有4个血清型,可引起典型登革热、登革出血热及登革休克综合征,广泛流行于热带和亚热带地区,据WHO估计,目前全球每年约有5千万到1亿人感染登革病毒,其中25万至50万人发展为登革出血热,每年约有24000人死亡,主要是儿童。国内外尚未有商品化的登革病毒抗原检测试剂盒。主要原因是很难获得特异性单克隆抗体,而我们的技术优势是具有成熟的单克隆抗体制备和特异性筛选以及诊断性抗体的质控标准化体系评价的技术平台,通过对“SARS冠状病毒抗原检测试剂盒”研发,在抗原免疫诊断试剂盒研发方面积累了丰富的经验。由于有较成熟的生产工艺,易规模化大量生产,故生产成本低;按目前国内外抗原诊断试剂盒行情,产品进入市场后零售价保守估计为1000元/盒(96份/盒),每盒应有900元的利润,销售超过10000万盒,成本可降到1%。如平均每年即可售出100000盒,销售额为:1000元/盒×100000=10000万元,扣除其他成本,利润在7000万元以上。产品的研制获得国家863计划的支持。开发进展阶段:已获得多株特异性的单克隆抗体,正在筛选抗体和检测抗体最佳组合。预计完成时间:企业参与的情况下,2007年年底送中国生物制品检定所进行三批成品检定,然后进行临床样品检定完成所规定的样品数,可上报申报资料,预计1年内可拿到批文预计研究经费:500万元合作方式:一次性转让、合作开发、技术入股等。

疟疾免疫层析检测试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
诊断试剂盒,用于疟疾筛查和诊断 。本项目以重组的恶性疟诊断靶抗原HRP-II为靶,制备相应单克隆抗体,经筛选配对,结合Dipstick-免疫胶体金技术建立了恶性疟的快速免疫层析检测方法,有较好的敏感性和特异性。新型诊断试剂盒大大提高恶性疟的诊断水平,有利于恶性疟的早期发现、早期治疗及疫情监控,为疟区/战场恶性疟的快速诊断和流行病学调查提供了新的有效手段。这种检测方法无需特殊设备,容易判读,产品成本比进口产品低,适合我国和发展中国家国情,易于在基层普及。产品在不影响检测效果的情况下,在材料及抗原、抗体制备方面降低了成本(不超过1元/条),市场价格较低(以3~5元计),不到进口同类产品的一半。因此在国内和国际市场上将有很强的的竞争力,尤其在非洲及东南亚的泰国、老挝、缅甸、越南、菲律宾、柬埔寨等国,目前疟疾仍很猖獗,如果能抢占这些市场,市场潜在价值可观。目前已获国家发明专利,诊断试纸条已试销至东南亚、非洲等一些疟疾流行猖獗的国家,获得较好的经济效益。恶性疟免疫层析诊断试剂盒在国内的报批工作正在进行中,已经对试剂盒进行了三批中试,临床试验已接近尾声,各项报批资料正在撰写中,预计年内可获得批准文号。恶性疟与间日疟同步诊断试剂盒的研制,已制备出单克隆抗体,筛选出抗原与抗体的最佳组合。研究时间1年,研究经费120万元。合作方式:一次性转让、合作开发、技术入股等

乙型肝炎病毒基因分型诊断试剂盒(PCR荧光法)
成熟度:-
技术类型:-
应用行业:制造业
技术简介
国内外学者从病毒学,流行病学和临床医学等方面对HBV基因型进行了大量研究,各基因型的地理性分布特点已基本明确,不同基因型的临床表现也得到了进一步的认识,而HBV基因型与HBV引起的临床疾病的进一步深入研究,必将对乙型肝炎患者的治疗管理提供更有指导性的价值;同时,随着对HBV基因型重要性不断的认识,它将极可能成为HBV感染日常临床诊治工作的一部分;HBV基因型也有于人们进一步理解HBV流行病学与人口迁移;也将对慢性乙型肝炎患者的治疗与管理个体化产生积极的作用。针对国内HBV基因型分布特点,确定研制开发乙型肝炎病毒B型、C型以及B/C混合型检测试剂盒。该产品基于TaqMan探针荧光PCR原理,设计一对涵盖八个HBV基因型的共有引物和B、C基因型特异性荧光探针,从而开发一个在多通道荧光PCR仪器上使用可检测乙型肝炎病毒B、C基因型及B/C混合型检测试剂盒;试剂盒使用dUTP和UNG酶,有效防止扩增产物的污染;该产品的优点在于一个反应中同时检测B型、C型以及B/C混合型,同时,根据检测结果可分析B/C混合型中B型、C型比例关系;操作简便。该产品符合核酸扩增类检测试剂的基本生产工艺,依据工艺配方配制成半成品,抽样检验合格后的半成品组合成成品,抽样完成检验。产品改进方面,首先增强试剂盒仪器兼容性;其次针对非B非C型HBV的型别鉴定,为进入海外市场作准备;再次建立外部标准曲线,提升产品的线性指标,实现分型同时对HBV进行定量。

循环miRNA生物标志物的鉴定及诊断试剂盒研发
成熟度:-
技术类型:-
应用行业:科学研究和技术服务业
技术简介
生物医药领域的原创性发现和基础研究的突破,是产生并发明核心技术与方法的重要基础。该项目“循环miRNA生物标志物的鉴定及诊断试剂盒研发”系列核心技术的发明就是在“循环miRNA”发现基础上,在“循环miRNA是疾病的分子标志物”原创性理论指导下产生的。在经典生物化学概念中,由于血淸/血浆等细胞外环境下存在高浓度RNA水解酶,RNA不能完整、稳定地存在,只存在无生物学功能和意义的核酸降解碎片。2007年,该项目组在国际上率先发现:动物和人的血清/血浆等体液中稳定存在完整的、高浓度、种类众多的miRNA,并能对抗酸、反复冻融及酶的降解。循环miRNA具有不同于经典RNA的理化特性,这个发现突破了生物化学的传统观念,开辟了“细胞外RNA”研宄和应用新领域。在分析2000余种循环miRNA在不同疾病中的表达谱后,发现疾病状态下循环miRNA存在特异性变化模式,提出“循环miRNA是疾病分子标志物”的理论观点。基于这个发现和相关理论研究,该项目组于2007年11月申请了国际上首个“循环miRNA”发明专利和PCT,率先提出了“血清/血浆miRNA”的概念,并发明和建立了一套涵盖循环RNA提取、高通量分析、精准定量的实验方法和技术手段。围绕“循环miRNA生物标志物的鉴定”,38项国际国内发明专利已授权。在10项代表性发明专利中,发明了低浓度循环miRNA深度测序及芯片检测的筛选方法;建立了特定循环miRNA组合的检测应用标准与归一化方法:鉴定并发明了胰腺癌、肝癌、食管癌、胃癌及肺癌的特异性循环miRNA表达谱及其作为生物标志物的筛选、测定、判定标准和方法,在上述发明核心技术的基础上,自主研发了国际上首个将循环miRNA作为生物标志物应用于临床的产品——胰腺癌血淸miRNA诊断试剂盒,准确率达88.05% (I、II期准确率为87.6%),并于2015年11月获得国家三类医疗器械注册证,为胰腺癌的早期诊断提供了更准确的新手段,获得临床单位普遍认可,2018年签约合同总金额共计4290万美。作为该项目的成果总结,与上述发明专利相关的10篇论文共被CA-Cancer J Clin、Nat Rev Drug Discov等期刊他引4216次;最高单篇他引2684次;7篇论文入选ESI Top 1%高被引论文:国际著名的MIT“Technology Review”为“血清/血浆miRNA是疾病标志物”的发现及发明的检测方法写了专题评论;国内外也有大量跟进研究,迄今关于“循环miRNA”及其应用的SCI综述已有1178篇,国内申请循环miRNA相关专利537项。这些数据均显示出国际国内学术界、产业界对该项目科学发现和理论及由此产生的发明技术的认可。项目完成人多次受邀撰写循环miRNA相关专题评述、研究前瞻及书籍,并多次被国际会议邀请作大会报告:同时通过科技部“973”项目“循环miRNA生物学功能及临床应用”等项目的立项和执行,带动了国际国内“循环miRNA”领域的相关研究。

耐多药结核病噬菌体快速诊断试剂盒研制
成熟度:-
技术类型:-
应用行业:卫生和社会工作
技术简介
该项目研制了耐多药结核病的噬菌体快速诊断试剂盒,可同时检测结核分枝杆菌临床分离株和/或肺结核患者痰标本对5种抗结核药物(利福平、链霉素、异烟肼、乙胺丁醇、吡嗪酰胺)的耐药性。全程只需3天时间,比常规方法缩短4~8周,与传统方法的诊断符合率达85%以上。该试剂盒可用于各级医院及卫生防疫单位。国内外无同类产品,市场需求巨大,可获得显著经济效益。

国际三代人类免疫缺陷病毒(HIV-1/2)抗体酶标法诊断试剂盒
成熟度:-
技术类型:-
应用行业:制造业
技术简介
被称为“世纪瘟疫”的艾滋病致死率极高,由于没有有效疫苗和药物防治而将成为较长时间内危害人类健康最为严重的传染性疾病。该项目旨在建立更加灵敏的双抗原夹心法HIV抗体检测试剂盒,缩短无知窗口期,对防止艾滋病的传播意义重大,属生物医学领域高新技术项目。该项目是河南省科技厅支持的重大科技攻关计划项目,它全面采用了分子生物学、细胞工程、基因工程等最新科技成果,突破了HIV抗原表达、标记的瓶颈问题,各项技术指标完全符合国家标准,与美国FDA批准的试剂同处国际先进水平,并具有以下特点:①包被采用独有的特异性基因工程嵌合抗原,同时捕获艾滋病病毒Ⅰ型和Ⅱ型抗体;②首次在大肠杆菌中表达出可溶性HIV重组抗原,用于标记;③采用独特的果胶酶表达系统,可大量表达抗原;④将原核表达的重组抗原和合成肽抗原与辣根过氧化物酶耦联成功;⑤采用特异的双抗原夹心法,可检测血清、血浆、唾液、脑脊液和血液制品等样品,应用范围广泛;⑥可检测IgG、IgM、IgA、IgD、IgE等多种抗体,提高了检出率;⑦缩短了无知窗口期,有利于早期发现HIV感染者;⑧采用独特稳定技术,实现效期内试剂质量始终稳定如一;⑨阳性对照无害化,避免了对人员和环境的潜在危害。该项目自研制成功以来,批批产品均通过了中国药品生物制品检定所的质量检定,并在卫生部艾滋病预防与控制中心、中国药品生物制品检定所、新疆维吾尔自治区防疫站等五家单位进行了临床考核和试用。与国际先进水平的产品平行对比,阳性符合率99.6%,阴性符合率99.8%,获得了考核单位的一致好评和充分肯定。该项目已通过国家药品监督管理局的新药审评,于2001年7月获国家二类新药证书和新药生产批文,国家行政保护8年。预计未来十年内仍不会有有效的艾滋病治疗药物和疫苗,在艾滋病加速蔓延之时,市场亟待新型检测试剂。该成果形成的产品设计先进、性能优越,投入市场后,将以显著优势替代原有二代产品,预计三年内可创产值15000万元,其间接经济效益和社会效益在140亿元/年以上,将为保障人民健康,保护改革开放成果和改善投资环境发挥巨大作用。

化学发光免疫诊断试剂盒
成熟度:-
技术类型:-
应用行业:制造业
技术简介
该研究突破了文献报道,改进了传统的持续发光型化学发光免疫分析技术,建立了稳定的化学发光免疫分析技术平台,使化学发光强度十分稳定,测定结果十分重复,解决了传统的持续发光型化学发光免疫分析难以在临床上应用和推广的技术难题,为其在临床上应用奠定了基础,填补了该领域的空白。该项目为我国提供了先进的临床免疫分析技术,促进了我国化学发光免疫分析技术的发展,具有先进性、创新性,在持续发光型化学发光免疫分析领域处于国际领先地位。

人丙型肝炎诊断试剂盒及疫苗
成熟度:-
技术类型:-
应用行业:科学研究和技术服务业
技术简介
人丙型肝炎是世界病毒性肝炎,其病症晚期可导致人体肝硬化和肝癌。目前目际上和国内已有诊断试剂生产。国内诊断试剂的生产主要是依赖进口丙肝病毒抗原,该校采用遗传工程技术已成功地表达和提纯了丙肝病毒的全长的囊膜抗原和全长的核心抗原,并利用这些抗原为材料已制成了诊断试剂盒。经卫生部药检所检测和临床试用其检出试剂盒。经卫生部药检所检测和临床试用其检出灵敏度稳定在98%,现正在申报批文。目前国际上尚无丙肝疫苗生产,但许多国家正在积极研制,该校利用丙肝病毒工程蛋白质已在试验动物体内诱导生产高滴度抗体,下步主要做动物保护性试验和临床试验,希望尽快研制成功丙肝疫苗造福于人类。丙肝诊断试剂主要用于血库、血制品、临床等方面。该试剂盒投产产值可逾亿元,中国有12亿人口,每年约有2000万新生婴儿出生,丙肝疫苗研制成功并投产,年产值可达数亿元。
找到74项技术成果数据。
找技术 >
两核苷酸合成焦测序仪及其核酸体外诊断试剂盒
成熟度:通过中试
技术类型:-
应用行业:制造业
技术简介
两核苷酸合成焦测序仪依据于自主知识产权的两核苷酸合成测序原理(Analytica Chimica Acta, 2014,852,274-283),不仅可以替代现有进口焦测序仪的应用领域、并满足解决直接检测PCR 产物的单倍型等分子关联分析等需求、为“精准医疗”检测核酸标志物提供临床硬件支撑。 核酸体外诊断试剂盒依据两核苷酸合成测序具有更长测序长度、更低检测限等特点(Analytical and Bioanalytical Chemistry, 408(12),3113-3123),发展针对疾病诊断、个性化治疗中涉及核酸序列分子诊断而开发的试剂盒。核酸序列对象包括SNP,突变、插入、缺失,CpG甲基化,基因拷贝数等定性、定量分析;以及单倍型、菌种、病毒等。

戊型肝炎系列诊断试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
一、项目特点 戊肝诊断试剂质量提高的关键点在于病毒优势抗原决定簇的发现、基因工程再现、应用于试剂研制以及试剂性能的优化。本项目主要创新发明点在于:发现戊肝病毒优势构象性抗原决定簇,阐明其关键结构特征;发明能再现该抗原决定簇的基因工程抗原及其规模制备方法;研制出适用于诊断急性感染、既往感染和动物感染的三种试剂盒,实现产业化和国际化。项目已获得:3项7个授权发明专利;1项新药证书、1项新医疗器械注册证书、2项欧盟CE 证书、1项国家重点新产品证书; 获得2项欧盟CE认证。 二、技术成熟度 已经实现产业转化和市场化,并已拓展到欧洲市场。 三、应用范围 未知肝炎疾病的诊断。 四、投产条件和预期经济效益 满足免疫诊断试剂产品的生产,预计年销售额可达2000万元 五、合作方式 国内市场已有合作企业占据60以上的市场份额,现需要拓展欧盟以外的国际市场,有该资格的企业可以商谈合作方式。

登革病毒抗原系列检测试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
用途:登革热的早期检测产品类型:诊断试剂盒产登革病毒共有4个血清型,可引起典型登革热、登革出血热及登革休克综合征,广泛流行于热带和亚热带地区,据WHO估计,目前全球每年约有5千万到1亿人感染登革病毒,其中25万至50万人发展为登革出血热,每年约有24000人死亡,主要是儿童。国内外尚未有商品化的登革病毒抗原检测试剂盒。主要原因是很难获得特异性单克隆抗体,而我们的技术优势是具有成熟的单克隆抗体制备和特异性筛选以及诊断性抗体的质控标准化体系评价的技术平台,通过对“SARS冠状病毒抗原检测试剂盒”研发,在抗原免疫诊断试剂盒研发方面积累了丰富的经验。由于有较成熟的生产工艺,易规模化大量生产,故生产成本低;按目前国内外抗原诊断试剂盒行情,产品进入市场后零售价保守估计为1000元/盒(96份/盒),每盒应有900元的利润,销售超过10000万盒,成本可降到1%。如平均每年即可售出100000盒,销售额为:1000元/盒×100000=10000万元,扣除其他成本,利润在7000万元以上。产品的研制获得国家863计划的支持。开发进展阶段:已获得多株特异性的单克隆抗体,正在筛选抗体和检测抗体最佳组合。预计完成时间:企业参与的情况下,2007年年底送中国生物制品检定所进行三批成品检定,然后进行临床样品检定完成所规定的样品数,可上报申报资料,预计1年内可拿到批文预计研究经费:500万元合作方式:一次性转让、合作开发、技术入股等。

疟疾免疫层析检测试剂盒
成熟度:正在研发
技术类型:-
应用行业:制造业
技术简介
诊断试剂盒,用于疟疾筛查和诊断 。本项目以重组的恶性疟诊断靶抗原HRP-II为靶,制备相应单克隆抗体,经筛选配对,结合Dipstick-免疫胶体金技术建立了恶性疟的快速免疫层析检测方法,有较好的敏感性和特异性。新型诊断试剂盒大大提高恶性疟的诊断水平,有利于恶性疟的早期发现、早期治疗及疫情监控,为疟区/战场恶性疟的快速诊断和流行病学调查提供了新的有效手段。这种检测方法无需特殊设备,容易判读,产品成本比进口产品低,适合我国和发展中国家国情,易于在基层普及。产品在不影响检测效果的情况下,在材料及抗原、抗体制备方面降低了成本(不超过1元/条),市场价格较低(以3~5元计),不到进口同类产品的一半。因此在国内和国际市场上将有很强的的竞争力,尤其在非洲及东南亚的泰国、老挝、缅甸、越南、菲律宾、柬埔寨等国,目前疟疾仍很猖獗,如果能抢占这些市场,市场潜在价值可观。目前已获国家发明专利,诊断试纸条已试销至东南亚、非洲等一些疟疾流行猖獗的国家,获得较好的经济效益。恶性疟免疫层析诊断试剂盒在国内的报批工作正在进行中,已经对试剂盒进行了三批中试,临床试验已接近尾声,各项报批资料正在撰写中,预计年内可获得批准文号。恶性疟与间日疟同步诊断试剂盒的研制,已制备出单克隆抗体,筛选出抗原与抗体的最佳组合。研究时间1年,研究经费120万元。合作方式:一次性转让、合作开发、技术入股等

乙型肝炎病毒基因分型诊断试剂盒(PCR荧光法)
成熟度:-
技术类型:-
应用行业:制造业
技术简介
国内外学者从病毒学,流行病学和临床医学等方面对HBV基因型进行了大量研究,各基因型的地理性分布特点已基本明确,不同基因型的临床表现也得到了进一步的认识,而HBV基因型与HBV引起的临床疾病的进一步深入研究,必将对乙型肝炎患者的治疗管理提供更有指导性的价值;同时,随着对HBV基因型重要性不断的认识,它将极可能成为HBV感染日常临床诊治工作的一部分;HBV基因型也有于人们进一步理解HBV流行病学与人口迁移;也将对慢性乙型肝炎患者的治疗与管理个体化产生积极的作用。针对国内HBV基因型分布特点,确定研制开发乙型肝炎病毒B型、C型以及B/C混合型检测试剂盒。该产品基于TaqMan探针荧光PCR原理,设计一对涵盖八个HBV基因型的共有引物和B、C基因型特异性荧光探针,从而开发一个在多通道荧光PCR仪器上使用可检测乙型肝炎病毒B、C基因型及B/C混合型检测试剂盒;试剂盒使用dUTP和UNG酶,有效防止扩增产物的污染;该产品的优点在于一个反应中同时检测B型、C型以及B/C混合型,同时,根据检测结果可分析B/C混合型中B型、C型比例关系;操作简便。该产品符合核酸扩增类检测试剂的基本生产工艺,依据工艺配方配制成半成品,抽样检验合格后的半成品组合成成品,抽样完成检验。产品改进方面,首先增强试剂盒仪器兼容性;其次针对非B非C型HBV的型别鉴定,为进入海外市场作准备;再次建立外部标准曲线,提升产品的线性指标,实现分型同时对HBV进行定量。

循环miRNA生物标志物的鉴定及诊断试剂盒研发
成熟度:-
技术类型:-
应用行业:科学研究和技术服务业
技术简介
生物医药领域的原创性发现和基础研究的突破,是产生并发明核心技术与方法的重要基础。该项目“循环miRNA生物标志物的鉴定及诊断试剂盒研发”系列核心技术的发明就是在“循环miRNA”发现基础上,在“循环miRNA是疾病的分子标志物”原创性理论指导下产生的。在经典生物化学概念中,由于血淸/血浆等细胞外环境下存在高浓度RNA水解酶,RNA不能完整、稳定地存在,只存在无生物学功能和意义的核酸降解碎片。2007年,该项目组在国际上率先发现:动物和人的血清/血浆等体液中稳定存在完整的、高浓度、种类众多的miRNA,并能对抗酸、反复冻融及酶的降解。循环miRNA具有不同于经典RNA的理化特性,这个发现突破了生物化学的传统观念,开辟了“细胞外RNA”研宄和应用新领域。在分析2000余种循环miRNA在不同疾病中的表达谱后,发现疾病状态下循环miRNA存在特异性变化模式,提出“循环miRNA是疾病分子标志物”的理论观点。基于这个发现和相关理论研究,该项目组于2007年11月申请了国际上首个“循环miRNA”发明专利和PCT,率先提出了“血清/血浆miRNA”的概念,并发明和建立了一套涵盖循环RNA提取、高通量分析、精准定量的实验方法和技术手段。围绕“循环miRNA生物标志物的鉴定”,38项国际国内发明专利已授权。在10项代表性发明专利中,发明了低浓度循环miRNA深度测序及芯片检测的筛选方法;建立了特定循环miRNA组合的检测应用标准与归一化方法:鉴定并发明了胰腺癌、肝癌、食管癌、胃癌及肺癌的特异性循环miRNA表达谱及其作为生物标志物的筛选、测定、判定标准和方法,在上述发明核心技术的基础上,自主研发了国际上首个将循环miRNA作为生物标志物应用于临床的产品——胰腺癌血淸miRNA诊断试剂盒,准确率达88.05% (I、II期准确率为87.6%),并于2015年11月获得国家三类医疗器械注册证,为胰腺癌的早期诊断提供了更准确的新手段,获得临床单位普遍认可,2018年签约合同总金额共计4290万美。作为该项目的成果总结,与上述发明专利相关的10篇论文共被CA-Cancer J Clin、Nat Rev Drug Discov等期刊他引4216次;最高单篇他引2684次;7篇论文入选ESI Top 1%高被引论文:国际著名的MIT“Technology Review”为“血清/血浆miRNA是疾病标志物”的发现及发明的检测方法写了专题评论;国内外也有大量跟进研究,迄今关于“循环miRNA”及其应用的SCI综述已有1178篇,国内申请循环miRNA相关专利537项。这些数据均显示出国际国内学术界、产业界对该项目科学发现和理论及由此产生的发明技术的认可。项目完成人多次受邀撰写循环miRNA相关专题评述、研究前瞻及书籍,并多次被国际会议邀请作大会报告:同时通过科技部“973”项目“循环miRNA生物学功能及临床应用”等项目的立项和执行,带动了国际国内“循环miRNA”领域的相关研究。

耐多药结核病噬菌体快速诊断试剂盒研制
成熟度:-
技术类型:-
应用行业:卫生和社会工作
技术简介
该项目研制了耐多药结核病的噬菌体快速诊断试剂盒,可同时检测结核分枝杆菌临床分离株和/或肺结核患者痰标本对5种抗结核药物(利福平、链霉素、异烟肼、乙胺丁醇、吡嗪酰胺)的耐药性。全程只需3天时间,比常规方法缩短4~8周,与传统方法的诊断符合率达85%以上。该试剂盒可用于各级医院及卫生防疫单位。国内外无同类产品,市场需求巨大,可获得显著经济效益。

国际三代人类免疫缺陷病毒(HIV-1/2)抗体酶标法诊断试剂盒
成熟度:-
技术类型:-
应用行业:制造业
技术简介
被称为“世纪瘟疫”的艾滋病致死率极高,由于没有有效疫苗和药物防治而将成为较长时间内危害人类健康最为严重的传染性疾病。该项目旨在建立更加灵敏的双抗原夹心法HIV抗体检测试剂盒,缩短无知窗口期,对防止艾滋病的传播意义重大,属生物医学领域高新技术项目。该项目是河南省科技厅支持的重大科技攻关计划项目,它全面采用了分子生物学、细胞工程、基因工程等最新科技成果,突破了HIV抗原表达、标记的瓶颈问题,各项技术指标完全符合国家标准,与美国FDA批准的试剂同处国际先进水平,并具有以下特点:①包被采用独有的特异性基因工程嵌合抗原,同时捕获艾滋病病毒Ⅰ型和Ⅱ型抗体;②首次在大肠杆菌中表达出可溶性HIV重组抗原,用于标记;③采用独特的果胶酶表达系统,可大量表达抗原;④将原核表达的重组抗原和合成肽抗原与辣根过氧化物酶耦联成功;⑤采用特异的双抗原夹心法,可检测血清、血浆、唾液、脑脊液和血液制品等样品,应用范围广泛;⑥可检测IgG、IgM、IgA、IgD、IgE等多种抗体,提高了检出率;⑦缩短了无知窗口期,有利于早期发现HIV感染者;⑧采用独特稳定技术,实现效期内试剂质量始终稳定如一;⑨阳性对照无害化,避免了对人员和环境的潜在危害。该项目自研制成功以来,批批产品均通过了中国药品生物制品检定所的质量检定,并在卫生部艾滋病预防与控制中心、中国药品生物制品检定所、新疆维吾尔自治区防疫站等五家单位进行了临床考核和试用。与国际先进水平的产品平行对比,阳性符合率99.6%,阴性符合率99.8%,获得了考核单位的一致好评和充分肯定。该项目已通过国家药品监督管理局的新药审评,于2001年7月获国家二类新药证书和新药生产批文,国家行政保护8年。预计未来十年内仍不会有有效的艾滋病治疗药物和疫苗,在艾滋病加速蔓延之时,市场亟待新型检测试剂。该成果形成的产品设计先进、性能优越,投入市场后,将以显著优势替代原有二代产品,预计三年内可创产值15000万元,其间接经济效益和社会效益在140亿元/年以上,将为保障人民健康,保护改革开放成果和改善投资环境发挥巨大作用。

化学发光免疫诊断试剂盒
成熟度:-
技术类型:-
应用行业:制造业
技术简介
该研究突破了文献报道,改进了传统的持续发光型化学发光免疫分析技术,建立了稳定的化学发光免疫分析技术平台,使化学发光强度十分稳定,测定结果十分重复,解决了传统的持续发光型化学发光免疫分析难以在临床上应用和推广的技术难题,为其在临床上应用奠定了基础,填补了该领域的空白。该项目为我国提供了先进的临床免疫分析技术,促进了我国化学发光免疫分析技术的发展,具有先进性、创新性,在持续发光型化学发光免疫分析领域处于国际领先地位。

人丙型肝炎诊断试剂盒及疫苗
成熟度:-
技术类型:-
应用行业:科学研究和技术服务业
技术简介
人丙型肝炎是世界病毒性肝炎,其病症晚期可导致人体肝硬化和肝癌。目前目际上和国内已有诊断试剂生产。国内诊断试剂的生产主要是依赖进口丙肝病毒抗原,该校采用遗传工程技术已成功地表达和提纯了丙肝病毒的全长的囊膜抗原和全长的核心抗原,并利用这些抗原为材料已制成了诊断试剂盒。经卫生部药检所检测和临床试用其检出试剂盒。经卫生部药检所检测和临床试用其检出灵敏度稳定在98%,现正在申报批文。目前国际上尚无丙肝疫苗生产,但许多国家正在积极研制,该校利用丙肝病毒工程蛋白质已在试验动物体内诱导生产高滴度抗体,下步主要做动物保护性试验和临床试验,希望尽快研制成功丙肝疫苗造福于人类。丙肝诊断试剂主要用于血库、血制品、临床等方面。该试剂盒投产产值可逾亿元,中国有12亿人口,每年约有2000万新生婴儿出生,丙肝疫苗研制成功并投产,年产值可达数亿元。




