靶向脂肪酸代谢(果友7麦粒)
快速增殖的肿瘤细胞通过增加外源性脂质的摄取或过度激活的合成途径表现出对脂质和胆固醇的高亲和力。许多肿瘤细胞被发现可以提高脂质和胆固醇生物合成的酶数量(BeloribiDjefaflia et al., 2016; Wegiel et al., 2018)。过多的脂质和胆固醇储存在脂滴中,其数量与肿瘤侵袭性相关(Beloribi-Djefaflia et al., 2016)。由于这些原因,脂肪酸合成(FAS)抑制剂一直是肿瘤治疗的重点关注领域,尤其是以脂肪酸合成酶 (FASN)为代表的靶点(Lu et al., 2018; Mullen and Yet, 2015)。然而,抑制癌细胞中的脂肪酸代谢也会间接影响免疫细胞的功能(图4)。
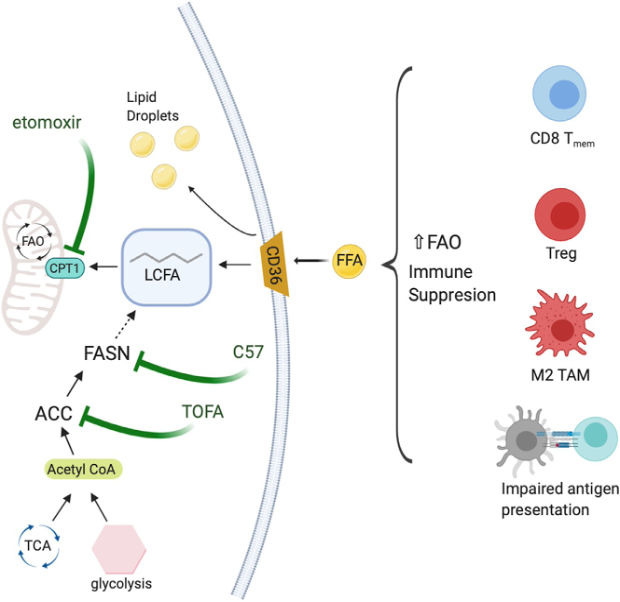
图4. 脂肪酸的操控
肿瘤微环境中脂肪酸的增加可导致免疫细胞内脂滴的积累或促进线粒体脂肪酸 β-氧化的发展。免疫抑制表型通常依赖线粒体脂肪酸 β-氧化作为产生能量的手段。已经发现,抑制CD36、脂滴积累或通过脂肪酸合成酶(FASN)合成FA(脂肪酸)的靶点可以改善依赖于线粒体脂肪酸 β-氧化的免疫抑制代谢。线粒体脂肪酸 β-氧化,线粒体脂肪酸氧化; FA,脂肪酸;FASN,脂肪酸合成酶。
脂肪酸和脂质蓄积对不同的免疫细胞亚群影响也不同,但脂质蓄积一般会导致免疫抑制作用。在骨髓细胞中,脂质在细胞内的蓄积可增强氧化代谢并促进免疫抑制功能(Le Bourgeois et al., 2018)。不饱和脂肪酸油酸使骨髓来源的骨髓细胞极化为免疫抑制性M2型肿瘤相关巨噬细胞(Wu et al., 2019)。肿瘤浸润性DC细胞(tumor-infiltrating DCs, TIDCs)的异常脂质积累损害了它们的抗原呈递(Herber et al., 2010)。在小鼠卵巢癌模型中,肿瘤浸润性DC细胞(TIDCs)从TME中摄取过多的脂质导致T细胞启动和激活变差(Jiang et al., 2018)。因此,TME中脂肪酸堆积对免疫细胞有直接影响,在小鼠肿瘤模型中可以通过靶向脂肪酸合成(FAS)或脂肪酸氧化(FAO)来有效改善脂质丰度。比如,通过乙酰辅酶A羧化酶(ACC)抑制剂TOFA抑制脂肪酸合成(FAS),使得DC细胞中的脂质至正常水平以恢复其活性,并显著提高肿瘤疫苗的效果(Herber et al., 2010)。在卵巢癌模型中,抑制脂肪酸合成酶(FASN)能够部分逆转肿瘤浸润性DC细胞的功能(Jiang et al., 2018)。另外,抑制脂肪酸氧化(FAO)可能会限制M2型巨噬细胞的免疫抑制功能(Zhang et al., 2018)。
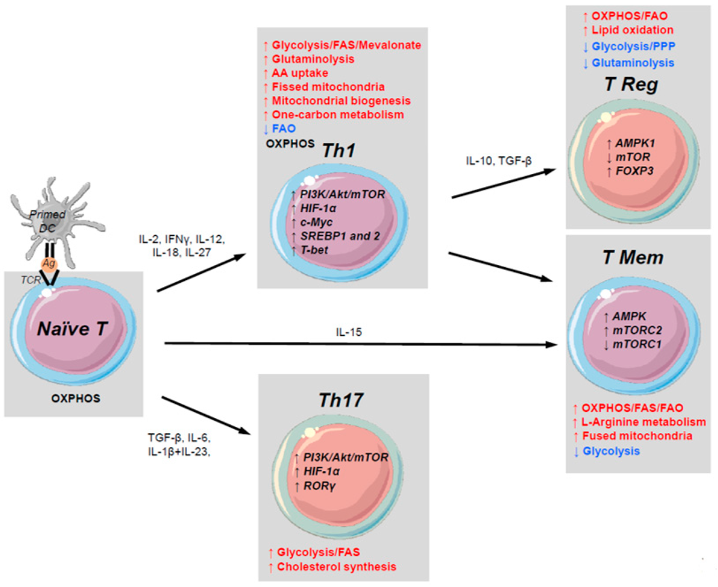
这张图总结的很全面
靶向T细胞中的脂肪酸代谢可对不同的T细胞亚群产生不同的作用。一方面,脂肪酸氧化(FAO)是CD8+记忆性T细胞形成的必要条件(O’Sullivan et al., 2014);同时其对Tregs的分化也很重要,阻断脂肪酸氧化(FAO)可避免这种免疫抑制性T细胞群的聚集Tregs(Beier et al., 2015; Michalek et al., 2011)。在小鼠黑色素瘤模型中,CD8+ TILs通过增强过氧化物酶体增殖物激活受体(PPAR-α)信号和脂肪酸分解代谢来保持其功能效应(Zhang et al., 2017),表明脂肪酸摄取可能对某些TME有利。然而,最近发现脂质转运蛋白CD36可促进肿瘤中Treg的存活和功能(Wang et al., 2020),抑制T细胞脂肪酸结合蛋白FABP5,增强对Treg的抑制(Field et al., 2020)。在原代人T细胞的脂肪酸代谢和细胞凋亡敏感性研究中,通过C75(人工合成的较稳定的化合物)或siRNA敲除抑制脂肪酸合成酶(FASN),可通过减少脂肪酸合成(FAS)配体的诱导,保护T细胞免受再刺激诱导的细胞死亡(restimulation-induced cell death ,RICD)( Voss et al., 2019)。因此,脂肪酸合成酶(FASN)抑制除了其直接对癌细胞的抗肿瘤功效,还可避免TME中的T细胞因反复受到T细胞抗原受体的刺激导致凋亡,增强T细胞的抗肿瘤作用。此外破坏脂肪酸氧化(FAO)对细胞死亡(restimulation-induced cell death, RICD)并无重要影响,这突出了不同脂肪酸代谢途径在编程免疫细胞凋亡敏感性中的特异性。然而在另一项研究中,抑制脂肪酸氧化(FAO)可减缓肿瘤生长,促进T细胞抗肿瘤作用 (Zhang et al., 2018)。复杂的脂质和胆固醇代谢为调节TME和特定的免疫细胞群提供了机会(Eichner et al., 2019)。超过血管交换能力的TME中高糖消耗可能促进AMPK活化,这可能有助于抑制性免疫细胞的持续存在,包括TAM、MDSC和Tregs (Blagih et al., 2015; Eichner et al., 2019; Michalek et al., 2011; Siska and Rathmell, 2015)。Tregs的特异性依赖于OXPHOS(氧化磷酸化)主导的代谢,以便在葡萄糖限制,乳酸丰富的环境中发挥作用(Angelin et al., 2017)。效应T细胞也可能受到AMPK激活所限制,进而抑制mTORC1通路和分解代谢(Ma et al., 2017)。此外,DC(树突细胞)中的AMP依赖的蛋白激酶(AMPK)激活可能阻碍其诱导CD8+T细胞活化的能力(Challier et al., 2013; Giovanelli et al., 2019)。
(果友8九千七)
然而,AMP依赖的蛋白激酶(AMPK)的活性必须保持平衡,因为过量的AMP依赖的蛋白激酶(AMPK)可能会抑制效应T细胞效应,而使AMP依赖的蛋白激酶(AMPK)的激活失效使细胞对代谢应激敏感的同时,可能会增强糖酵解和炎症。为了支持这一作用,AMPK-a缺乏的巨噬细胞和树突细胞通过增加炎症细胞因子的产生和增强抗原呈递能力表现出增强的炎症功能,有利于促进Th1和Th17应答(Carroll et al., 2013)。同样,AMPKa缺乏的T细胞表现出糖酵解增强和IFN-g产生增加MacIver et al., 2011。然而,AMP依赖的蛋白激酶(AMPK)缺陷T细胞也变得对应激和凋亡更加敏感,如其在肺部炎症等情况下,体内的疗效下降所示(Blagih et al., 2015)。这些研究表明,AMP依赖的蛋白激酶(AMPK)的破坏已显示出促进炎症的前景,但可能会限制炎症细胞的存活,应谨慎平衡。二甲双胍是靶向AMP依赖的蛋白激酶(AMPK)最著名的药物之一,它能激活AMP依赖的蛋白激酶(AMPK)信号,被广泛用于治疗糖尿病。在小鼠中,二甲双胍治疗可以降低某些癌症的风险,并降低乳腺癌模型的肿瘤负担(Anisimov et al., 2005; Bodmer et al., 2010)。在人类队列中,尽管这些分析因糖尿病等共病而变得复杂,二甲双胍在结直肠癌患者中也显示出好的前景(Cheng et al., 2020)。AMP依赖的蛋白激酶(AMPK)激活被认为是通过减缓肿瘤生长来部分减轻肿瘤负担,同时支持TME中TIL的扩增和存活(Blagih et al., 2015; Eikawa et al., 2015; Wegiel et al., 2018)。值得注意的是,二甲双胍还可以通过阻断磷酸果糖激酶-1(PFK1)(Hu et al., 2019)和HIF-1a(肿瘤细胞低氧反应的重要媒介)诱导的其他糖酵解酶来降低癌细胞的糖酵解通量(Tyszka-Czochara et al., 2018)。在AMP依赖的蛋白激酶(AMPK)缺陷白血病的多种小鼠模型中,观察到肿瘤细胞死亡和小鼠存活增加(Chan et al., 2017; Kishton et al., 2016; Saito et al., 2015)。尽管AMP依赖的蛋白激酶(AMPK)信号可能支持抑制性免疫细胞群的存活,但它也可能减轻细胞压力以支持癌细胞存活。AMP依赖的蛋白激酶(AMPK)调控的矛盾结果表明AMP依赖的蛋白激酶(AMPK)通路在TME中发挥着着重要作用,尽管它调节了癌细胞应激和抗肿瘤免疫的背景和时间依赖性平衡。因此,AMP依赖的蛋白激酶(AMPK)靶向治疗必须同时考虑对癌细胞死亡的直接影响以及TME内的免疫细胞表型的影响。

未完待续!
编辑:榴莲
审校:芒果