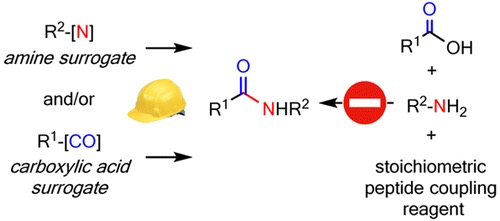
酸酐偶联法
通过混合酸酐的方法制备酰胺,与经酰氯活化方法类似,均为古老并且实用的方法。
1)混合羧酸酐,例如使用乙酸酐或特戊酰氯制备。主要缺点有:化学区域选择性,可以通过增大空间位阻解决(特戊酰氯);歧化生成两种对称的混合酸酐,可以通过生成混合酸酐后立即与胺反应消除。2)混合碳酸酐,使用氯甲酸酯类或EEDQ试剂制备。碳酸酐的两个羰基是不相等的,胺通常加成到需要的羰基上,因为不需要的羰基的亲电性较低(碳酸盐)。这就是为什么氯甲酸乙酯在缺乏空间位阻的情况下,对所需羰基上的酰胺键形成具有良好的选择性的原因。
EEDQ与羧酸反应,先脱去一分子乙醇,接着在羧酸根进攻下脱去喹啉,生成混合碳酸酐(与氯甲酸乙酯制备的混合碳酸酐一致),随后再与胺进行缩合,得到相应的酰胺,同时生成当量的二氧化碳与乙醇。混合羧酸酐或混合碳酸酐的制备,通常是羧酸与碱(NMM或N-甲基哌啶)混合在溶剂中,加入酸酐试剂,制备得到的酸酐不经分离,直接与胺进行偶联。
乙酸酐通常直接用于胺乙酰化。乙酸酐制备得到的混合羧酸酐羰基区域选择性差,一般不用于羧酸活化。
特戊酰氯(PivCl)由于其较大的空间位阻,有较多报道用于混合羧酸酐法大量制备酰胺。并且,特戊酰氯(PivCl)价格便宜、商品化、副产物为水溶性特戊酸,因此工业应用广泛。但是,需要注意特戊酰氯(PivCl)是刺激物,皮肤接触会导致化学灼伤,因此使用时候需要注意做好防护和通风。氯甲酸乙酯(ECF)也是可用于大量制备酰胺的偶联试剂,主要优势在于其价格便宜。但是该试剂毒性大,易挥发。
氯甲酸异丁酯(IBCF)也是大量制备酰胺键的通用偶联试剂。虽然价格较高,但是毒性低,并且生成的混合羧酸酐与胺反应的选择性高。
Boc酸酐在大量制备酰胺中应用不多。该化合物为低熔点(23 °C)固体,通常将其融化为溶液状态而更容易使用。EEDQ与CDI和碳二亚胺相似,不需要额外的碱,制备酰胺。该试剂价格相对低廉,使用广泛,其偶联副产物(喹啉、乙酸乙酯)可被萃取到酸性水溶液中。磺酸基混合酸酐
黄酰氯(MsCl)尚未普遍用于大规模的酰胺偶联。MsCl具有剧毒、腐蚀性、对水分敏感和催泪剂,这些特性使得在工业过程中处理这种试剂具有挑战性。然而,MsCl相对便宜,并已被证明抑制手性酸偶联的异构化。对甲基苯磺酸(TsCl)甚至比MsCl更不常用于大规模的酰胺制备。TsCl很容易买到,价格便宜,但也有毒和吸湿磷酸基混合酸酐
第一个混合羧酸-磷酸酐的例子是在1972年报道的,使用的是二苯磷酸叠氮。然而,在大量文献中还没有发现使用这种试剂进行酸活化的例子,很可能是由于叠氮基团的成本高、能量高和毒性。另一方面,更适合的试剂,如N-丙膦酸酐(T3P)和乙基甲基膦酸酐(EMPA)(图4)已被工艺化学组用于合成候选药物。
N-丙膦酸酐,通常称为T3P(或PPA),是1980年开发的肽偶联试剂。十年前,已在大规模酰胺偶联中使用该试剂。T3P在工业规模上使用的原因有:毒性低(LD50 >2000 mg/kg),保质期长,稳定性好,操作方便(可商品购买的50%的有机溶剂溶液,如乙酸乙酯、DMF或甲腈),水溶性副产物可以通过水萃取除去。乙基甲基膦酸酐(EMPA)作为酰胺偶联剂,远不如T3P的规模。EMPA增强的水解稳定性,允许在水介质中合成肽;然而,其相对较高的毒性(LD50 = 7 mg/kg)和在药物中低含量的要求,限制了该试剂在工业规模上的使用。
CDI
CDI,即1,1 ' -羰基二咪唑,是一种非常有效的酰胺类大规模偶联试剂。它是一种晶体,价格便宜,以公斤计广泛供应,相对安全,它的副产物咪唑很容易被水溶液净化。
首先,羧酸质子转移至咪唑生成离子对,然后脱去一分子咪唑生成混合羧酸酐,接着咪唑作用下脱去二氧化碳和咪唑,生成酰基咪唑(该化合物可以分离),再与胺进行偶联缩合,得到酰胺产物,同时释放咪唑。羧酸与CDI反应生成瞬时混合酸酐,该酸酐重新排列为羰基咪唑烷。这种羰基咪唑烷相对容易处理,必要时可以分离。将初始的混合酸酐重新排列成羰基咪唑胺,生成的二氧化碳当量可以加速随后的酰胺偶联速率。另一个优点是,CDI促进的偶联通常不需要额外的碱基来执行,因为生成的咪唑可以提供这个功能。这种试剂的一个缺点是其对空气湿度敏感。活化酯偶联

1955年,Sheehan和Hess在首次报道利用DCC(N,N ' -双环己基碳二酰亚胺)形成肽和其他酰胺键。从那时起,碳二酰亚胺就成为高效制备酰胺键的一类极其重要的化合物。许多碳二亚胺已作为偶联试剂进行了研究,但基于可用性、成本、分离和环境考虑,只有少数用于常规大规模使用(图5)。这些化合物通常是皮肤敏感的,使用需要小心。当选择碳二亚胺时,主要考虑是后处理,因为去除尿素副产品的方法可能有很大的不同。例如,DCC中的二环己脲在大多数有机溶剂中溶解度非常有限,因此通常通过过滤去除。DIC中的二异丙脲在二氯甲烷中有合理的溶解度,通常用水萃取法去除。最后,EDC的副产物尿素是水溶性的,可以通过水洗去除。
首先从羧酸向碳二酰亚胺上的弱碱性氮转移质子,得到离子对,所得到的羧酸阴离子加成形成O-酰异脲,这是一种反应性很强的酰化剂,能与胺迅速发生胺解反应,得到所需的酰胺。另外,过量的羧酸可以与邻酰异脲反应生成对称酸酐,这也是一种良好的酰化剂。氨基与对称酸酐的酰化反应也产生与起始酸等价的产物。邻酰基异脲还可以通过分子内酰基转移重新排列得到N-酰基脲,这是一个不可逆的途径,不再生成所需的酰胺。使用辅助亲核试剂是一种常见的做法,以减少N-酰基脲的形成和通过增加酰胺偶联的总速率减少立体中心外酰化。虽然已经报道了许多添加剂,但1-羟基苯并三唑(HOBt)是迄今为止在化学计量或催化方式下用于碳二亚胺介导的反应中最常用的添加剂。
DDC广泛应用于药物中酰胺键的制备。相对而言,DIC则较少报道于酰胺大量制备。
EDC则是目前碳二亚胺中最广泛应用于药物中酰胺键合成。尿素副产物是水溶性的,可以在水溶液中去除,这比DCC和DIC等碳二亚胺具有明显的优势。然而,这种试剂的高成本是一个问题,特别是在后期开发。
Phosphonium Salts
BOP((苯并三唑-1-基氧基)三(二甲胺基)六氟磷酸氢铵(Castro试剂,图7)是第一个引入的以HoBt基溴盐为基础的酰胺键形成的试剂,以避免与碳二亚胺试剂发生双酰化和其他副反应。
尽管BOP促进了快速偶联并在其结构中含有抑制外源化的HOBt,但由于会产生一种相当于六甲基磷酰胺(HMPA)的已知致癌物,BOP在工艺化学中的应用有限。
羧酸于有机碱生成离子对,随后羧酸根与BOP生成酰氧膦中间体,脱下的HOBt负离子进攻羰基碳,脱下HMPA同时生成活性酯,最后与胺偶联得到酰胺。作为替代,开发了PyBOP((苯并三唑-1-yloxy)三(吡rrolidine)六氟磷酸氢铵(图7),它产生更温和的膦氧化物,但这种试剂相对昂贵,并没有发现描述其大规模使用的例子。另一个重要的考虑是苯并三唑部分的存在,这需要进行彻底的安全性研究以确定该方案(在药物制备)的可行性。
Guanidinium and Uronium Salts
基于苯并三唑的HBTU在BOP应用与酰胺键制备不久被开发(图8),自那以后,大量的胍盐和脲盐被报告。这些试剂能快速形成酰胺键,并对肽合成中位阻氨基酸的偶联非常有用。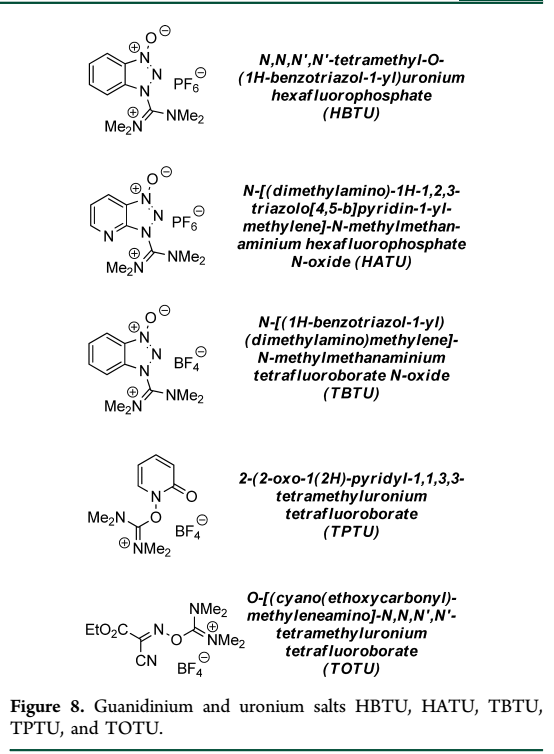
一些原因限制膦这些化学试剂的应用,包括高分子量(这意味着每摩尔成本高),生成成细胞毒性副产品,和高能官能团的存在。然而,这些试剂可以在存在敏感官能团下进行偶联,同时反应条件温和。
从图式8中,我们可以得知,HBTU制备酰胺的机理与BOP是非常类似的。最终都是经过生成HOBt活性酯再与胺进行缩合得到酰胺产物。
Triazine-Based Coupling Reagents

三氯氰(1,3,5-三氯三嗪)是一种高度反应性的偶联试剂,每年通过氯化氰三聚反应产生数十万公吨的工业规模。因此,它是一种最经济有效的形成酰胺键的偶联剂。由于分子上存在三个氯原子作为离去基团,这种试剂可以在亚化学计量量上使用。
三聚氰氯的酸活化机理一般被描述为通过酸氯化物形成的过程(图式9)。该酸必须是羧酸的形式来取代氯并形成活性酯中间体,然后与氯反应生成所需的酰氯和副产物1,3-二氯-5-羟三嗪,后者与另外两分子羧酸反应可以产生氰酸作为副产物。
Et3N和NMM通常与三聚氯胺一起使用,但廉价的无机碱如NaOH也可以使用,并且可以在有水的情况下进行反应。所产生的氰尿酸副产品可以很容易地去除,通过过滤或洗涤。尽管三聚氰胺有这些明显的优点,但它在制药工业中很少受到制法化学家的关注。在Na2CO3为碱的情况下,由三聚氰氯和2倍的甲醇反应合成CDMT,即2-氯-4,6-二甲氧基-1,3,5-三嗪。它是一种稳定的晶体固体,可以在市场上批量购买。该试剂已被证明能有效地减少外旋异构化,并对空间受阻的伯烷基、仲烷基和芳胺起作用。DMTMM,即4-(4,6-二甲氧基-1,3,5-三嗪-2-yl)-4-甲基氯化铵,是一种空气和水稳定的固体,可以用NMM处理CDMT,但在过程化学中很少使用。该试剂的一个优点是,它可以在醇类或水溶液中形成酰胺键,而不产生相应的酯类或水解产物。DMTMM活化提供了副产物为NMM·HCl的活化酯。该试剂可加入酸和胺偶联剂的混合物中。在DMTMM中加入羧酸盐释放NMM, NMM作为碱促进酰胺的偶联。1-羟基-3,5-二甲氧基三嗪是一种水溶性的副产物,可通过水处理去除。然而,正如前面提到的CDMT,每摩尔DMTMM的较高成本是其大规模应用的阻碍因素。
Coupling via Boron Species
近年来,硼衍生试剂作为酰胺键形成催化剂的应用显著增加。最初的报告要求使用化学计量量的硼试剂,但最近,山本和同事描述了第一个使用亚化学计量量的硼试剂。许多硼基试剂被报道用于过程化学之外的酰胺键形成。然而,尽管有许多选择,硼酸显然是一个非常理想的试剂,因为它是廉价的,并显示了优秀的原子经济(图10)。此外,反应完成后,可将水溶性试剂萃取到水溶液中。另一方面,硼酸的缺点是高剂量的生殖毒性,欧洲化学署可能将其列入高度关注的物质清单,以限制其在欧洲的使用。
用于形成酰胺键的硼试剂在过程化学中使用有限,只发现了硼酸和3-硝基硼酸的例子。
羧酸和硼酸的反应在失去一分子水之后形成一种活化的混合酸酐中间体(水必须被共沸水移去以使平衡向酰化硼酸中间体移动)。这种中间产物然后与胺反应生成酰胺产物并再生硼酸,重新进行催化循环。其他方法
通过酯的胺解、转酰胺化、布朗特酸催化制备酰胺也有报道。同时,目前有很多催化法被报道用于酰胺的合成。
实例


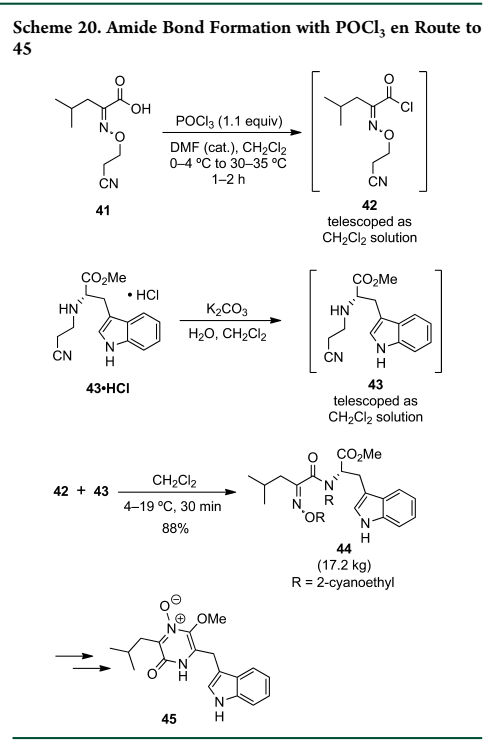
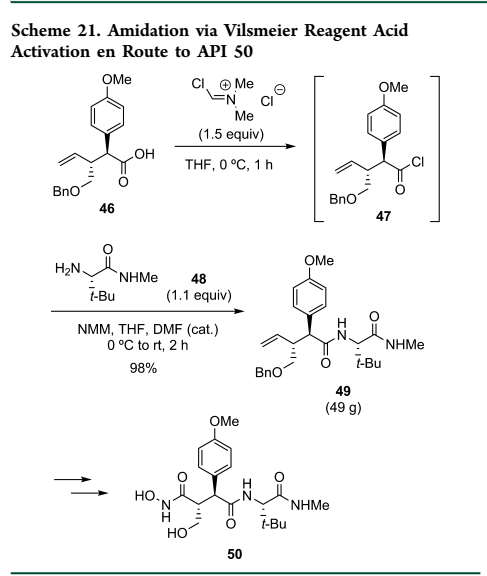
2)通过混合酸酐法

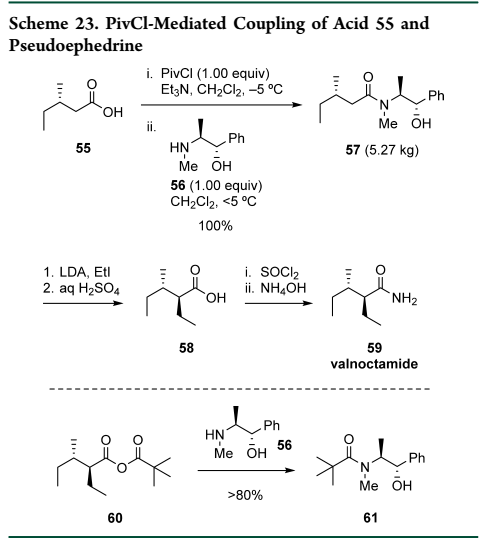

3)Coupling via Sulfonate-Based Mixed Anhydride
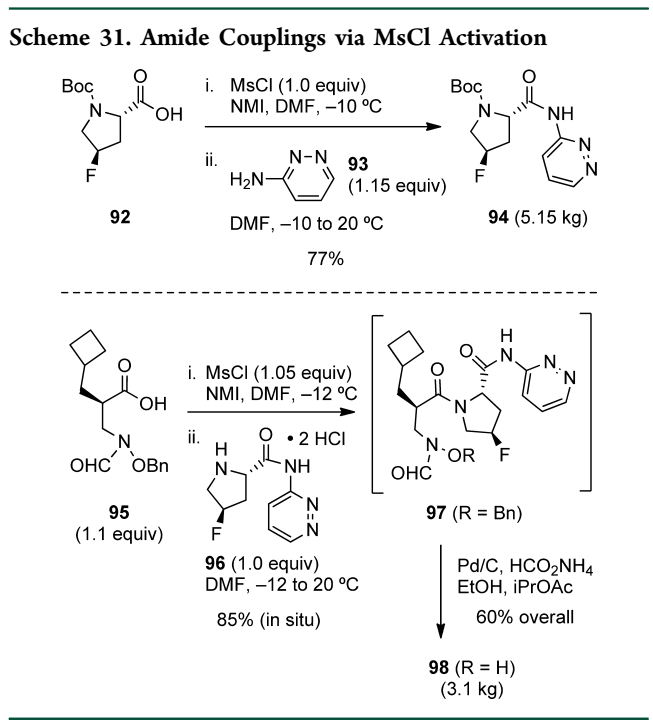

4)Coupling via Phosphorus-Based Mixed Anhydride

5)Coupling via CDI.

6)Coupling via Carbodiimide

7)Coupling via Phosphonium Salt.
8)Coupling via Guanidinium and Uronium Salt
9)Coupling via Triazine Reagent.
10)Coupling via Boron Reagent
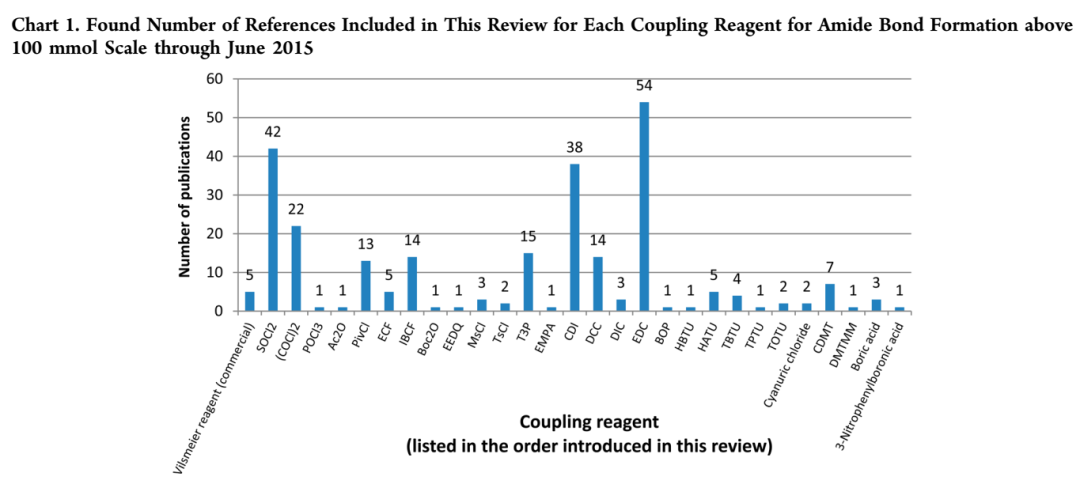
酰胺键的形成在过程化学中对候选药物的合成的重要性怎么强调都不过分。工艺化学家拥有广泛的生产酰胺的方法,但由于大规模操作的限制,只能选择更狭窄的试剂领域。基于本综述中包含的示例数量,首选的酸激活试剂是EDC、SOCl2、CDI和(COCl)2,其次是PivCl、IBCF、T3P和DCC。
无论选择何种试剂,酰胺键的形成无疑将继续是合成药物过程化学中最重要的转变之一。社会和经济压力已经对驾驶更安全、更环保、更便宜的试剂和方法产生了明显的影响。我们相信,如果这些新技术被证明是可扩展的,那么它们中的许多将被常规地整合到大规模的API合成操作中
Ref
Org. Process Res. Dev. 2016, 20, 2, 140–177